Περίληψη
Ο καρκίνος του πνεύμονα αποτελεί μια σύγχρονη μάστιγα/επιδημία, η οποία οφείλεται σε έκθεση στον καπνό των τσιγάρων και ευθύνεται για το 25% των θανάτων από καρκίνο που συμβαίνουν κάθε χρόνο. Η ορθολογική αντιμετώπιση του νεοπλάσματος βασίζεται στην απάντηση μιας σειράς ερωτημάτων, όπως είναι η ταυτοποίηση του ιστολογικού τύπου και του μοριακού προφίλ του νεοπλάσματος, η κατά το δυνατόν ακριβέστερη κλινική σταδιοποίηση με έμφαση στη σταδιοποίηση του μεσοθωρακίου για τους ασθενείς που πρόκειται να υποβληθούν σε χειρουργική θεραπεία και ο καθορισμός της ενδεδειγμένης θεραπείας για το συγκεκριμένο στάδιο ανάλογα με τη συνολική γενική κατάσταση του ασθενή. Το τελευταίο ερώτημα απαντάται σήμερα εντός ογκολογικού συμβουλίου πολλαπλών ειδικοτήτων, όπου θα συζητηθεί η κάθε περίπτωση ξεχωριστά. Η χειρουργική θεραπεία αποτελεί τον ακρογωνιαίο λίθο της θεραπείας στα πρώιμα στάδια (Ι, ΙΙ), με ή χωρίς χορήγηση επικουρικής θεραπείας. Η χορήγηση της επικουρικής θεραπείας θα βασιστεί στην τελική (παθολογοανατομική) σταδιοποίηση του νεοπλάσματος μετά την εκτομή. Στις ανεγχείρητες περιπτώσεις με τοπικά προχωρημένη νόσο (στάδιο ΙΙΙ), ο συνδυασμός χημειοθεραπείας, ακτινοθεραπείας και ανοσοθεραπείας έχει δώσει καλά αποτελέσματα τα τελευταία χρόνια. H εκτομή του όγκου μπορεί να γίνει με την κλασσική θωρακοτομή ή με τις ελάχιστα επεμβατικές τεχνικές, όπως η θωρακοσκοπική και η ρομποτική χειρουργική. Οι ελάχιστα επεμβατικές τεχνικές θεωρούνται σήμερα προτιμότερες στο στάδιο Ι, υπό την προϋπόθεση της τήρησης των αρχών της ογκολογικής χειρουργικής και των ανατομικών εκτομών του πνευμονικού παρεγχύματος.
Lung Cancer: Staging and minimally invasive approach.
Foroulis CN
Abstract
Lung cancer is the leading cause of death from cancer worldwide caused mainly by exposure of the patient to tobacco smoke for several years. The appropriate management of lung cancer depends on the correct determination of the histologic type and molecular profile with biopsy, on the meticulous clinical staging before treatment planning, especially mediastinal staging in patients who are candidates for surgery. The performance status of the patient needs exact determination with emphasis in heart and lung function. The treatment plan will be considered within a tumor multidisciplinary board where all the important details concerning the individual patient will be discussed. Surgery is the best treatment in earlier stages of lung cancer (I and II). The administration of adjuvant treatment after surgery depends on the final pathologic staging, while the combination of chemoradiotherapy with immunotherapy is currently considered to be the gold standard in inoperable locally advanced (stage III) cases. Tumor resection can be done with conventional thoracotomy or with minimally invasive techniques, such as thoracoscopic or robotic surgery. Minimally invasive techniques are recently adopted as the preferred techniques for the resection of early, stage I, non-small cell lung cancer. The principles of oncologic surgery and of anatomic lung parenchyma resection should not be sacrificed in order to complete lung cancer resection with a minimally invasive approach.
Εισαγωγή
Ο καρκίνος του πνεύμονα είναι το νεόπλασμα-μάστιγα του 20ου αιώνα και των αρχών του 21ου αιώνα.1 Πρόκειται για το 2ο σε συχνότητα κακόηθες νεόπλασμα (πέραν των νεοπλασμάτων του δέρματος), τόσο σε άνδρες (μετά τον καρκίνο του προστάτη), όσο και στις γυναίκες (μετά τον καρκίνο του μαστού). Ο καρκίνος του πνεύμονα ευθύνεται όμως για τους περισσότερους θανάτους από καρκίνο ανά έτος και στα δύο φύλα και συνολικά για το 25% των θανάτων από καρκίνο που συμβαίνουν κάθε χρόνο. [1] To κάπνισμα αποτελεί τον κυριότερο προδιαθεσικό παράγοντα για την ανάπτυξη του καρκίνου του πνεύμονα, αφού ευθύνεται για το 90% των περιπτώσεων.1-3
Ο καρκίνος του πνεύμονα μπορεί να είναι ασυμπτωματικός, οπότε μπορεί να αποτελεί τυχαίο εύρημα σε απεικονιστική εξέταση του θώρακα που γίνεται για άλλο λόγο. Το παραπάνω αποτελεί τον κανόνα σήμερα για το αδενοκαρκίνωμα που αναπτύσσεται ασυμπτωματικά στην περιφέρεια του πνεύμονα μέχρι να λάβει μεγάλο μέγεθος ή να δώσει συμπτωματικές μεταστάσεις (π.χ. στον εγκέφαλο). Όταν ο όγκος είναι συμπτωματικός, τα κυριότερα συμπτώματα είναι ο βήχας, το θωρακικό άλγος, τα αιμόφυρτα πτύελα, η δύσπνοια, η απώλεια όρεξης και σωματικού βάρους, το βράγχος φωνής, κ.ά. Αρκετά συχνά το νεόπλασμα εκδηλώνεται με συμπτωματολογία από την ύπαρξη απομακρυσμένων μεταστάσεων (π.χ. κεφαλαλγία, ζάλη και έμετοι σε εγκεφαλικές μεταστάσεις, οστικά άλγη επί οστικών μεταστάσεων, κτλ), ενώ λείπουν τα συμπτώματα από του πνεύμονες. Επί υπόπτων συμπτωμάτων ακολουθεί ακτινογραφικός έλεγχος του θώρακα, ο οποίος συνήθως αναδεικνύει την ύποπτη βλάβη σαν σκίαση ή όζο στον πνεύμονα, με άλλοτε άλλα απεικονιστικά χαρακτηριστικά.3
Η ανεύρεση σκίασης στον πνεύμονα πρέπει να διερευνηθεί προς την κατεύθυνση της επιβεβαίωσης ή του αποκλεισμού της ύπαρξης κακοήθους νεοπλάσματος, το οποίο αποτελεί το 1ο βασικό διαγνωστικό ερώτημα. Για το σκοπό αυτό απαιτείται η λήψη βιοπτικού υλικού από τη σκίαση. Η λήψη του βιοπτικού υλικού μπορεί να γίνει με την κλασσική ινοπτική βρογχοσκόπηση σε κεντρικώς εντοπιζόμενα στο πνευμονικό παρέγχυμα νεοπλάσματα (εγγύς των πνευμονικών πυλών) ή με διατοιχωματική, κατευθυνόμενη από τον αξονικό τομογράφο λήψη βιοψίας με λεπτή ή trucut βελόνη σε περιφερικά εντοπιζόμενη στο πνευμονικό παρέγχυμα μάζα ή όζο. Τελευταία έχει αναπτυχθεί και η βρογχοσκόπηση με ηλεκτρομαγνητική καθοδήγηση, η οποία σε συνδυασμό ή όχι με το radial EBUS (ενδοσκοπικό υπερηχογράφημα/endobronchial ultrasound) μπορεί να προσεγγίσει για λήψη βιοψίας βλάβες εντοπιζόμενες στην ενδιάμεση ζώνη, αλλά ακόμη και περιφερικά εντοπιζόμενες βλάβες. Σημειώνεται τέλος ότι οι κυτταρολογικές εξετάσεις δεν θεωρούνται σήμερα επαρκές διαγνωστικό υλικό για την έναρξη θεραπείας στον καρκίνο του πνεύμονα.
Σε συνέχεια του 1ου ερωτήματος έρχεται το 2ο βασικό διαγνωστικό ερώτημα που πρέπει να απαντηθεί, δηλαδή αν πρόκειται για μικροκυτταρικό (ΜΚΠ) ή μη μικροκυτταρικό καρκίνωμα του πνεύμονα (ΜΜΚΠ), αφού το ΜΚΠ δεν επιδέχεται συνήθως χειρουργικής θεραπείας, ει μη μόνο αν πρόκειται για τυχαίο εύρημα με τη μορφή μιας μονήρους νομισματοειδούς σκίασης του πνεύμονα. O συχνότερος τύπος του ΜΜΚΠ σήμερα είναι μακράν το αδενοκαρκίνωμα, το οποίο αποτελεί το 40% του συνόλου των καρκινωμάτων του πνεύμονα και το 60% των ΜΜΚΠ, εντοπίζεται δε σε ποσοστό >70% στην περιφέρεια του πνευμονικού παρεγχύματος. Η συχνότητα του πλακώδους καρκινώματος από την άλλη υποχώρησε σημαντικά και αποτελεί το 20% του συνόλου των καρκίνων του πνεύμονα, γεγονός που αντανακλά τις αλλαγές στην καπνιστική συνήθεια με τη μεγάλη διάδοση των ελαφρών (light) τσιγάρων. Οι νευροενδοκρινείς όγκοι αφορούν το 20-25% των καρκινωμάτων του πνεύμονα, με το μικροκυτταρικό καρκίνωμα να αποτελεί το 3ο σε συχνότητα καρκίνωμα του πνεύμονα (10-15%) του συνόλου.2, 3
Το 3ο βασικό προθεραπευτικό ερώτημα στον καρκίνο του πνεύμονα είναι το ποιο είναι το ακριβές στάδιο του νεοπλάσματος (κλινική σταδιοποίηση). Εφόσον πιστοποιηθεί μικροκυτταρικό καρκίνωμα στο βιοπτικό υλικό, το οποίο είναι συνήθως προχωρημένο τοπικά ή παρουσιάζει απομακρυσμένες μεταστάσεις κατά την ώρα της διάγνωσης, η σταδιοποίηση θα γίνει με τις κλασσικές αξονικές τομογραφίες άνω, κάτω κοιλίας και εγκεφάλου, σε συνδυασμό με το σπινθηρογράφημα οστών. Η σταδιοποίηση του μικροκυτταρικού καρκινώματος είναι αδρή και περιλαμβάνει την περιορισμένη νόσο (εξάπλωση εντός του ημιθωρακίου) και τη γενικευμένη νόσο (εξάπλωση πέραν του ημιθωρακίου ή ανεύρεση σύστοιχης με τον όγκο πλευριτικής συλλογής με θετική κυτταρολογική εξέταση).3 Στη συνέχεια ο ασθενής θα οδηγηθεί στον Παθολόγο Ογκολόγο για έναρξη της κατάλληλης χημειοθεραπείας, με ή χωρίς ακτινοθεραπεία στον εγκέφαλο. Εφόσον όμως στη βιοψία διαπιστωθεί ΜΜΚΠ, θα ακολουθήσει η ενδελεχής κλινική σταδιοποίηση με το σύστημα ΤΝΜ (clinical TNM/c-TNM), η οποία βασίζεται σήμερα στο σπινθηρογράφημα ποζιτρονίων (PET-CT scan) και τη μαγνητική ή αξονική τομογραφία εγκεφάλου στις περιπτώσεις που μελετάται η εφαρμογή χειρουργικής θεραπείας. Στις υπόλοιπες περιπτώσεις που κρίνονται ανεγχείρητες λόγω τοπικής επέκτασης ή υπάρχει μεταστατική νόσος ή ο ασθενής δεν είναι ικανός να υποβληθεί σε χειρουργική επέμβαση, θα γίνει η συμβατική σταδιοποίηση, όπως γίνεται στο μικροκυτταρικό καρκίνωμα. Η τελευταία σταδιοποίηση του καρκίνου του πνεύμονα του 2017 παρουσιάζεται αναλυτικά στη συνέχεια και συνοπτικά στον Πίνακα 1.4
H Νεότερη Σταδιοποίηση του Καρκίνου του Πνεύμονα (2017)
Παράμετρος Τ (Πρωτοπαθής Όγκος)
-Όγκος Τ0: Χωρίς πρωτοπαθή όγκο
Τis: Καρκίνωμα in situ (για αδενοκαρκινώματα και πλακώδη καρκινώματα)
–Όγκοι Τ1
Όγκοι ≤ 3 εκατοστά
- Τ1a (mi): Αδενοκαρκίνωμα με ελάχιστη διήθηση (minimally invasive adenocarcinoma)
- T1a ss: Όγκος με επιφανειακή επέκταση (superficial spreading): Όγκος με επιφανειακή επέκταση, οποιουδήποτε μεγέθους, ο οποίος όμως περιορίζεται εντός του τοιχώματος του βρόγχου ή της τραχείας
- Τ1a: Όγκος ≤ 1 εκατοστό
- Τ1b: Όγκος > 1 εκατοστό, αλλά ≤ 2 εκατοστά
- Τ1c: Όγκος > 2 εκατοστά, αλλά ≤ 3 εκατοστά
-Όγκοι Τ2
- Όγκος > 3 εκατοστά, αλλά ≤ 5 εκατοστά
- ή όγκος που διηθεί το σπλαχνικό υπεζωκότα (Τ2visc pl)
- ή όγκος που διηθεί τον κύριο (στελεχιαίο) βρόγχο αλλά όχι την κύρια τρόπιδα ή όγκος που προκαλεί ατελεκτασία που επεκτείνεται στην πύλη του πνεύμονα (T2centr)
- T2a: Όγκος > 3 εκατοστά, αλλά ≤ 4 εκατοστά
- T2b: Όγκος > 4 εκατοστά, αλλά ≤ 5 εκατοστά
-Όγκοι Τ3
- Όγκος > 5εκατοστά, αλλά ≤ 7 εκατοστά (T3>5-7) ή όγκος που διηθεί το θωρακικό τοίχωμα, το περικάρδιο, το φρενικό νεύρο (Τ3inv) ή ύπαρξη δορυφόρων οζιδίων στον ίδιο λοβό με αυτόν που φέρει τον πρωτοπαθή όγκο (Τ3satell)
-Όγκοι Τ4
- Όγκος > 7 εκατοστά (Τ4>7) ή όγκος που διηθεί το μεσοθωράκιο, το διάφραγμα, την καρδιά, τα μεγάλα αγγεία, το παλίνδρομο λαρυγγικό νεύρο, την κύρια τρόπιδα, την τραχεία, τον οισοφάγο, τη σπονδυλική στήλη (Τ4inv) ή ύπαρξη δορυφόρων οζιδίων στον ίδιο πνεύμονα, αλλά σε διαφορετικό λοβό από αυτόν που φέρει τον πρωτοπαθή όγκο (Τ4ips node)
Σημαντική σημείωση: H μέγιστη διάμετρος του συμπαγούς όγκου στις απεικονιστικές τεχνικές (κλινική σταδιοποίηση, c-stage) ή η μέγιστη διάμετρος του διηθητικού τμήματος στην παθολογοανατομική σταδιοποίηση (p-stage) χρησιμοποιούνται για τον καθορισμό του σταδίου Τ.
Παράμετρος Ν (Περιοχικοί Λεμφαδένες)
- Ν0: Χωρίς προσβολή των περιοχικών λεμφαδένων
- Ν1: Μετάσταση στους σύστοιχους ενδοπνευμονικούς και πυλαίους λεμφαδένες
- Ν2: Μετάσταση στους σύστοιχους (ομόπλευρους) με τον όγκο μεσοθωρακικούς/υποτροπιδικούς λεμφαδένες
- Ν3: Μετάσταση στους ετερόπλευρους μεσοθωρακικούς/ πυλαίους λεμφαδένες ή στους υπερκλείδιους λεμφαδένες
H κατά συνέχεια ιστού επέκταση του όγκου σε παρακείμενο λεμφαδένα θεωρείται ότι αποτελεί λεμφαδενική προσβολή
Παράμετρος Μ (Απομακρυσμένες Μεταστάσεις)
- M0: Δεν υπάρχουν απομακρυσμένες μεταστάσεις
- M1a: Κακοήθους αιτιολογίας πλευρική/περικαρδιακή συλλογήc ή οζίδια στον υπεζωκότα ή το περικάρδιο (Μ1aPl Dissem) ή νεοπλασματικά οζίδια σε λοβό του αντίθετου πνεύμονα από αυτόν που φιλοξενεί τον πρωτοπαθή όγκο (Μ1aContr Nod).
Εξαιρούνται πλευριτικές συλλογές οι οποίες δεν είναι αιμορραγικές, έχουν αρνητική κυτταρολογική εξέταση, είναι διιδρωματικές και τέλος, εκτιμάται κλινικώς ότι δεν οφείλονται στο καρκίνωμα (π.χ. ατελεκτασία συστοίχου πνεύμονος)
- M1b: Μονήρης εξωθωρακική μετάσταση (M1bSingle)
- M1c: Πολλαπλές εξωθωρακικές μεταστάσεις σε ένα ή περισσότερα όργανα (M1cmulti)
- ΤΧ και ΝΧ: Οι παράμετροι Τ και Ν δε μπορούν να εκτιμηθούν καρκίνο του πνεύμονα
| N0 | N1 | N2 | N3 | ||
| T1 | Τ1a | IA1 | IIB | IIIA | IIIB |
| Τ1b | IA2 | IIB | IIIA | IIIB | |
| Τ1c | IA3 | IIB | IIIA | IIIB | |
| T2 | T2Cent, Visc Pl | IB | IIB | IIIA | IIIB |
| T2a>3-4 | IB | IIB | IIIA | IIIB | |
| T2a>4-5 | IIA | IIB | IIIA | IIIB | |
| T3 | T3>5-7 | IIB | IIIA | IIIB | IIIC |
| T3inv | IIB | IIIA | IIIB | IIIC | |
| T3satell | IIB | IIIA | IIIB | IIIC | |
| T4 | T4>7 | IIIA | IIIA | IIIB | IIIC |
| T4inv | IIIA | IIIA | IIIB | IIIC | |
| T4ipsi nod | IIIA | IIIA | IIIB | IIIC | |
| M1 | M1aContr Nod | IVA | IVA | IVA | IVA |
| M1aPl Dissem | IVA | IVA | IVA | IVA | |
| M1bSingle | IVA | IVA | IVA | IVA | |
| M1cMulti | IVB | IVB | IVB | IVB |
Πίνακας 1: Η συνοπτική παρουσίαση της νεότερης σταδιοποίησης του 2017 για τον καρκίνο του πνεύμονα
Ιδιαίτερη σημασία στη κλινική προθεραπευτική σταδιοποίηση έχει η διάκριση ανάμεσα σε πρώιμη νόσο και τοπικά προχωρημένη νόσο, με κύριο κριτήριο την ύπαρξη ή όχι προσβολής των λεμφαδένων του μεσοθωρακίου από το νεόπλασμα και τη διήθηση των πέριξ δομών και ιστών. Τα βήματα της σταδιοποίησης παρουσιάζονται λεπτομερώς στον Αλγόριθμο 1, όπου φαίνεται ότι η σύγχρονη σταδιοποίηση βασίζεται στο PET-CT scan, το ενδοβρογχικό υπερηχογράφημα (EBUS-TBNA), το διοισοφάγειο υπερηχογράφημα (EUS-TBNA) και την βιντεο-μεσοθωρακοσκόπηση.5
Αλγόριθμος 1: Η Σταδιοποίηση του Μεσοθωρακίου με Βάση τις Οδηγίες της European Society of Thoracic Surgeons (2014)
Μετά την ακριβή κατά το δυνατόν προθεραπευτική σταδιοποίηση στο ΜΜΚΠ, το 4ο βασικό προθεραπευτικό ερώτημα είναι ποια είναι η καταλληλότερη θεραπεία για το συγκεκριμένο ασθενή και το συγκεκριμένο νεόπλασμα. Η θεραπευτική αντιμετώπιση του ΜΜΚΠ εξαρτάται κυρίως από το στάδιο της νόσου και τη γενική κατάσταση του ασθενή, κυρίως όσον αφορά την ύπαρξη συνοσηρότητας που αφορά την καρδιά (στεφανιαία νόσος, καρδιακή ανεπάρκεια, κτλ.) και/ή την ύπαρξη κλινικά σημαντικής χρόνιας αποφρακτικής πνευμονοπάθειας, όπως προκύπτει από την κλινική εικόνα και την προεγχειρητική σπιρομέτρηση, η οποία αποτελεί απαραίτητη και ιδιαίτερα σημαντική προεγχειρητική εξέταση.6 H εκτίμηση της πιθανότητας θανάτου ενόψει επέμβασης εκτομής πνευμονικού παρεγχύματος για καρκίνο του πνεύμονα πρέπει να εκτιμάται σφαιρικά με το Thoracoscore, το οποίο πρέπει να εφαρμόζεται σε κάθε περίπτωση.7 Σημειώνεται ότι η πιθανή διενέργεια πνευμονεκτομής επιβαρύνει σημαντικά τον προγνωστικό δείκτη Thoracoscore.7 Πρέπει επίσης στο σημείο αυτό να τονιστεί ότι η ηλικία από μόνη της δεν αποτελεί αποτρεπτικό παράγοντα για τη χειρουργική θεραπεία σε ασθενείς χωρίς σοβαρά συνυπάρχοντα προβλήματα. Στον πρώιμο ΜΜΚΠ σταδίου Ι και ΙΙ η θεραπεία είναι καταρχήν χειρουργική και περιλαμβάνει την εκτομή του πνευμονικού παρεγχύματος που φέρει τον όγκο μετά των προσαγωγών και απαγωγών λεμφαγγείων και το συστηματικό λεμφαδενικό καθαρισμό στη μεσολόβιο σχισμή (λεμφική δεξαμενή του πνεύμονα) και στο μεσοθωράκιο. Η εκρίζωση του όγκου μπορεί να γίνει με λοβεκτομή, διλοβεκτομή (δεξιά μόνο), πνευμονεκτομή, περιορισμένη εκτομή και εκτεταμένη εκτομή σε επιλεγμένες περιπτώσεις. Η περιορισμένη εκτομή δύναται να λάβει τη μορφή της άτυπης σφηνοειδούς εκτομής σε μικρά περιφερικά νεοπλάσματα ή της ανατομικής τμηματεκτομής, η οποία συνίσταται στην εκρίζωση του όγκου με εκτομή ενός ή περισσότερων βρογχοπνευμονικών τμημάτων με ανατομικό τρόπο (εκτομή της γλωσσίδας, των κορυφαίων τμημάτων των κάτω λοβών, τριτμηματεκτομή του αριστερού ιδίως άνω λοβού, κ.ά.).3 Η εκτεταμένη εκτομή ορίζεται ως η συναφαίρεση του πνευμονικού παρεγχύματος που φέρει τον όγκο μαζί με τις πέριξ διηθημένες από το όγκο δομές, όπως το θωρακικό τοίχωμα, το ημιδιάφραγμα, τα σώματα των θωρακικών σπονδύλων, το περικάρδιο με ή χωρίς τμήμα του αριστερού κόλπου, κ.ά. Οι εκτεταμένες εκτομές εφαρμόζονται σε επιλεγμένες περιπτώσεις, σε ασθενείς οι οποίοι δεν έχουν παράγοντες κινδύνου και μετά από ενδελεχή αποκλεισμό της προσβολής των μεσοθωρακικών λεμφαδένων από το νεόπλασμα.8 Σε τοπικά προχωρημένα ΜΜΚΠ σταδίου ΙΙΙΑ μπορεί να εφαρμοστεί η χειρουργική θεραπεία σε επιλεγμένες περιπτώσεις, κυρίως μετά από τη χορήγηση θεραπείας εισαγωγής (induction treatment), η οποία μπορεί να λάβει τη μορφή της χημειοθεραπείας, της χημειο-ακτινοθεραπείας και λίαν προσφάτως της ανoσοθεραπείας.9,10 Στα ανεγχείρητα τοπικά προχωρημένα ΜΜΚΠ σταδίου ΙΙΙΑ, ΙΙΙΒ και ΙΙΙC η θεραπεία περιλαμβάνει την χημειο-ακτινοθεραπεία η οποία ακολουθείται από τη χορήγηση ανοσοθεραπείας για 12 μήνες, σύμφωνα με τα ιδιαίτερα θετικά πρόσφατα αποτελέσματα που έχουν προκύψει από τη μελέτη PACIFIC.11 Προσπελάσεις πέραν των καθιερωμένων απαιτούνται για τη ριζική χειρουργική εκτομή των όγκων που εντοπίζονται στην κορυφή των πνευμόνων και διηθούν κατά συνέχεια ιστών την είσοδο του θώρακα (Pancoast tumors), όπως οι Shaw-Paulson, Dartevelle, Masaoka, κ.ά. (Εικόνα 1) Οι όγκοι αυτοί προκαλούν χαρακτηριστική κλινική εικόνα (σύνδρομο Pancoast) και δύνανται να εκταμούν μετά από καλή απάντηση στη χημειο-ακτινοθεραπεία εισαγωγής, η οποία είναι απαραίτητη και επιβεβλημένη.3,12
Σημειώνεται με ιδιαίτερη έμφαση ότι η αντιμετώπιση του τοπικά προχωρημένου ΜΜΚΠ, η οποία απαιτεί τη λήψη σοβαρών και δύσκολων αποφάσεων για τον ασθενή, πρέπει να αποφασίζεται πάντα εντός ογκολογικού συμβουλίου πολλαπλών ειδικοτήτων (MultiDisciplinary Team/MDT).9
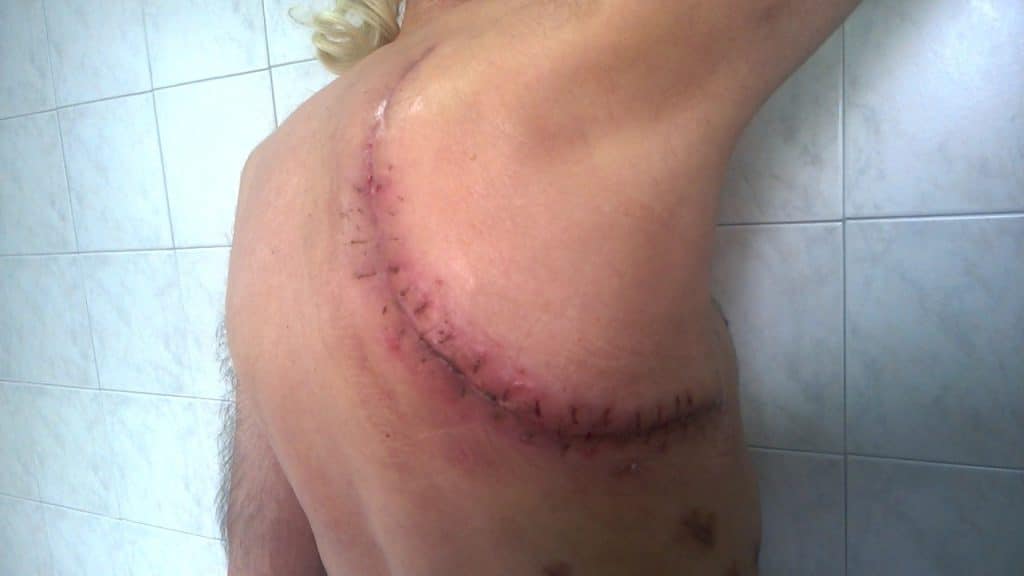
Εικόνα 1:Τομή Shaw-Paulson για τη ριζική χειρουργική αφαίρεση όγκου Pancoast μετά από χημειο-ακτινοθεραπεία εισαγωγής (Από την Καρδιοθωρακοχειρουργική Κλινική του ΑΠΘ).
Η παθολογοανατομική εξέταση και η ανοσοϊστοχημική μελέτη του παρασκευάσματος της χειρουργικής εκτομής του όγκου και των εξαιρεθέντων λεμφαδένων του μεσοθωρακίου θα καθορίσει το τελικό ή παθολογοανατομικό στάδιο της νόσου (pathologic-TNM/p-TNM). Η παθολογοανατομική εξέταση θα καθορίσει επίσης τη ριζικότητα της εκτομής, δηλαδή αν πρόκειται για εκτομή χωρίς υπολειμματική νόσο (ριζική εκτομή/R0) ή την ατελή εκτομή (R1 ή R2 ανάλογα με την ύπαρξη μικροσκοπικών ή μακροσκοπικών ορίων εκτομής διηθημένων από τον όγκο αντίστοιχα). Η τελική σταδιοποίηση θα καθορίσει την ανάγκη για περαιτέρω επικουρική θεραπεία.3 Η ανάλυση των μοριακών δεικτών του νεοπλάσματος (έκφραση PDL-1, ανίχνευση μεταλλάξεων EGFR, ALK, και άλλων) είναι ιδιαίτερα σημαντική σήμερα, αφού φαίνεται ότι και σε αρχικού σταδίου νεοπλάσματα κάποιοι ασθενείς θα ωφεληθούν από τη χορήγηση στοχευμένης θεραπείας, με βάση την ύπαρξη των παραπάνω αναφερομένων μεταλλάξεων.13
Οι ανατομικές εκτομές που απαιτούνται για την εκρίζωση του καρκίνου του πνεύμονα μπορούν να γίνουν με την κλασσική προσθιοπλάγια ή οπισθοπλάγια θωρακοτομή και με τις ελάχιστα επεμβατικές τεχνικές, δηλαδή τη θωρακοσκοπική τεχνική (Video-Assisted Thoracic Surgery/VATS) και τη ρομποτική προσπέλαση (Robotic-Assisted Thoracic Surgery/RATS). Οι ελάχιστα επεμβατικές τεχνικές (VATS, RATS) περιλαμβάνουν τη διενέργεια μιας μικρής βοηθητικής θωρακοτομής (utility thoracotomy) για διευκόλυνση των χειρισμών και την έξοδο του παρασκευάσματος από τη θωρακική κοιλότητα. Η βοηθητική τομή πρέπει να είναι μικρότερη από 7 εκ., ειδάλλως η επέμβαση δε μπορεί να χαρακτηριστεί ως ελάχιστα επεμβατική. (Εικόνα 2) Οι σύγχρονοι ατραυματικοί διαστολείς εκ πολυουρεθάνης (wound protectors) έχουν διευκολύνει τα μέγιστα στη διενέργεια των θωρακοσκοπικών επεμβάσεων. (Εικόνα 3)
Εικόνα 2: Δύο περιπτώσεις ελάχιστα επεμβατικής εκτομής) πρώιμων καρκινωμάτων του πνεύμονα. Σημειώνεται η βοηθητική θωρακοτομή. (Από την Καρδιοθωρακοχειρουργική Κλινική του Α.Π.Θ.)
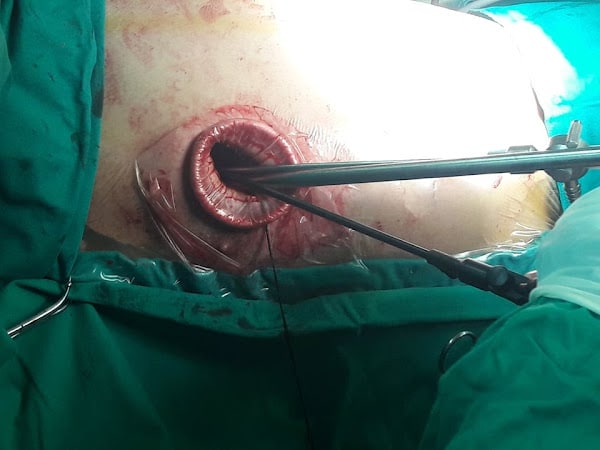
Εικόνα 3: Θωρακοσκοπική εκτομή περιφερικού όζου του πνεύμονα με μια πύλη εισόδου στο θωρακικό τοίχωμα, με τη βοήθεια του ατραυματικού διαστολέα από πολυουρεθάνη. (Από την Καρδιοθωρακοχειρουργική Κλινική του Α.Π.Θ.)
Κάθε προσπέλαση έχει τα δικά της πλεονεκτήματα και μειονεκτήματα. Οι ελάχιστα επεμβατικές τεχνικές είναι προτιμότερες στα πρώιμα στάδια του ΜΜΚΠ. Η VATS μπορεί να εφαρμοστεί σαν προσπέλαση εκλογής σε νεοπλάσματα σταδίου Ι (δηλ. < 4εκ. στη μέγιστη διάμετρο), όταν έχουν περιφερική εντόπιση, όταν δεν υπάρχουν ανατομικές παραλλαγές και όταν δεν υπάρχει λεμφαδενοπάθεια στη μεσολόβιο σχισμή ή την πύλη του πνεύμονα. Απαραίτητη προϋπόθεση είναι η τήρηση των αρχών της ογκολογικής χειρουργικής και των αρχών της ανατομικής λοβεκτομής και του συστηματικού λεμφαδενικού καθαρισμού του μεσοθωρακίου, που δεν πρέπει να θυσιαστούν προκειμένου η επέμβαση να γίνει με ελάχιστα επεμβατική προσπέλαση.9 Τα πλεονεκτήματα της θωρακοσκοπικής προσπέλασης είναι ο λιγότερος μετεγχειρητικός πόνος και η μικρότερη παραμονή στο Νοσοκομείο, ενώ το ποσοστό των μετεγχειρητικών επιπλοκών δε φαίνεται να διαφέρει ανάμεσα στη θωρακοσκοπική και την ανοιχτή προσπέλαση. Τα πλεονεκτήματα της ρομποτικής προσπέλασης έναντι της VATS είναι η τρισδιάστατη όραση με απόλυτη ευκρίνεια, η μεγαλύτερη ακρίβεια των κινήσεων λόγω της τεχνολογίας endo-wrist του ρομποτικού συστήματος και ο ελάχιστος μετεγχειρητικός πόνος. Τα μειονεκτήματα της ρομποτικής προσπέλασης είναι το πολύ υψηλό κόστος των επεμβάσεων, η περιορισμένη επί του παρόντος διαθεσιμότητα των ρομποτικών συστημάτων και ο αυξημένος χρόνος που απαιτείται για τη διενέργεια των επεμβάσεων.3,14,15
Η θωρακοσκοπική χειρουργική (VATS) έχει επιπλέον σημαντικές εφαρμογές στην αντιμετώπιση του καρκίνου του πνεύμονα. Η VATS εφαρμόζεται στην καθημερινή κλινική πρακτική για διαγνωστικούς σκοπούς (λήψη βιοπτικού υλικού σε επιλεγμένες περιπτώσεις, στην εκτομή προς βιοψία περιφερικών νομισματοειδών σκιάσεων πνεύμονα, κ.ά.), για τη σταδιοποίηση του νεοπλάσματος [διερεύνηση πλευριτικής συλλογής, βιοψία λεμφαδένων μεσοθωρακίου στο αορτοπνευμονικό παράθυρο (Νο 5), στην παρα-αορτική θέση (Νο 6), στον κάτω πνευμονικό σύνδεσμο (Νο 9) και στους παρά το οισοφάγο (Νο 8)] και τέλος, για την παρηγορική θεραπεία του καρκίνου του πνεύμονα, με συχνότερη εφαρμογή τη διενέργεια πλευροδεσίας με talc σε κακοήθη πλευριτική συλλογή.
Η επιβίωση των ασθενών μετά από χειρουργική εξαίρεση του όγκου στο στάδιο Ι του ΜΜΚΠ κυμαίνεται από 90% στο στάδιο ΙΑ1 έως 73% στο στάδιο ΙΒ, ενώ είναι 85% και 80% για τα στάδια ΙΑ2 και ΙΑ3 αντίστοιχα. Η επιβίωση στη συνέχεια μειώνεται στο 65% για το στάδιο ΙΙΑ, στο 56% για το στάδιο ΙΙΒ. Στη συνέχεια η επιβίωση μειώνεται στο 41% για το στάδιο ΙΙΙΑ , ενώ στο στάδιο IV η 5ετής επιβίωση είναι σχεδόν μηδενική.4 Από τα παραπάνω φαίνεται η μεγάλη σημασία της έγκαιρης διάγνωσης, έτσι ώστε ο όγκος να αφαιρεθεί χειρουργικά όταν είναι στο στάδιο Ι, δηλαδή <3εκ., πριν δώσει λεμφαδενικές ή απομακρυσμένες μεταστάσεις. Ο μόνος τρόπος να μειωθεί η θνητότητα από τον καρκίνο του πνεύμονα είναι να μειωθεί το ποσοστό των καπνιστών στο γενικό πληθυσμό και να γίνει διάγνωση του καρκινώματος σε πρώιμο στάδιο με τα πρωτόκολλα εφαρμογής προσυμπτωματικού ελέγχου με CT θώρακα χαμηλής δόσης ακτινοβολίας στον πληθυσμό που έχει υψηλό κίνδυνο ανάπτυξης καρκινώματος του πνεύμονα.16
ΒΙΒΛΙΟΓΡΑΦΙΑ
- Barta JA, Powell CA, Wisnivesky JP. Global Epidemiology of Lung Cancer. Ann Glob Health 2019; 85: 8.
- Travis WD, Brambilla E, Nicholson AG, et al, on behalf of the WHO panel. The 2015 World Health Organization classification of lung tumors. Impact of genetic, clinical and radiologic Advances since the 2004 classification. J Thorac Oncol. 2015; 10: 1243–1260.
- Φορούλης ΧΝ, Παπακωνσταντίνου Χ. Πρωτοπαθής καρκίνος του πνεύμονα. Σε: Φορούλης ΧΝ (επιμελητής έκδοσης), Θωρακοχειρουργική, 2η έκδοση. Εκδόσεις University Studio Press, Θεσσαλονίκη 2020, σελ. 199-249.
- Detterbeck FC, Boffa DJ, Kim AW, Tanoue LT. The eighth edition lung cancer stage classification. Chest 2017; 151: 193-203.
- Leyn P, Dooms C, Kuzdzal J, et al. Revised ESTS guidelines for preoperative mediastinal lymph node staging for non-small-cell lung cancer. Eur J Cardiothorac Surg 2014; 45(5): 787-798.
- Brunelli A, Charloux A, Bolliger CT, Rocco G, Sculier J-P, Varela G, Licker M, Ferguson MK, Faivre-Finn C, Huber RM, Clini EM, Win T, De Ruysscher D, Goldman L, European Respiratory Society and European Society of Thoracic Surgeons joint task force on fitness for radical therapy. ERS/ESTS clinical guidelines on fitness for radical therapy in lung cancer patients (surgery and chemo-radiotherapy). Eur Respir J 2009; 34: 17-41.
- Falcoz PE, Conti M, Brouchet L, Chocron S, Puyraveau M, Mercier M, Etievent JP, Dahan M. The Thoracic Surgery Scoring System (Thoracoscore): risk model for in-hospital death in 15,183 patients requiring thoracic surgery. J Thorac Cardiovasc Surg 2007; 133: 325-332.
- Foroulis CN. Extended surgery for Non-Small Cell Lung Cancer (NSCLC). Surg Chron 2017; 22: 125-128.
- Postmus PE, Kerr KM, Oudkerk M, Senan S, Waller DA, Vansteenkiste J, Escriu C, Peters S, on behalf of the ESMO Guidelines Committee. Early and locally advanced non-small-cell lung cancer (NSCLC): ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol 2017; 28 (Supplement 4): iv1–iv21.
- Allaeys T, Berzenji L, Van Schil PE. Surgery after Induction Targeted Therapy and Immunotherapy for Lung Cancer. Cancers (Basel) 2021; 13: 2603.
- Antonia SJ, Villegas A, Davey Daniel D, et al. for the PACIFIC Investigators Overall survival with durvalumab after chemoradiotherapy in stage III NSCLC. N Engl J Med 2018; 379:2342-2350.
- Foroulis CN, Zarogoulidis P, Darwiche K, et al. Superior sulcus (Pancoast) tumors: current evidence on diagnosis and radical treatment. J Thorac Dis 2013; 5 (Suppl 4): S342-S358.
- Wu YL, Tsuboi M, He J, John T, Grohe C, Majem M, Goldman JW, Laktionov K, Kim SW, Kato T, Vu HV, Lu S, Lee KY, Akewanlop C, Yu CJ, de Marinis F, Bonanno L, Domine M, Shepherd FA, Zeng L, Hodge R, Atasoy A, Rukazenkov Y, Herbst RS; ADAURA Investigators. Osimertinib in Resected EGFR-Mutated Non-Small-Cell Lung Cancer. N Engl J Med 2020; 383: 1711-1723.
- Hu J, Chen Y, Dai J, Zhu X, Gonzalez-Rivas D, Jiang G, Li H, Zhang P. Perioperative outcomes of robot-assisted vs video-assisted and traditional open thoracic surgery for lung cancer: A systematic review and network meta-analysis. Int J Med Robot 2020; 16: 1-14.
- Montagne F, Bottet B, Sarsam M, Mbadinga F, Chaari Z, Rinieri P, Melki J, Peillon C, Baste J-M. Robotic versus open and video-assisted thoracoscopic surgery approaches for lobectomy. Mini-invasive Surg 2020; 4: 17.
- Leleu O, Basille D, Auquier M, Clarot C, et al. Lung cancer screening by low-dose CT scan: Baseline results of a French prospective study. Clin Lung Cancer 2020; 21: 145-152.










Άφησε σχόλιο