Περίληψη
Η ουρική αρθρίτιδα είναι συχνή φλεγμονώδης αρθρίτιδα ως αποτέλεσμα της υπερβολικής παραγωγής ουρικού οξέος, η οποία συνήθως εκδηλώνεται ως οξέα επεισόδια και φλεγμονή δευτεροπαθώς λόγω εναποθέσεως των μονονατριακών ουρικών κρυστάλλων ή τόφων στις αρθρώσεις, τένοντες και πέριξ ιστούς. Η υπερουριχαιμία προκαλείται από την αυξημένη παραγωγή ή ελαττωμένη απέκκριση του ουρικού οξέος ή αμφότερα. Τα μη στεροειδή αντιφλεγμονώδη φάρμακα, κολχικίνη και κορτικοστεροειδή χρησιμοποιούνται για τη θεραπεία της οξείας κρίσης της ουρικής αρθρίτιδας, έχουν δε περίπου παρόμοια επίδραση. Για την αντιμετώπιση της υπερουριχαιμίας χρησιμοποιούνται οι αναστολείς της οξειδάσης της ξανθίνης (αλλοπουρινόλη, φεβουξοστάτη), προβενεσίδη και πεγλοτικάση. Οι ιατροί έχουν αναπόσπαστο ρόλο στην εκπαίδευση του ασθενούς και στη βελτίωση της φροντίδας των ασθενών με ουρική αρθρίτιδα.
Gout: Therapeutic Options
Kataxaki E.
Rheumatologist, Director, General Hospital of Elefsina “Thriasio”
Abstract
Gout is a common inflammatory arthritis as a result of excessive uric acid production, which usually manifests itself as acute episodes and inflammation secondary to the deposition of unilateral urinary crystals or mucilages in the joints, tendons and around the tissues. Hyperuricaemia is caused by increased production or decreased uric acid excretion or both. Non-steroidal anti-inflammatory drugs, colchicine and corticosteroids are used to treat the acute gout and have a similar effect. Xanthine oxidase inhibitors (allopurinol, febuxostat, probenecid, and pegylated) are used to treat hyperuricaemia. Doctors have an integral role in patient education and care for patients with gout.
Εισαγωγή
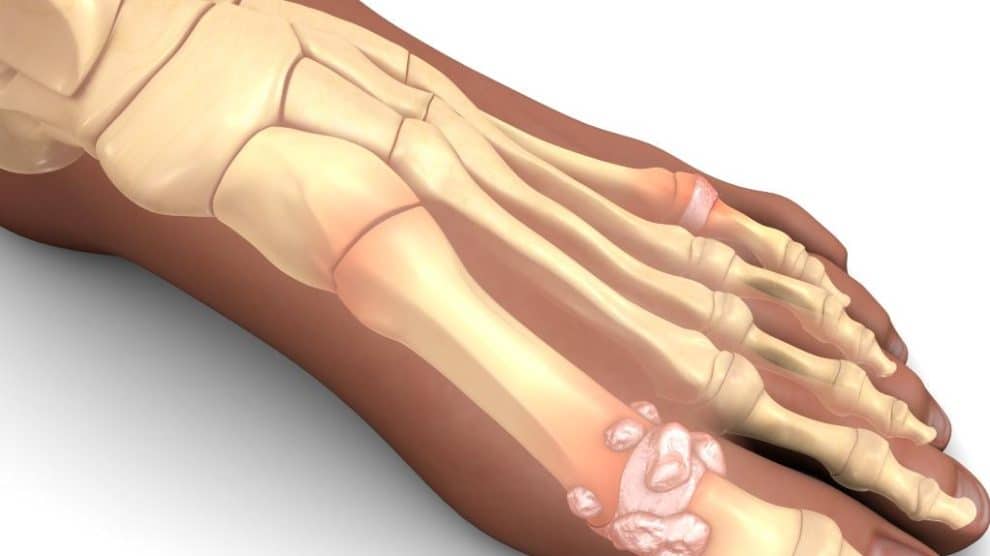
Η ουρική αρθρίτις είναι μια από τις πλέον συνήθεις μορφές της φλεγμονώδους αρθρίτιδας, προκαλείται δε από την εκσεσημασμένη εναπόθεση μονονατριακών ουρικών κρυστάλλων (MSU) στο αρθρικό υγρό, χόνδρο, οστά, τένοντες, θυλάκους και άλλες περιοχές1,2. Αυτή η συσσώρευση είναι το αποτέλεσμα της παρατεταμένης υπερουριχαιμίας1. Οι MSU κρύσταλλοι είναι η στερεά μορφή του ουρικού οξέος, το τελικό προϊόν μεταβολισμού της πουρίνης1,2.
Οι υποξανθίνη και ξανθίνη είναι ενδιάμεσα παράγωγα αυτού του καταβολισμού. Η ξανθίνη οξειδορεδουκτάση καταλύει τις τελικές δύο αντιδράσεις στη βιοχημική άλυσο οι οποίες προκαλούν το σχηματισμό του ουρικού οξέος: μετατροπή της υποξανθίνης σε ξανθίνη και ξανθίνης σε ουρικό οξύ. Το ουρικό οξύ διηθείται ελευθέρως στο νεφρικό σπείραμα, αλλά πλέον του 90% του διηθημένου ουρικού οξέος επαναπορροφάται. Οι κύριοι συμμεταφορείς υπεύθυνοι για τη σωληναριακή επαναπορρόφηση είναι οι URAT1 και GLUT93.
Η υπερουριχαιμία ορίζεται ως η υψηλή συγκέντρωση του ουρικού οξέος του ορού ή ίση προς 6,8mg/dL και είναι η βιοχημική ανωμαλία υποκείμενη στην ανάπτυξη ουρικής αρθρίτιδας. Η υπερουριχαιμία συνήθως οφείλεται στην υπερπαραγωγή ή ελαττωμένη απέκκριση του ουρικού οξέος, η τελευταία δε αποτελεί την αιτία της υπερουριχαιμίας στο 90% των ασθενών με ουρική αρθρίτιδα4. Πάντως, όλοι οι ασθενείς με υπερουριχαιμία δεν αναπτύσσουν ουρική αρθρίτιδα. Στις Η.Π.Α., 21% έχει υπερουριχαιμία και μόνο 4% έχει ουρική αρθρίτιδα5.
Επιδημιολογία
Παρά την ευρεία διακύμανση των δεδομένων μεταξύ των διαφόρων κρατών, πιστεύεται ότι η επίπτωση της ουρικής αρθρίτιδας έχει αυξηθεί κατά την τελευταία δεκαετία6. Στις Η.Π.Α. η Study National Health Interview βρήκε αύξηση της επίπτωσης της αυτο-αναφερθείσας ουρικής αρθρίτιδας από 4,8/1000 το 1967 σε 9,4/1000 το 19967.
Οι λόγοι της φανερής αύξησης στη συχνότητα της ουρικής αρθρίτιδας τα τελευταία χρόνια δεν έχουν πλήρως διευκρινιστεί, αν και έχουν περιγραφεί διάφοροι παράγοντες κινδύνου, όπως το μεταβολικό σύνδρομο, αλλαγές στη δίαιτα, παχυσαρκία, μακρότερος χρόνος ζωής, οινόπνευμα και αρτηριακή πίεση7. Αντιστρόφως, τα γαλακτούχα προϊόντα, καφές και βιταμίνη C έχουν βρεθεί ότι έχουν προστατευτική επίδραση για την ανάπτυξη της ουρικής αρθρίτιδας8.
Στις γυναίκες, τα οιστρογόνα προστατεύουν από την ουρική αρθρίτιδα επειδή αυτά συνοδεύονται με αυξημένη απέκκριση του ουρικού οξέος και η ορμονική θεραπεία αποκατάστασης έχει παρόμοια επίδραση9. Η ουρική αρθρίτις παρατηρείται μόνον σε 0,2/1000 περιπτώσεις νεαρών γυναικών μικρότερες των 45 ετών, ενώ γυναίκες με ουρική αρθρίτιδα τείνουν να είναι μεγαλύτερες και έχουν επιπλέον συνοσηρότητες, όπως η παχυσαρκία και νεφρική νόσος, συγκριτικά με τους άνδρες10.
Ποσοστό περίπου 25% των ασθενών με ουρική αρθρίτιδα έχουν οικογενειακό ιστορικό και ειδικότερα σε ασθενείς με πρώιμη εμφάνιση της νόσου (ηλικία <25 ετών), το 80% έχει οικογενές ιστορικό ουρικής αρθρίτιδας11.
Διάγνωση
Για τη διάγνωση της ουρικής αρθρίτιδας έχουν δημοσιευτεί αριθμός κριτηρίων12,13. Ο χρυσός κανόνας για τη διάγνωση της ουρικής αρθρίτιδας είναι η διαπίστωση των MSU στο αρθρικό υγρό ή τόφους. Άπαξ οριστικοποιηθεί η διάγνωση σε περίπτωση επαναλήψεως δεν χρειάζεται νέα εξέταση του αρθρικού για MSU. Το φυσιολογικό ή χαμηλό ουρικό οξύ δεν αποκλείει τη διάγνωση της οξείας ουρικής αρθρίτιδας, επειδή η συγκέντρωση μπορεί να μην αυξηθεί κατά τη διάρκεια της οξείας φάσεως14.
Η οξεία ουρική αρθρίτιδα είναι η συχνότερη αρχική κλινική εκδήλωση της ουρικής αρθρίτιδας. Συνήθως, στην αρχή προσβάλλεται μια μόνο άρθρωση, αλλά παρατηρείται και πολυαρθρική οξεία ουρική αρθρίτιδα σε άρρενες υπερτασικούς ασθενείς και μετεμμηνοπαυσιακές γυναίκες. Συχνά προσβάλλεται η μεταταρσιοφαλαγγικη άρθρωση του μεγάλου δακτύλου, όπως και οι αρθρώσεις του ταρσού, οι ποδοκνημικές και τα γόνατα. Στους ηλικιωμένους μπορεί να αναπτυχθεί φλεγμονή στις αρθρώσεις των δακτύλων. Μερικές φορές η φλεγμονή των όζων Heberden ή Bouchard αποτελεί την πρώτη εκδήλωση της ουρικής αρθρίτιδας. Το πρώτο επεισόδιο της οξείας ουρικής αρθρίτιδα συχνά αρχίζει τη νύχτα με σφοδρό αρθρικό άλγος και οίδημα. Οι αρθρώσεις καθίστανται ταχέως θερμές, ερυθρές και ευαίσθητες και η κλινική εικόνα συχνά υποδύεται την κυτταρίτιδα. Οι πρώτες προσβολές έχουν την τάση να υποχωρούν αυτομάτως εντός 3-10 ημερών και οι περισσότεροι ασθενείς δεν έχουν κατάλοιπα συμπτώματα έως το επόμενο επεισόδιο. Πολλοί παράγοντες μπορεί να προκαλέσουν οξεία ουρική αρθρίτιδα: διατροφικές παρεκτροπές, τραυματισμός, χειρουργική επέμβαση, υπερβολική κατανάλωση οινοπνευματωδών ποτών, φάρμακα (διουρητικά, λασαρτάνη, ατορβαστατίνη, φαινοφιμπράτη, αποκλειστές διαύλων ασβεστίου, χαμηλή δόση ασπιρίνης κα.). Διάφορες παρεμβάσεις και εργαστηριακές εξετάσεις, όπως η αναρρόφηση αρθρικού υγρού, ακτινογραφικός έλεγχος, ουρικό οξύ αίματος και νεφρική απέκκριση ουρικού οξέος μπορεί να εξεταστούν εάν υποψιαζόμεθα την ουρική αρθρίτιδα.
Θεραπεία
Βασικά η θεραπεία της ουρικής αρθρίτιδας μπορεί να διαιρεθεί σε δύο στάδια: αντιμετώπιση της οξείας κρίσης και μακράς διάρκειας θεραπεία (Πίνακας 1). Στο πρώτο στάδιο είναι κριτικής σημασίας η ανακούφιση του άλγους, ελάττωση της φλεγμονής και αρθρικής βλάβης. Για αυτό το σκοπό ο ασθενής πρέπει να θεραπεύεται με αντιφλεγμονώδεις παράγοντες. Στο δεύτερο στάδιο, η βοήθεια είναι η ελάττωση των συγκεντρώσεων του ουρικού οξέος του ορού και η πρόληψη νέων κρίσεων. Σε αυτό το στάδιο δεν χρησιμοποιούνται για μακρό διάστημα οι αντιφλεγμονώδεις παράγοντες, αλλά θα πρέπει να εφαρμόζονται αμφότερα φαρμακολογικά και μη φαρμακολογικά μέτρα16.
Όσον αφορά το συνταγογραφούμενο φάρμακο, αμφότερα για την οξεία αντιμετώπιση και μακράς διαρκείας θεραπεία, ορισμένες μεταβλητές μπορεί να επηρεάσουν την εκλογή του φαρμάκου, όπως η διαθεσιμότητα, κόστος, αποτελεσματικότητα και κλινικές ενδείξεις οφειλόμενες σε πιθανές συνοσηρότητες του ασθενούς. Προ της εφαρμογής της καταλλήλου θεραπείας θα πρέπει να λαμβάνονται υπόψιν οι συχνά παρατηρούμενες καταστάσεις συνδυαζόμενες με την ουρική αρθρίτιδα, όπως η υπέρταση, καρδιαγγειακή νόσος, χρονία νεφρική νόσος και σακχαρώδης διαβήτης16,17-21.
Πίνακας 1. Αντιμετώπιση της Οξεία και Χρόνιας Ουρικής Αρθρίτιδας
| Οξεία Κρίση | Θεραπεία Μακράς Διαρκείας (Χρόνια) |
| Σκοπός – Ανακούφιση από το άλγος – Ελάττωση της φλεγμονής – Αποκατάσταση της δυναμικής της άρθρωσης Αντιμετώπιση – Μη στεροειδή αντιφλεγμονώδη φάρμακα – Κορτικοστεροειδή – Κολχικίνη Εξετάζεται η πολυαρθρική προσβολή | – Πρόληψη των νέων κρίσεων – Ελάττωση της συγκέντρωσης των κρυστάλλων του ουρικού οξέος – Αναστολείς οξυδάσης της ξανθίνης – Ουρικοδιουρητικά – Ανασυνδυασμός ουρικάσης Συνιστάται η τροποποίηση των παραγόντων κινδύνου |
Αντιμετώπιση της Οξείας Κρίσης
Για την αντιμετώπιση των κρίσεων μέτριας ή χαμηλής έντασης που αφορούν την προσβολή μίας εκ των τριών μικρών αρθρώσεων ή μίας έως δύο μεγάλων αρθρώσεων, συνιστάται η μονοθεραπεία. Αυτή συνίσταται στη χορήγηση μη στεροειδών αντιφλεγμονωδών φαρμάκων (NSAIDs), κολχικίνης ή κορτικοστεροειδών16-21. Για τη μέγιστη αποτελεσματικότητα, η θεραπεία θα πρέπει να αρχίσει πρωίμως, προτιμότερα εντός 24 ωρών από της εμφανίσεως της οξείας κρίσης.
Τα μη στεροειδή αντιφλεγμονώδη φάρμακα (NSAIDs) είναι η πλέον ευρέος χρησιμοποιούμενη θεραπεία για την πρώιμη θεραπεία της οξείας ουρικής αρθρίτιδας και λόγω της έντασης της κρίσης αυτά τα φάρμακα μπορεί να χορηγηθούν στις μέγιστες δόσεις14. Δεν υπάρχει ιδιαιτερότητα μεταξύ των NSAIDs, επειδή αυτά έχουν παρόμοια επίδραση στην ελάττωση της οξείας δραστηριότητας της ουρικής αρθρίτιδας22. Για τη θεραπεία των οξέων κρίσεων της ουρικής αρθρίτιδας έχουν εγκριθεί η ναπροξένη, δικλοφενάκη, ινδομεθακίνη και σουλινδάκη. Σε ανθεκτικές ή σοβαρές περιπτώσεις φάρμακο από διαφορετική κατηγορία θα πρέπει να προστεθεί στη θεραπεία. Ο συνδυασμός θεραπείας με 2 διαφορετικές κατηγορίες παραγόντων θα πρέπει να εφαρμόζεται στην περίπτωση σοβαράς κρίσεως ή για πολυαρθρική νόσο (≥ 4 αρθρώσεις)14-22. Ο συνδυασμός NSAIDs και κορτικοστεροειδούς θα πρέπει να αποφεύγεται καθόσον συνεπάγεται επιπρόσθετες ανεπιθύμητες επιδράσεις. Πάντως, ενδοαρθρικά κορτικοστεροειδή μπορεί να χρησιμοποιηθούν σε συνδυασμό με οποιαδήποτε κατηγορία φαρμάκων. Τυπικώς, τα NSAIDs χορηγούνται σε πλήρη δόση για τις 3 πρώτες ημέρες της οξείας κρίσεως και ακολούθως στη χαμηλότερη δόση για 4 έως 7 ημέρες με βάση την κλινική απάντηση. Σε μια πρόσφατη τυχαιοποιημένη, ελεγχόμενη μελέτη που συγκρίθηκε η πρεδνιζόνη με την ινδομεθακίνη στο επείγον τμήμα αναφέρθηκε παρόμοια κλινική αποτελεσματικότητα για τη θεραπεία της οξείας ουρικής αρθρίτιδας, γεγονός που υποδεικνύει ότι η πρεδνιζόνη είναι παράγοντας πρώτης εκλογής όταν αντενδείκνυνται τα NSAIDs23. Τα NSAIDs θα πρέπει να αποφεύγονται σε ασθενείς με στεφανιαία νόσο, καρδιαγγειακή νόσο, γαστροοισοφαγική παλινδρόμηση ή πεπτικό έλκος και σε ασθενείς λαμβάνοντες αντιπηκτικά από του στόματος. Σε αυτές τις περιπτώσεις μπορεί να καταστεί αναγκαία η προφυλακτική χορήγηση αναστολέων αντλίας πρωτονίων (PPIs). Πάντως, λόγω της νεφρικής και καρδιαγγειακής τοξικότητας, η χρήση αυτών των φαρμάκων θα πρέπει να εξετάζεται προσεκτικά και να εξατομικεύεται. Τα NSAIDs είναι αποτελεσματικά στο 90% περίπου των ασθενών και η αποδρομή των συμπτωμάτων λαμβάνει χώρα εντός 5-7 ημερών14-23.
Η κολχικίνη ασκεί τις επιδράσεις της δια της ελαττώσεως της παραγωγής του γαλακτικού οξέος, η οποία στη συνέχεια ελαττώνει την εναπόθεση του ουρικού οξέος και επίσης ελαττώνει τη φαγοκυττάρωση με ελάττωση της φλεγμονώδους απάντησης. Αν και η κολχικίνη είναι παλαιό φάρμακο, μόλις προσφάτως (2012) επανεισήχθη από το FDA η ένδειξη για χρήση σε ασθενείς με οξεία ουρική αρθρίτιδα24. Η κολχικίνη θα πρέπει να χορηγείται μόνο στην πρώιμη ή καλώς κατοχυρωμένη κρίση ουρικής αρθρίτιδας. Η κολχικίνη χορηγείται σε δόση 1,2mg ακολουθούμενη από άλλη δόση 0,6mg σε 1 ώρα. Μετά 12 ώρες, 0,6mg μπορεί να χορηγηθούν άπαξ ή δύο φορές ημερησίως μέχρι υποχωρήσεως της νόσου25. Αυτό το θεραπευτικό σχήμα είναι πλέον αποτελεσματικό εάν χρησιμοποιηθεί εντός 36 ωρών από της εμφανίσεως της οξείας κρίσης25, αλλά δεν είναι αποτελεσματικό εάν η κρίση υπάρχει για 72 ώρες ή περισσότερο.
Τα κορτικοστεροειδή και η πρότυπος αυτών μορφή η πρεδνιζόνη χρησιμοποιούνται ως μονοθεραπεία για την οξεία κρίση της ουρικής αρθρίτιδας, αλλά αυτοί οι παράγοντες γενικώς επιφυλάσσονται για τους ασθενείς που δεν ανέχονταν την κολχικίνη ή τα NSAIDs λόγω των υπ’ αυτών προκαλούμενων συστηματικών ανεπιθύμητων επιδράσεων25. Η πρεδνιζόνη μπορεί να χορηγηθεί με διάφορους τρόπους. Ένας τρόπος είναι η χορήγηση 30 έως 35mg ημερησίως για 5 ημέρες28. Για σοβαρές περιπτώσεις μπορεί να χορηγηθεί δόση 0,5mg/Kg για 5 έως 10 ημέρες και στη συνέχεια διακόπτεται χωρίς πρόβλημα25. Η υψηλότερη δόση μπορεί επίσης να χρησιμοποιηθεί για άτομα με υψηλό δείκτη μάζας σώματος. Άλλο σχήμα περιλαμβάνει τη χορήγηση δόσεως 30 έως 60mg κάθε 2 ημέρες για συνολικά 10 έως 14 ημέρες.
Ωα αποτέλεσμα, έχουν αναπτυχθεί νέες θεραπείες για την καλύτερη αντιμετώπιση της οξείας ουρικής αρθρίτιδας. Μεταξύ αυτών, το μεγαλύτερο ενδιαφέρον εστιάζεται στις βιολογικές θεραπείες που στοχεύουν στην καταπολέμηση της φλεγμονώδους αντίδρασης IL-1 βήτα, που θεωρείται το κλειδί-μεσολαβητής στην παθογένεση της ουρικής αρθρίτιδας και πυροδότησης των MSU κρυστάλλων. Συγκεκριμένα, σε μια ανοικτή μελέτη βρέθηκαν ότι η Analcrina, ένας ανταγωνιστής του IL-1 υποδοχέα, είχε ως αποτέλεσμα την ταχεία και πλήρη ανακούφιση του άλγους χωρίς την πρόκληση οιονδήποτε ανεπιθύμητων ενεργειών σε ασθενείς που απέτυχαν με τις συμβατικές θεραπείες, όπως τα NSAIDs, κολχικίνη ή κορτικοστεροειδή. Η ριλονασέπτη (ένας διαλυτός IL-υποδοχές που συνδέεται με την IL-1 για την πρόληψη της συνδέσεως με τον αρχέγονο υποδοχέα) και η κανακινουμάμπη (ένα μονοκλωνικό αντίσωμα εναντίον της IL-1 βήτα) επίσης έχουν ως αποτέλεσμα τη μεγαλύτερη αποτελεσματικότητα έναντι της αλλοπουρινόλης και των κορτικοστεροειδών.
Όλα αυτά τα φάρμακα μπορεί να αντιπροσωπεύουν έγκυρες εναλλακτικές θεραπείες για τους ασθενείς στους οποίους η καρδιαγγειακή, νεφρική και γαστρεντερική συνοσηρότητα μπορεί να παρακωλύει τη χρήση NSAIDs, κολχικίνης και κορτικοστεροειδών.
Μια άλλη πρόοδος στην αντιμετώπιση της οξείας ουρικής αρθρίτιδας ήταν σχετικά με τη χρήση των χαμηλότερων δόσεων της κολχικίνης. Πράγματι, έχει παρατηρηθεί ότι η χορήγηση χαμηλότερων δόσεων κολχικίνης ήταν αποτελεσματικές όπως οι υψηλές δόσεις στην ανακούφιση του άλγους εμφανίζοντας ελάττωση των ανεπιθύμητων ενεργειών.
Προφύλαξη της Οξείας Κρίσης της Ουρικής Αρθρίτιδας
Η φαρμακολογική αντιφλεγμονώδης προφύλαξη συνιστάται για όλες τις περιπτώσεις της ουρικής αρθρίτιδας όταν αρχίζει η θεραπεία ελάττωσης του ουρικού οξέος του ορού. Για την προφύλαξη της κρίσης της ουρικής αρθρίτιδας συνιστάται ως πρώτης σειράς επιλογή η χρήση κολχικίνης από του στόματος. Εναλλακτικά, χρησιμοποιούνται NSAIDs25. Η κολχικίνη μπορεί να είναι ο προτιμώμενος προφυλακτικός παράγοντας έναντι των NSAIDs για την ελαχιστοποίηση των ανεπιθύμητων επιδράσεων. Η κολχικίνη προλαμβάνει ή ελαττώνει τη συχνότητα των κρίσεων στο 80% έως 85% των ασθενών. Η χρησιμοποιούμενη δόση της κολχικίνης είναι 0,5mg άπαξ ή δύο φορές ημερησίως. Για τηναπροξένη, η δόση είναι 250mg δύο φορές ημερησίως με ταυτόχρονη γαστρεντερική προφύλαξη. Στην περίπτωση που δεν δύναται να χρησιμοποιηθούν η κολχικίνη και NSAIDs, μπορεί να χορηγηθεί η πρεδνιζόνη ή πρεδνιζολόνη σε χαμηλή (<10mg/Kg ημερησίως) με κατάλληλη παρακολούθηση για πιθανές ανεπιθύμητες επιδράσεις (γαστρεντερικό σύστημα, οστά). Εάν δεν μπορεί να χρησιμοποιηθούν η κολχικίνη, NSAIDs και κορτικοστεροειδή, χορηγούνται οι ανταγωνιστές της IL-1 (ριλονασέπτη, κανακινουμάμπη)25.
Η προφύλαξη θα πρέπει να συνεχίζεται επί μακρόν εφόσον υπάρχει πρόσφατη (εντός των προηγούμενων 3 μηνών) κρίση ουρικής αρθρίτιδας ή παρουσία τόφου. Εάν δεν υπάρχει πρόσφατη κρίση ουρικής αρθρίτιδας ή συμπτώματα αρθροθυλακίτιδας, η προφύλαξη μπορεί να συνεχίζεται για το ελάχιστον 6 μήνες ή εναλλακτικά, για 3 μήνες μετά τη συνεχή επίτευξη του επιπέδου-στόχου του ουρικού οξέος του ορού σε ασθενή που δεν έχει τόφο ή για 6 μήνες σε ασθενείς που είχαν υποχωρήσαντα τόφο και ο στόχος του επιπέδου του ουρικού οξέος του ορού είναι επιτυχής και συνεχής25.
Θεραπεία της Υπερουριχαιμίας
Η ελάττωση του επιπέδου του ουρικού οξέος του ορού είναι σημαντική για την μακράς διαρκείας πρόληψη της αρθρικής βλάβης και της ανάπτυξης τόφων. Με βάση τις οδηγίες του American College of Rheumatology (ACR) 2012, η θεραπεία ελαττώσεως του ουρικού οξέος συνιστάται στην κατοχυρωμένη διάγνωση της ουρικής αρθρίτιδας με δύο ή περισσότερες οξείες κρίσεις ουρικής αρθρίτιδας, παρουσία τόφου, χρόνιας νεφρικής νόσου Σταδίου 2 ή περισσότερο ή παρουσία λίθων του νεφρού28. Αυτές είναι σε συμφωνία με συστάσεις από «άλλες οδηγίες». Ο σκοπός είναι η ελάττωση του ουρικού οξέος μικρότερη των 6mg/dl με βάση τις οδηγίες του ACR και European League Against Rheumatism (EULAR), σε σύγκριση προς τον χαμηλότερο στόχο των 5mg/dl που συνιστάται από την British Society of Rheumatology (BSR)14,28,29. Ο σκοπός της χαμηλής τιμής των 5mg/dl που υποστηρίζεται από το ACR και EULAR σε σοβαρές περιπτώσεις ουρικής αρθρίτιδας προσδιορίζει ασθενείς με τόφο, χρόνια αρθροπάθεια ή συχνές κρίσεις.
Όλες οι οδηγίες εξακολουθούν να συνιστούν ως πρώτη σειρά θεραπείας τους αναστολείς της οξειδάσης της ξανθίνης (αλλοπουρινόλη, φεβουξοστάτη [XOIs]). Τα ουρικοζουρικά φάρμακα είναι θεραπεία δεύτερης σειράς ή εναλλακτικοί παράγοντες και όλες οι πρόσφατες οδηγίες επίσης υποστηρίζουν το συνδυασμό των παραγόντων (π.χ. XOIs και ουρικοζουρικό) όταν η μονοθεραπεία είναι αναποτελεσματική14,28. Όσον αφορά τα οφέλη της αντιμετώπισης της ασυμπτωματικής υπερουριχαιμίας δεν είναι εισέτι σαφή, αλλά οι Ιαπωνικές οδηγίες συνιστούν τη θεραπεία σε ασθενείς με μη ουρική αρθρίτιδα με ουρικό οξύ του ορού μεγαλύτερο των 8mg/dl επειδή υπάρχει αυξημένος κίνδυνος ανάπτυξης ουρικής αρθρίτιδας ή ανάπτυξης άλλων παθήσεων, όπως η καρδιαγγειακή νόσος30.
- Αναστολείς Οξειδάσης της Ξανθίνης (XOIs)
Οι αναστολείς οξειδάσης της ξανθίνης (XOIs) περιλαμβάνουν την αλλοπουρινόλη και φεβουξοστάτη και είναι ο στυλοβάτης της θεραπείας ελαττώσεως του ουρικού οξέος. Όταν χρησιμοποιούνται οι XOIs, είναι απαραίτητη η περιοδική παρακολούθηση της γενικής αίματος και νεφρικής και ηπατικής λειτουργίας. Το ουρικό οξύ θα πρέπει να παρακολουθείται κάθε 4 εβδομάδες μέχρις ότου επιτευχθεί ο στόχος του επιπέδου του ουρικού οξέος και ακολούθως κάθε 6 μήνες. Οι XOIs αντενδείκνυνται σε ασθενείς που λαμβάνουν αζαθειοπρίνη ή μεταβολίτες των. Δεν συνιστάται η ταυτόχρονη χρήση αλλοπουρινόλης και φεβουξοστάτης καθόσον δεν φαίνεται ότι υπάρχει επιπρόσθετο όφελος επειδή αμφότεροι οι παράγοντες διαγωνίζονται για τον αυτό υποδοχέα19. Οι ασθενείς θα πρέπει να ενημερώνονται όσον αφορά την πιθανότητα των αυξημένων κρίσεων με την έναρξη της θεραπείας ελαττώσεως του ουρικού οξέος.
Η αλλοπουρινόλη παραμένει η αρχική θεραπεία για την ελάττωση του ουρικού οξέος λόγω της αποτελεσματικότητας, διαθεσιμότητας και χαμηλού κόστους. Η έναρξη θεραπείας με αλλοπουρινόλη θα πρέπει να γίνεται συνήθως με τη χορήγηση χαμηλής δόσης και η αύξηση να είναι βραδεία. Η αρχική δόση για άτομα με φυσιολογική νεφρική λειτουργία είναι 100mg ημερησίως με βραδεία τιτλοποίηση της δόσης κάθε 4 εβδομάδες οπότε αυξάνεται κατά 100mg εξαρτώμενη από την επίτευξη του στόχου του ουρικού οξέος18,28. Δόσεις που φτάνουν τα 800mg ημερησίως είναι εγκεκριμένες στις Η.Π.Α. σε σύγκριση με τα 900mg ημερησίως στην Ευρώπη29. Ένα συχνό σφάλμα στην αντιμετώπιση της ουρικής αρθρίτιδας είναι η διακοπή στην αύξηση της δόσης των 300mg ακόμη και εάν δεν έχει ο στόχος του επιπέδου του ουρικού οξέος. Η ανεπαρκής τιτλοποίηση της δόσης επηρεάζεται σε σημαντικό βαθμό από την έλλειψη γνώσεων από τους ιατρούς επειδή πιστεύουν ότι υπάρχει αυξημένος κίνδυνος πιθανών ανεπιθύμητων ενεργειών. Γενικότερα, η αλλοπουρινόλη είναι ασφαλές φάρμακο, αλλά ποσοστό ασθενών περίπου 2% αναπτύσσουν αντιδράσεις υπερευαισθησίας οι οποίες μπορεί ενίοτε να είναι σοβαρές και θανατηφόρες με θνησιμότητα περίπου 20%. Πάντως, η αλλοπουρινόλη μπορεί να έχει αμφότερες δράσεις σχετιζόμενες με τη δόση (π.χ. μη γαστρεντερική και εξανθήματα) και ανεπιθύμητες ιδιοσυγκρασιακές επιδράσεις. Αυτές κυρίως παρατηρούνται μεταξύ ασθενών με νεφρική δυσλειτουργία, όπου η δόση πρέπει να προσαρμόζεται καταλλήλως.
Η φεβουξοστάτη είναι ένας μη πουρινικός – ειδικός ΧΟI που πρωτοπαθώς μεταβολίζεται στο ήπαρ. Η συνιστώμενη δόση της φεβουξοστάτης είναι 40-80mg ημερησίως στις Η.Π.Α. και μεγαλύτερες μέχρι 120mg ημερησίως στην Ευρώπη. Η δόση της φεβουξοστάτης μπορεί να αυξάνεται κάθε 2 εβδομάδες εάν τα επίπεδα του ουρικού οξέος δεν ελαττώνονται. Σε δύο τυχαιοποιημένες, ελεγχόμενες μελέτες όλες οι δόσεις της φεβουξοστάτης ήταν περισσότερο αποτελεσματικές έναντι της αλλοπουρινόλης σε συνήθεις δόσεις όσον αφορά στην ελάττωση του ουρικού οξέος σε συγκεντρώσεις των <6mg/dl σε αμφότερους τους ασθενείς με φυσιολογική ηπατική λειτουργία και διαταραχή της νεφρικής λειτουργίας31,32. Οι ασθενείς συχνά παραπονέθηκαν για κρίση ουρικής αρθρίτιδας με υψηλή δόση φεβουξοστάτης31. Ο κύριος περιορισμός αμφοτέρων των μελετών ήταν ότι οι δόσεις της αλλοπουρινόλης δεν τιτλοποιήθηκαν υψηλότερα των 300mg που είναι συχνά απαραίτητο και περισσότερο αποτελεσματικό στην επίτευξη του στόχου συγκεντρώσεως του ουρικού οξέος33. Οι πλέον συχνά αναφερθείσες ανεπιθύμητες αντιδράσεις ήταν τρανσαμιναιμία, διάρροια, κεφαλαλγία, ναυτία και εξάνθημα. Η φεβουξοστάτη φαίνεται ότι είναι ολιγότερο τοξική έναντι της αλλοπουρινόλης και σε ασθενείς με μέτρια έως σοβαρή νεφρική νόσο και δεν είναι αναγκαία η προσαρμογή της δοσολογίας, καθόσον αυτή μεταβολίζεται κυρίως στο ήπαρ34. Πάντως, η φαρμακοκινητική και φαρμακοδυναμική της φεβουξοστάτης δεν διαταράσσεται σημαντικώς σε ασθενείς με μέτρια ηπατική διαταραχή26.
Ανεξάρτητα των επωφελών επιδράσεων της αλλοπουρινόλης και φεβουξοστάτης στην ουρική αρθρίτιδα, ο αριθμός των ασθενών στους οποίους επιτυγχάνεται επίπεδα ουρικού οξέος <6mg/dl είναι κατά μέσο όρο 20-40% για την αλλοπουρινόλη και 45-67% για τη φεβουξοστάτη (δεδομένα Φάσεως 3), δεικνύοντα ότι είναι αναγκαίες επιπλέον θεραπείες26.
- Ουρικοζουρικά Φάρμακα
Οι ουρικοζουρικοί παράγοντες ελαττώνουν τη συγκέντρωση του ουρικού οξέος του ορού μέσω αποκλεισμού της νεφρικής επαναπορροφήσεως του ουρικού οξέος. Η προβενεσίδη, βενζμπρομαρόνη και τελευταία η λεσινουράδη είναι οι κύριοι διαθέσιμοι παράγοντες αυτής της κατηγορίας των ουρικοζουρικών φαρμάκων.
Η προβενεσίδη δρα δι’ αναστολής των URA1 και GLUT9 συμμεταφορέων και είναι το πρωτότυπο ουρικοζουρικό φάρμακο στη θεραπεία της υπερουριχαιμίας. Πάντως, η προβενεσίδη υπο-χρησιμοποιείται συγκριτικά με τους XOIs και χρειάζεται τη χορήγηση δύο φορές ημερησίως με συνέπεια τη μη συμμόρφωση πολλών ασθενών. Η προβενεσίδη αντενδείκνυται σε ασθενείς με νεφρολιθίαση, επί παρουσίας υπερπαραγωγής ουρικού οξέος ή σε ασθενείς με κάθαρση κρεατινίνης μικρότερης των 30ml/λεπτό/1,73m2. Οι ασθενείς συμβουλεύονται να λαμβάνουν αυξημένη ποσότητα υγρών και επίτευξη αλκαλοποιήσεως των ούρων με διττανθρακικό νάτριο ή κιτρικό κάλιο. Η τυπική δόση της προβενεσίδης είναι 250mg δύο φορές ημερησίως, η οποία μπορεί να αυξηθεί στα 2000 έως 3000mg ημερησίως. Η προβενεσίδη μπορεί να χρησιμοποιηθεί σε συνδυασμό με XOIs ή άλλο εναλλακτικό παράγοντα πρώτης γραμμής17,19,28. Η προβενεσίδη έχει επίσης πολλαπλές φαρμακευτικές αλληλεπιδράσεις με συνήθως χρησιμοποιούμενα φάρμακα, όπως NSAIDs, αντιβιοτικά βήτα-λακτάμης και ηπαρίνη, τα οποία περιορίζουν τη χρήση της.
Η βενζμπρομαρόνη είναι δραστικός ουρικοζουρικός παράγοντας και είναι δραστικότερος της προβενεσίδης όταν χρησιμοποιηθεί προστιθέμενος στην αλλοπουρινόλη σε δόση 300mg ημερησίως με επιτυγχανόμενο στόχο ουρικού οξέος στα 5mg/dl στο 92% των ασθενών. Το φάρμακο αυτό εμφανίζει σημαντικές ανεπιθύμητες ενέργειες και έχει αποσυρθεί σε πολλές χώρες.
Η λεσινουράδη, ένας άλλος ουρικοζουρικός παράγοντας, χρησιμοποιείται σε σταθερό συνδυασμό με αλλοπουρινόλη ή φεβουξοστάτη για τη θεραπεία της υπερουριχαιμίας με ουρική αρθρίτιδα. Το φάρμακο χορηγείται σε άπαξ ημερήσια δόση συνδυασμού (200mg) το πρωί για την επίτευξη του επιθυμητού στόχου ουρικού οξέος σε ασθενείς που δεν επιτυγχάνεται μόνο με την αλλοπουρινόλη. Η λεσινουράδη δεν θα πρέπει να χρησιμοποιείται ως μονοθεραπεία επειδή είναι πιθανές οι ανεπιθύμητες ενέργειες επί των νεφρών36, γεγονός που επιβάλλει την προσεκτική παρακολούθηση της νεφρικής λειτουργίας, αλλά η λεσινουράδη μπορεί να χρησιμοποιείται σε ασθενείς με ιστορικό νεφρολιθίασης36. Οι πλέον συχνές ανεπιθύμητες επιδράσεις είναι κεφαλαλγία, γριππώδης λοίμωξη, αύξηση των επιπέδων κρεατινίνης του ορού και γαστροοισοφαγική παλινδρόμηση36.
- Ουρικάση (Πεγλοτικάση)
Η ουρικάση είναι ένζυμο που μετατρέπει το ουρικό οξύ σε πλέον διαλυτούς κρυστάλλους και συνιστάται για την ουρική αρθρίτιδα που είναι ανθεκτική στις συμβατικές θεραπείες της ουρικής αρθρίτιδας ή σε ασθενείς με σοβαρά νόσο (π.χ. παραμορφωτική τοφική ουρική αρθρίτιδα)28. Η ανεπάρκεια της γλυκοζο-6-φωσφορικής δεϋδρογονάσης αποτελεί αντένδειξη στη θεραπεία. Η πεγλοτικάση χορηγείται ενδοφλεβίως σε δόση 8mg κάθε 2 εβδομάδες. Κατά τη διάρκεια της θεραπείας με πεγλοτικάση είναι συχνές οι κρίσεις ουρικής αρθρίτιδας οφειλόμενες στη ταχεία ελάττωση των επιπέδων του ουρικού οξέος. Η μακράς διαρκείας θεραπεία και η διάρκεια της θεραπείας με πεγλοτικάση δεν είναι γνωστά. Επειδή η πεγλοτικάση είναι πρωτεΐνη, αλλεργικές αντιδράσεις όπως εξανθήματα, κνίδωση και βρογχόσπασμος είναι πιθανές επιπλοκές, ειδικότερα μετά επανειλημμένες εγχύσεις35.
Συμπέρασμα
Η ουρική αρθρίτιδα είναι παγκοσμίως διαδεδομένη νόσος με αύξουσα συχνότητα οφειλόμενη στον αυξημένο αριθμό ατόμων με καταστάσεις που προδιαθέτουν στην υπερουριχαιμία, όπως η υπέρταση, παχυσαρκία, σακχαρώδης διαβήτης, χρόνια νεφρική νόσος και η χρήση διουρητικών. Η επιτυχής αντιμετώπιση της ουρικής αρθρίτιδας χρειάζεται την κατανόηση της εξέλιξης της νόσου και τη χρονιότητα, όπως επίσης την εφαρμογή της θεραπείας από τους ιατρούς και τη συμμόρφωση των ασθενών. Η εφαρμογή της θεραπείας ελαττώσεως του ουρικού οξέος ελαττώνει τον κίνδυνο για περαιτέρω κρίσεις της ουρικής αρθρίτιδας, αλλά είναι απαραίτητη η προφύλαξη εναντίον των κρίσεων μέχρι σταθεροποιήσεως της δόσης συντήρησης.
ΒΙΒΛΙΟΓΡΑΦΙΑ
- Bardin T, Richette P. Definition of hyperuricemia and gouty conditions. Curr Opin Rheumatol 2014; 26: 186-191.
- Perez Ruiz F, Herrerro-Beites AM. Evaluation and treatment of gout as a chronic disease. Adv Ther 2012; 29: 935-946.
- Gustafsson D, Unwin R. The pathophysiology of hyperuricemia and its possible relationship of cardiovascular disease, morbidity and mortality. BMC Nephrol 2013; 14: 164.
- Choi HK, Mont HB, Reginato AM. American College of Physicians, American College Physiological Society. Pathogenesis of gout. Ann Intern Med 2005; 143: 499-516.
- Zhu Y, Pandya BJ, Choi HK. Prevalence of gout and hyperuricemia in the US general population: the National Health and Nutrition Examination Survey 2007-2008. Arthr Rheum 2011; 63: 3136-3141.
- Roddy E, Choi HK. Epidemiology of gout. Rheum Dis Clin North Am 2014; 40: 155-175.
- Lawrence RC, Felson DT, Helmick GG, et al. Estimates of prevalence of arthritis and other rheumatic conditions in the United States. Part II. Arthritis Rheum 2008; 58: 26-35.
- Choi HK. A prescription for lifestyles changes in patients with hyperuricemia and goyt. Curr Opin Rheumatol 2010; 22: 165-172.
- Sumino H, Ichikawa S, Kanda T, et al. Reduction of serum uric acid by hormone replacement therapy in post-menopausal women with hyperuricemia. Lancet 1999; 334: 650.
- Harrold LR, Etzel CJ, Gibifsky A, et al. Sex differences in gout characteristics: tailoring care for women and men. BMC Mucoskelet Dis 2017; 18: 108.
- Neogi T. Gout. Ann Intern Med 2016; ITC1-ITC16.
- Kienhorst LBE, Janssens HJEM, Fransen J, et al. The validation of a diagnostic rule for gout without joint, fluid analysis: a prospective study. Rheumatology (Oxford) 2015; 54: 609-614.
- Taylor MJ, Fransen J, Dalbeth N, et al. Performance of classification criteria for gout in early and established disease. Ann Rheum Dis 2016; 75: 178-182.
- Zhang W, Doherty M, Pascual E, et al. EULAR evidence-based recommendations for gout: Part II: Diagnosis. Report of Task Force of the EULAR Standing Committee for International Clinical studies Including Therapeutics (ESCISIT). Ann Rheum Dis 2006; 65: 1301-1311.
- Neogi T. Clinical practice. Gout. N Engl J Med 2011; 364: 443-452.
- Schlesinger N. Treatment of acute gout. Rheum Dis Clin North Am 2014; 40: 329-341.
- Sattui SE, Gaffo AL. Treatment of hyperuricemia in gout: current therapeutic options, latest developments and clinical implications. Ther Adv Muscuscel Dis 2016; 8: 145-159.
- Richette P, Doherty M, Pascual E, et al. 2016 updated EULAR evidence-evidence-based recommendations for the management of gout. Ann Rheum Dis 2017; 76: 29-42.
- Aslam F, Michet C Jr. My treatment of gout. Mayo Clin Proc 2017; 92: 1234-1247.
- Engel B, Just J, Blackwenn K. Treatment options for gout. Dtsch Arztebl Int 2017; 114: 215-222.
- Qaseem A, Harris RP, Forciea MA. Management of acute and reccurent gout: A clinical practice guideline from the American College of Physicians. Ann Intern Med 2017; 166: 58-68.
- Rees F, Hui M, Doherty M. Optimizing current treatment of gout. Nat Rev Rheumatol 2014; 10: 271-283.
- Rainer TH, Cheng CH, Janssens HJ, et al. Oral prednisone in the treatment of acute gout: a pragmatic, multicenter, double-blind, randomized trial. Ann Intern Med 2016; 164: 464-471.
- Colcrys (colchicine) package insert. Deerfield, IL: Takeda Pharmaceuticals America, Inc. June 2012.
- Khanna D, Khanna PP, Fitzgerald JD, et al. 2012 American College of Rheumatology Guidelines for management of gout, Part 2: therapy and anti-inflammatory prophylaxis of acute gouty arthritis. Arthritis Care Res (Hoboken) 2012; 64: 1447-1461.
- Suresh P. Recent advances in management of gout. WJ Med 2012; 105: 407-417.
- Terkeltaub RA, Furst DE, Bennett K, et al. High versus low dosing of oral colchicine for early acute gout flare: twenty-four hour outcome of the first multicenter, randomized, double-blind, placebo-controlled, parallel group, dose comparison colchicine study. Arthritis Rheum 2010; 62: 1060-1068.
- Khanna D, Fitzgerald J, Khanna P, et al. American College of Rheumatology Guidelines for management of gout. Part I: systematic non-pharmacologic and pharmacologic therapeutic approaches to hyperuricemia. Arthritis Care Res (Hoboken) 2012; 64: 1431-1446.
- Jordan K, Cameron J, Snaith M, et al. British Society for Rheumatology and British Health Professionals in Rheumatology Guidelines for the management of gout. Rheumatology (Oxford) 2007; 46: 1372-1374.
- Yamanaka H. Japanese Guidelines for the management of hyperuricemia and gout: Second Edition. Mucleosides Nucleic Acid 2011; 30: 1018-1029.
- Becker MA, Schumacher HR Jr, Wortmann RL, et al. Febuxostat compared with allopurinol in patients with hyperuricemia and gout. N Eng J Med 2005; 353: 2450-2461.
- Becker MA, Schumacher HR, Espinoza LR, et al. The urate-lowering efficacy and safety of febuxostat in the treatment of the hyperuricemia of gout: the CONFIRMS trial. Arthritis Ther Res 2010; 12: R63.
- Lee MH, Stocker SL, Anderson J, et al. Initiating allopurinol therapy: do we need to know the patients HLA status? Intern Med J 2011; 42: 411-416.
- Saag KG, Whelton A, Becker MA, et al. Impact of febuxostat on renal function in gouty patients with moderate-to-severe renal impairment. Arthritis Rheum 2016; 68: 2035-2043.
- Reinders M, VanRoo E, Houtman P, et al. Biochemical effectiveness of allopurinol and allopurinol-probenecid in previously benzbromarone-treated gout patients. Clin Rheumatol 2007; 26: 1459-1465.
- Hoy Sm. Lesinurad: first global approach. Drugs 2016; 76: 509-516.
- Becker MA, Baraf HS, Yood RA, et al. Long-term safety of pegloticase in chronic gout refractory to conventional treatment. Ann Rheum dis 2013; 72: 1469-1474.









Άφησε σχόλιο