John A. Cuenca1, Javier Balda1, Ana Palacio2,3, Larry Young3,4, Michael H. Pillinger5,6, Leonardo Tamariz2,3
1 Universidad Catolica de Santiago de Guayaquil, Ecuador
2 Division of Population Health and Computational Medicine, Miller School of Medicine,University of Miami, Miami, FL, USA
3 Veterans Affairs Medical Center, Miami, FL, USA
4 Division of Rheumatology, University of Miami, USA
5 Division of Rheumatology, New York University School of Medicine, USA
6 Veterans Affairs Medical Center, New York, NY, USA
Ιστορικό. Η φεβουξοστάτη έχει εγκριθεί στις Ηνωμένες Πολιτείες για τη αντιμετώπιση της υπερουριχαιμίας σε ασθενείς με ουρική αρθρίτιδα. Τον Νοέμβριο του 2017, το FDA δημοσίευσε μια προειδοποίηση σχετικά με μια πιθανή σχέση μεταξύ της φεβουξοστάτης και της καρδιαγγειακής νόσου (CVD) που αναφέρθηκε σε μία κλινική δοκιμή.
Σκοπός. Επιχειρείται διεξαγωγή μιας συστηματικής ανασκόπησης και μετα-ανάλυσης και η αξιολόγηση τουκινδύνου σοβαρών δυσμενών καρδιαγγειακών επεισοδίων (MACE) σε ασθενείς που λαμβάνουν φεβουξοστάτη σε σύγκριση με ομάδα ελέγχου.
Μέθοδοι. Διερευνήσαμε τη βάση δεδομένων MEDLINE και EMBASE για μελέτες που δημοσιεύθηκαν μέχρι τον Μάρτιο του 2018. Περιλήφθηκαν τυχαιοποιημένες κλινικές δοκιμές (RCTs) που συνέκριναν τη φεβουξοστάτη με ομάδες ελέγχου, συμπεριλαμβανομένων του εικονικού φαρμάκου και της αλλοπουρινόλης. Υπολογίσαμε τον συγκεντρωμένο σχετικό κίνδυνο (RR) της θνησιμότητας MACE και της καρδιαγγειακής νόσου με τα αντίστοιχα διαστήματα εμπιστοσύνης 95% (CI).
Αποτελέσματα. Η αναζήτηση ανέδειξε 374 πιθανές σχετικές μελέτες. Μεταξύ των 25 RCT που περιλαμβάνονται στη συστηματική ανασκόπηση, 10 ήταν ποιοτικώς κατάλληλες για τη μετα-ανάλυση. Μεταξύ των 14.402 ατόμων που συμπεριλήφθηκαν, η μέση ηλικία ήταν 54 έτη (IQR 52-67) και 90% ήταν άνδρες (IQR 82-96). 8602 έλαβαν φεβουξοστάτη, 5118 αλλοπουρινόλη και 643 εικονικό φάρμακο. Η δεξαμενήRR του MACE για τη φεβουξοστάτη ήταν 0,9. 95% CI 0.6-1.5 (ρ = 0.96) σε σύγκριση με τον έλεγχο. Το RR του θανάτου που σχετίζεται με το CV για τηφεβουξοστάτη ήταν 1,29. 95% CI 1,01-1,66 (ρ = 0,03).
Συμπεράσματα. Σε σύγκριση με άλλες θεραπείες που ελαττώνουν το ουρικό οξύ, η φεβουξοστάτη δεν αυξάνει ή μειώνει τον κίνδυνο καρδιαγγειακής νόσου, αλλά μπορεί να αυξήσει τον κίνδυνο θανάτου από CVD. Για την επαρκή αξιολόγηση του κινδύνου καρδιαγγειακής νόσου με τη χρήση της φεβουξοστάτης απαιτούνται περισσότερες RCT μελέτες που να μετρούν την καρδιαγγειακή ασφάλεια ως κύριο σκοπό
1. Εισαγωγή
Η ουρική αρθρίτιδα είναι ένας ανεξάρτητος προγνωστικός παράγοντας των καρδιαγγειακών παθήσεων1 και ηουρία αίματος (SU) σχετίζεται με τη συχνότητα της κολπικής μαρμαρυγής2,3, τη θνησιμότητα της καρδιακής ανεπάρκειας4, της ασβεστοποίησης της στεφανιαίας αρτηρίας5 και άλλων καρδιαγγειακών νοσημάτων. Ωστόσο, η βελτίωση των καρδιαγγειακών κλινικών αποτελεσμάτων με τη μείωση του SU είναι αμφιλεγόμενη6,7.
Η φεβουξοστάτη είναι ένας μη-πουρινικόςαναστολέας της οξειδάσης της ξανθίνης και χρησιμοποιείται στην αντιμετώπιση της υπερουριχαιμίας. Οι μελέτες δεν έχουν δείξει καμιά κατωτερότητα στη μείωση του SU σε σύγκριση με την αλλοπουρινόλη, τον πιο συχνά χρησιμοποιούμενο παράγοντα μείωσης της SU8. Ωστόσο, στις 15 Νοεμβρίου 2017, το FDA εξέδωσε μια προειδοποίηση σχετικά με τη φεβουξοστάτη9 με βάση τα προκαταρκτικά αποτελέσματα της δοκιμής CARES, η οποία διεξήχθη σε περισσότερους από 6000 ασθενείς για να εκτιμηθεί η καρδιαγγειακή ασφάλεια της φεβουξοστάτης σε σύγκριση με την αλλοπουρινόλη. Η πλήρης μελέτη δημοσιεύθηκε στη συνέχεια10 και δεν παρουσίασε διαφοροποίηση των συνολικών καρδιαγγειακών συμβαμάτων, αλλά αυξημένο κίνδυνο για όλες τις αιτίες και την καρδιαγγειακή θνησιμότητα στην ομάδα της φεβουξοστάτης.
Έχουν δημοσιευτεί δώδεκα συστηματικές ανασκοπήσεις ή μετα-αναλύσεις σχετικά με τη θεραπεία ελαττώσεως του ουρικού οξέος και την ουρική αρθρίτιδα ή υπερουριχαιμία. Έξι αξιολόγησαν την αποτελεσματικότητα των φαρμάκων χωρίς να αναφέρουν τα καρδιαγγειακά επεισόδια8,11-15, τρείς αξιολόγησαν τα νεφροπροστατευτικά τους αποτελέσματα16-18, μια αξιολόγησε την επίδραση της θεραπείας ελαττώσεως του ουρικού οξέος στην καρδιαγγειακή πρόληψη7 και μια την επίδραση της θεραπείας ελαττώσεως του ουρικού οξέος στην αρτηριακή πίεση19. Μόνο μία μετα-ανάλυση20 αξιολόγησε τα καρδιαγγειακά συμβάντα της φεβουξοστάτης και δεν βρήκε περιστασιακά περιστατικά. Ωστόσο, αυτή η μελέτη δεν περιλάμβανε την CARES, η οποία αναζητούσε μόνο σε μία βάση δεδομένων για τον εντοπισμό των καρδιαγγειακών συμβαμάτων ως ανεπιθύμητων ενεργειών και περιλεάμβανε μόνο τέσσερις μελέτες.
Για να αξιολογήσουμε τα διαθέσιμα στοιχεία σχετικά με την καρδιαγγειακή ασφάλεια τηςφεβουξοστάτης, πραγματοποιήσαμε μια συστηματική ανασκόπηση και μετα-ανάλυση μελετών που συγκρίνουν τα υπερουριχαιμικά άτομα με ή/και χωρίς ουρική αρθρίτιδα και τα οποία έλαβαν φεβουξοστάτη, άλλες θεραπείες ελαττώσεως του ουρικού οξέος ή εικονικό φάρμακο.
2. Υλικό και Μέθοδος
2.1. Πρωτόκολλο και Καταγραφή. Πραγματοποιήσαμε τη συστηματική ανασκόπηση σύμφωνα με τη μεθοδολογία Cochrane. Το πρωτόκολλο της παρούσας μελέτης δεν καταχωρήθηκε. Τα ημέτερα αποτελέσματα είναι σε συμφωνία με τα προτιμούμενα στοιχεία αναφοράς για τη δήλωση Συστηματικών Ανασκοπήσεων και Μετα-Αναλύσεων (PRISMA).
2.2. Στρατηγική Αναζήτησης. Πραγματοποιήσαμε μια αναζήτηση βιβλιογραφίας χρησιμοποιώντας τη βάση δεδομένων MEDLINE μέσω του PubMed από την αρχή έως το 2018. Αναλύσαμε όλα τα άρθρα, εκτός από αυτά που περιέχουν βασικούς όρους όπως η υπερουριχαιμία και η φεβουξοστάτη. Πραγματοποιήσαμε όλες τις αναζητήσεις τον Μάρτιο του 2018 και συμπληρώσαμε τα αρχικά αποτελέσματα με χειρωνακτικές αναζητήσεις βιβλιογραφιών βασικών σχετικών άρθρων. Επιπλέον, αναζητήσαμε στη βάση δεδομένων EMBASE χρησιμοποιώντας το ίδιο χρονικό πλαίσιο και τα ίδια κριτήρια, καθώς και μια αναζήτηση της βάσης δεδομένων κλινικών δοκιμών για μη δημοσιευμένες μελέτες ή δεδομένα σχετικά με τα καρδιαγγειακά συμβάντα που δεν αναφέρονται στην αρχική δημοσίευση. Αποκλείσαμε περιλήψεις συνεδρίων και άρθρα που δεν δημοσιεύθηκαν στα αγγλικά λόγω της αδυναμίας να λάβουμε όλες τις απαραίτητες πληροφορίες.
2.3. Κριτήρια Ενσωμάτωσης και Αποκλεισμού. Συμπεριλάβαμε τυχαιοποιημένες κλινικές μελέτες που συγκρίνουν τη φεβουξοστάτη με μία ή περισσότερες ομάδες ελέγχου, αναφέραμε τα ανεπιθύμητα συμβάντα συμπεριλαμβανομένων των καρδιαγγειακών συμβαμάτων, συμπεριελήφθηκε η περίοδος παρακολούθησης οποιουδήποτε μήκους και οι δημοσιεύσεις στα αγγλικά. Εξαιρέσαμε ανασκοπήσεις, μελέτες κοχόρτης, cross-sectional εργασίες και αναφορές περιπτώσεων.
2.4. Κριτήρια Επιλογής. Δύο ερευνητές (JC και JB) επανεξέτασαν την περίληψη κάθε παραπομπής και ταυτοποίησαν περιλήψεις για επανεξέταση πλήρους κειμένου. Η επιλογήενός άρθρου για ανασκόπηση πλήρους κειμένου αξιολογήθηκε από τους δύο ερευνητές. Η συμφωνία για το κατά πόσον θα εξεταστεί το πλήρες κείμενο ή η ενσωμάτωση του άρθρου στον πίνακα αποδεικτικών στοιχείων υπολογίστηκε με τη χρήση συμφωνίας interrater.
2.5. Συλλογή Δεδομένων. Ένας ερευνητής (JC) ήταν υπεύθυνος για τη συμπλήρωση του πίνακα αποδεικτικών στοιχείων και ένας δεύτερος ερευνητής (JB) επιβεβαίωσε την ακρίβεια των δεδομένων που συλλέχθηκαν. Οι διαφορές μεταξύ των δύο τελικών κριτών επιλύθηκαν με συναίνεση με τον ανώτερο ερευνητή (LT). Από κάθε μελέτη συλλέξαμε τον πληθυσμό, την ένδειξη για τη χρήση φαρμάκων που ελαττώνουν το ουρικό οξύ, τα δημογραφικά στοιχεία, τα συγχορηγούμενα φάρμακα που χρησιμοποιήθηκαν στη μελέτη, το χρόνο παρακολούθηση, την επικράτηση παραγόντων καρδιαγγειακού κινδύνου, τον αριθμός εξάρσεων της ουρικής αρθρίτιδας και τη συχνότητα εμφάνισης καρδιαγγειακών συμβαμάτων κατά τη διάρκεια της περιόδου παρακολούθησης.
2.6. Ποιοτική Ανάλυση. Επειδή συμπεριελάβαμε μόνο τυχαιοποιημένες ελεγχόμενες μελέτες χρησιμοποιήσαμε τον κατάλογο ελέγχου 11-σημείωνΚριτικής Αξιολόγησης Ικανοτήτωνγια την αξιολόγηση της ποιότητας κάθε μελέτης45. Για να περιγράψουμε καλύτερα τις πιθανές πηγές προκατάληψης, αναφέραμε τις βασικές μετρήσεις ποιότητας: απόκρυψη κατανομής, απώλεια παρακολούθησης, διασταύρωση, πρόθεση για ανάλυση, επιτυχία τυχαιοποίησης, υπολογισμός μεγέθους δείγματος, έλλειψη δεδομένων, προκατάληψη απόσυρσης και μεροληψία μέτρησης. Δύο ερευνητές ήταν υπεύθυνοι για την ολοκλήρωση της αξιολόγησης της ποιότητας (JC και JB). Οι διαφορές μεταξύ των κριτών επιλύθηκαν με συναίνεση (υπό την καθοδήγηση της LT) και υπολογίσαμε τη συμφωνία μεταξύ των συνεργατών.
2.7. Ομάδες Φαρμάκων. Το κύριο φάρμακο ενδιαφέροντος ήταν η φεβουξοστάτη. Συγκρίναμε την επίδραση της φεβουξοστάτης με τις ομάδες ελέγχου οι οποίες ορίζονται ως εικονικό φάρμακο, αλλοπουρινόλη ή άλλα φάρμακα που ελαττώνουν το ουρικό οξύ, συμπεριλαμβανομένου της τοπιροξοστάτης και της βενζοβρωμαρόνης. Η λογική της ομαδοποίησης του εικονικού φαρμάκου και όλων των άλλων φαρμάκων ως μιας ομάδας ελέγχου οφείλεται στον μικρό αριθμό ελεγχόμενων με εικονικό φάρμακο δοκιμών (n=4). Ωστόσο, πραγματοποιήσαμε μια ανάλυση ευαισθησίας που περιλαμβάνει μόνο μελέτες που συνέκριναν τη φεβουξοστάτη και το εικονικό φάρμακο. Δεν συμπεριελάβαμε τη λεσινουράφη στις αναλύσεις μας, καθώς εγκρίθηκε μόνο για χρήση με αλλοπουρινόλη ή φεβουξοστάτη και δεν αξιολογήσαμε την ατομική επίδραση του φαρμάκου. Για να αξιολογηθεί κατά πόσο η δοσολογία της φεβουξοστάτης συσχετίστηκε με καρδιαγγειακά περιστατικά, ταξινομήσαμε όλες τις μελέτες είτε ως υψηλής δόσης (≥80mg) είτε ως χαμηλής δόσης (<80mg). Επιλέξαμε αυτό το μέγεθος ως προηγούμενη μετα-ανάλυση για την αποτελεσματικότητα του φαρμάκου που χρησιμοποίησε τα ίδια μεγέθη.8
2.8. Πρωτογενές και Δευτερογενές Αποτέλεσμα. Το κύριο αποτέλεσμα ήταν τα σημαντικάανεπιθύμητα καρδιαγγειακά επεισόδια (MACE). Ορίσαμε ως MACE το μη-θανατηφόρο έμφραγμα του μυοκαρδίου (EM), στηθάγχη, καρδιακή ανεπάρκεια, ισχαιμικές διαταραχές της στεφανιαίας αρτηρίας και καρδιαγγειακό θάνατο.21 Για να αξιολογήσουμε την επίδραση της φεβουξοστάτης σε μεμονωμένα αποτελέσματα, διεξήγαμε μια ανάλυση για τα δευτερογενή αποτελέσματα τα οποία ορίστηκαν ως ισχαιμική καρδιακή νόσος (συμπεριλαμβανομένης της ασταθούς στηθάγχης με επαναγγείωση της στεφανιαίας), του μη θανατηφόρου εμφράγματος του μυοκαρδίου και τον καρδιαγγειακό θάνατο.
Για την ποσοτική μας ανάλυση συμπεριλήφθηκαν μόνο 10 μελέτες οι οποίες ανέφεραν είτε το πρωτεύον είτε το δευτερογενές αποτέλεσμα που ορίστηκε προηγουμένως. Οι υπόλοιπες μελέτες δεν συμπεριλήφθηκαν στην ποσοτική ανάλυση.
2.9. Ανάλυση Υποομάδων. Για να αξιολογηθεί εάν τα αποτελέσματα επηρεάστηκαν από συγχεόμενους παράγοντες, συλλέξαμε τις ακόλουθες πληροφορίες από κάθε μελέτη: η μελέτη περιελάμβανε υπερουριχαιμικούς ασθενείς ή μόνο ασθενείς με ουρική αρθρίτιδα, συγχορηγούμενα φάρμακα που θα μπορούσαν να επηρεάσουν τον καρδιαγγειακό κίνδυνο46 όπως τα μη στεροειδή αντιφλεγμονώδη φάρμακα (NSAIDs) και η ασπιρίνη, βασικό καρδιαγγειακό κίνδυνο, συμπεριλαμβανομένης της στεφανιαίας νόσου και των καρδιαγγειακών παραγόντων κινδύνου και τέλος τον αριθμό των εξάρσεων ουρικής αρθρίτιδας στην ομάδα της φεβουξοστάτης ως δείκτη φλεγμονής. Ορίσαμε ως μελέτη αξιολόγησης της ουρικής αρθρίτιδας εάν όλοι οι ασθενείς που συμπεριλήφθηκαν στη μελέτη είχαν ουρική αρθρίτιδα και ορίσαμε ως υπερουριχαιμία εκείνες τις μελέτες που περιελάμβαναν υποκείμενα βασισμένα σε αυξήσεις του ουρικού οξέος μόνο. Αναφέρθηκε επίσης ο χρόνος των καρδιαγγειακών συμβάντων με μελέτη.
2.10. Στατιστική Ανάλυση. Αναφέραμε τα σχετικά βασικά χαρακτηριστικά ως βασικές τιμές με το τεταρτοταγές εύρος (IQR). Για να εκτιμηθεί η ετερογένεια μεταξύ των μελετών, χρησιμοποιήσαμε την στατιστική chi-square της Cochran Q και την στατιστική I- square. Καθορίσαμε την ετερογένεια ως I- square μεγαλύτερο από 50%. Για την ποσοτική ανάλυση χρησιμοποιήσαμε το Stata 14 (StataCorp LP, College Station, TX). Αξιολογήσαμε τη μεροληψία της δημοσίευσης χρησιμοποιώντας τη μέθοδο του Egger. Υπολογίσαμε τον συγκεντρωμένο σχετικό κίνδυνο (RR) του πρωτογενούς και δευτερογενούς αποτελέσματος με τα αντίστοιχα διαστήματα εμπιστοσύνης (CIs) 95% για τη φεβουξοστάτη συγκριτικά με την ομάδα ελέγχου χρησιμοποιώντας τη μέθοδο fixed effects.
Επίσης, διεξήγαμε μια επαναξιολόγηση για την πρωταρχική και δευτερογενή έκβαση ως εξαρτώμενη μεταβλητή47, στη συνέχεια υπολογίσαμε τον εκτεταμένο βήτα συντελεστή χρησιμοποιώντας το μοντέλο τυχαίων αποτελεσμάτων και συμπεριλάβαμε τον καρδιαγγειακό κίνδυνο βασικής γραμμής, τον χρόνο παρακολούθησης, την ουρική αρθρίτιδα έναντι υπερουριχαιμίας, τη χρήση NSAID ή ασπιρίνης και τον αριθμό των εξάρσεων ουρικής αρθρίτιδας στο πρότυπο.
3. Αποτελέσματα
3.1. Αναζήτηση Βιβλιογραφίας. Το Σχήμα 1 δείχνει το διάγραμμα ροής των συμπεριλαμβανόμενων και αποκλεισμένων μελετών. Η αναζήτησή μας ανέδειξε 374 περιλήψεις από το PubMed, 110 από το EMBASE και 18 από τα πρωτόκολλα της κλινικής database.traval.gov. Από τις συνολικά 502 παραπομπές αφαιρέσαμε 91 διπλές περιλήψεις. Εξαιρέσαμε 358 μελέτες σε αφηρημένο επίπεδο και επιλέξαμε 53 για επανεξέταση πλήρους κειμένου. Από αυτές εξαιρέσαμε 28. Έτσι, τελικά συμπεριλήφθηκαν 25 μελέτες. Η συμφωνία Interrater μεταξύ κριτών σχετικά με την ένταξη έναντι του αποκλεισμού των μελετών ήταν 100%. Από το αρχείο clinicaltrials.gov, ανακτήσαμε πρόσθετα δεδομένα καρδιαγγειακών συμβαμάτων για 5 από τις 25 δημοσιευμένες μελέτες.25,38-41 Μεταξύ των 25 περιλαμβανομένων μελετών, 10 ανέφεραν MACE και 15 δεν ανέφεραν καρδιαγγειακό συμβάν κατά την παρακολούθηση.
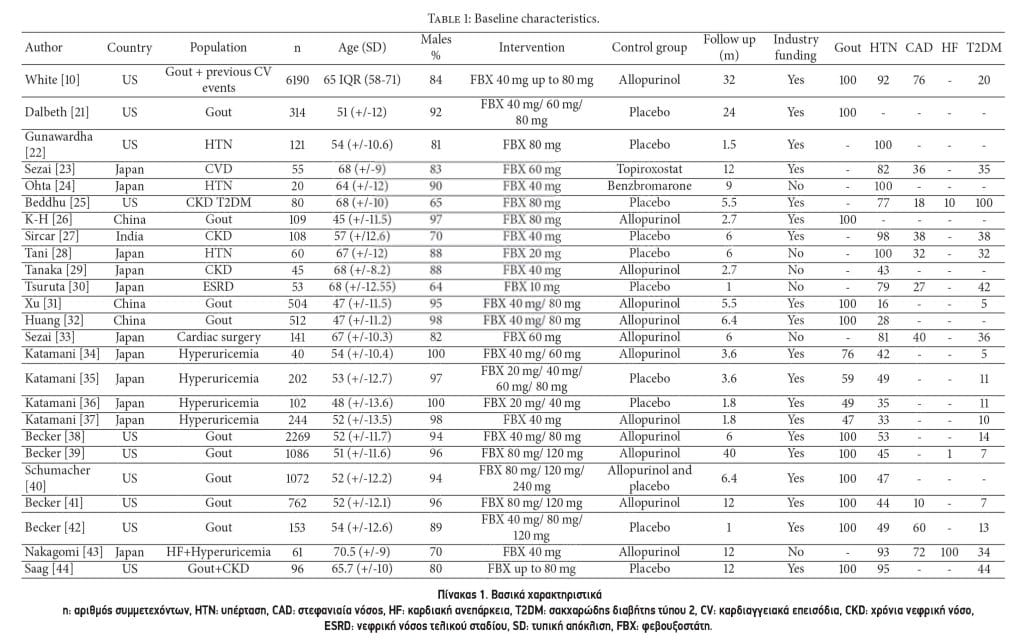
3.2. Χαρακτηριστικά Αναφοράς. Ο Πίνακας 1 παρουσιάζει τα βασικά χαρακτηριστικά των 25 μελετών που περιλαμβάνονται στην ποιοτική ανασκόπηση. Οι μελέτες περιελάμβαναν 14.402 συμμετέχοντες με υπερουριχαιμία: 8.602 (59%) έλαβαν φεβουξοστάτη, 5.118 (36%) αλλοπουρινόλη και 643 (4%) placebo. Η μέση ηλικία των συμμετεχόντων στη δοκιμή ήταν 54 έτη (IQR 52-67) και 90 % (IQR 82-96) ήταν άνδρες. Η μέση παρακολούθηση των μελετών ήταν 6 μήνες (IQR 2.7-12), 53% (IQR 43-92) είχαν υπέρταση και 32% (IQR 11-38) είχαν διαβήτη.
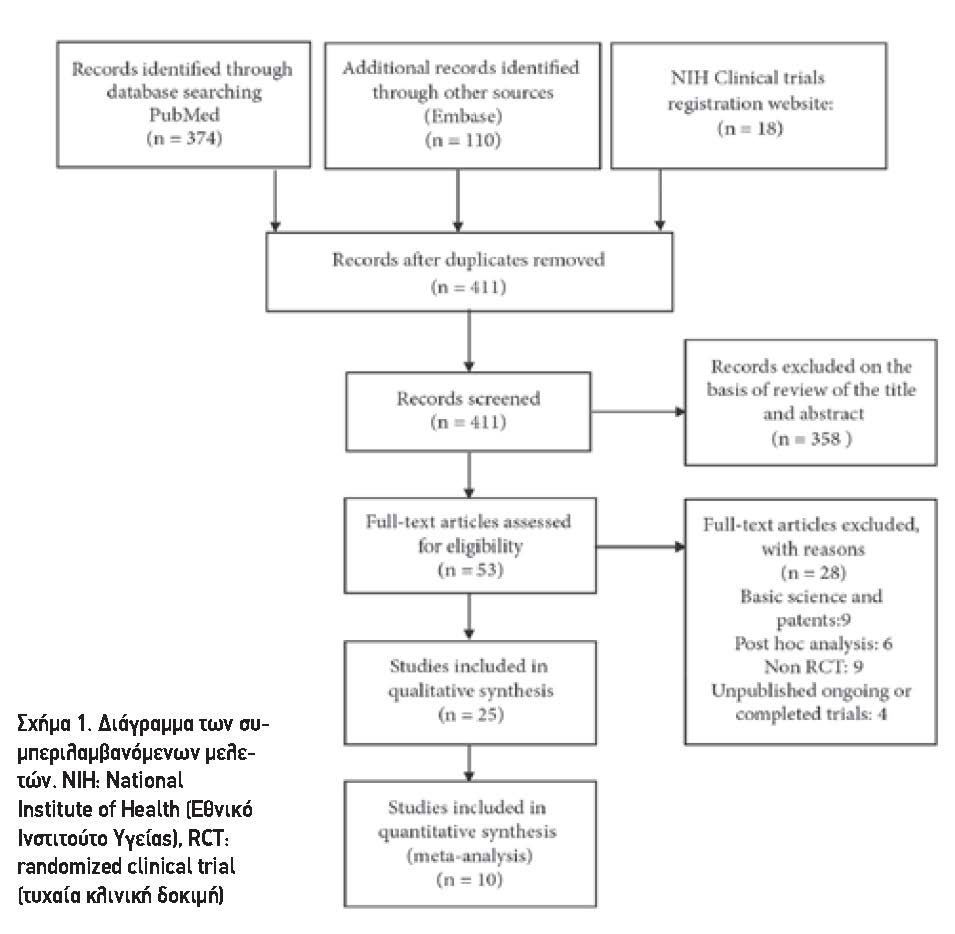
Οι μελέτες που ανέφεραν καρδιαγγειακά συμβάντα είχαν μέση παρακολούθηση 12 μηνών (IQR 6.4-24) σε σύγκριση με μελέτες που δεν ανέφεραν καρδιαγγειακά περιστατικά και στα οποία η μέση παρακολούθηση ήταν 3,6 μήνες (IQR 1,8-6). Εννέα από τις 15 μελέτες που δεν ανέφεραν καρδιαγγειακά περιστατικά που αξιολόγησαν τη φεβουξοστάτη σε διάφορες καρδιαγγειακές παθήσεις. Μόνο δέκα από τις μελέτες διεξήχθησαν αποκλειστικά στη Βόρεια Αμερική. Δώδεκα από τις μελέτες συνέκριναν τη φεβουξοστάτη με την αλλοπουρινόλη. Οι υπόλοιπες μελέτες συνέκριναν τη φεβουξοστάτη με το εικονικό φάρμακο (10), για αμφότερα το εικονικό φάρμακο όσο και στην αλλοπουρινόλη (1), την τοπιροξόστατη (n=1) και τη βενζβρωμαρόνη (n=1).
Έντεκα μελέτες περιελάμβαναν ασθενείς με ουρική αρθρίτιδα αποκλειστικά, 5 ασθενείς που είχαν αποθεραπευθεί με υπερουριχαιμία και χωρίς ενδείξεις ουρικής αρθρίτιδας και οι υπόλοιπες 9 μελέτες περιελάμβαναν ασθενείς με καρδιαγγειακά νοσήματα.
3.3. Ποιοτική Αξιολόγηση. Ο συντελεστής βήτα για τη μεροληψία της δημοσίευσης ήταν 0,30, 95% CI -0,81-1,42, p=0,53. Από την ποιοτική μας αξιολόγηση διαπιστώσαμε ότι και οι τρεις μελέτες ήταν τυφλές. Αποτελέσματα εκτός από το ουρικό οξύ σπάνια αναφέρθηκαν, ιδιαίτερα σε σύντομες μελέτες παρακολούθησης που αποσκοπούσαν στην αξιολόγηση της ασφάλειας της φεβουξοστάτης σε ασθενείς με παράγοντες καρδιαγγειακού κινδύνου. Η μελέτη CARES ήταν η μοναδική μελέτη που σχεδιάστηκε για να αξιολογήσει τη μακροπρόθεσμη καρδιαγγειακή ασφάλεια της φεβουξοστάτης ως κύριο τελικό σημείο. Παρά τη σπουδαιότητά της, η δοκιμή CARES είχε σημαντικό περιορισμό, σχεδόν το 57% των ασθενών διέκοψε πρόωρα τη δοκιμαστική θεραπεία και το 45% των συμμετεχόντων δεν ολοκλήρωσε την παρακολούθηση, κάτι το οποίο θα μπορούσε να έχει σημαντικές επιπτώσεις στα αποτελέσματα. Ωστόσο, ο αριθμός των συμμετεχόντων που διέκοψαν τη δοκιμή και δεν ολοκλήρωσαν την παρακολούθηση ήταν παρόμοιος και στα δύο σκέλη της μελέτης.
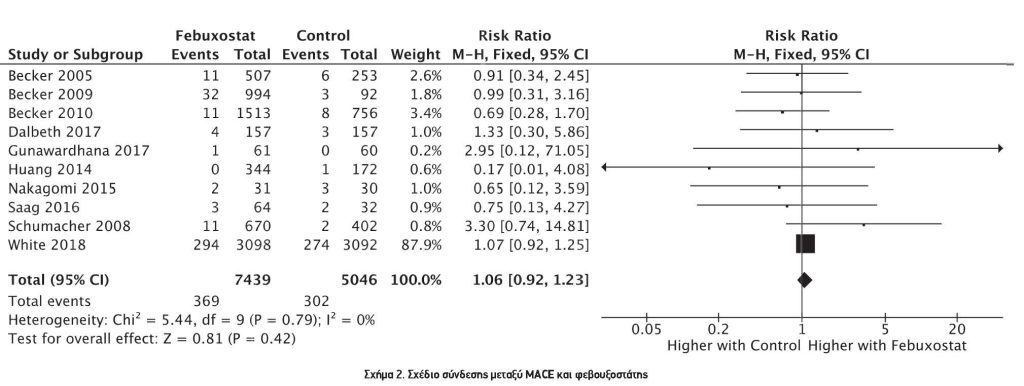
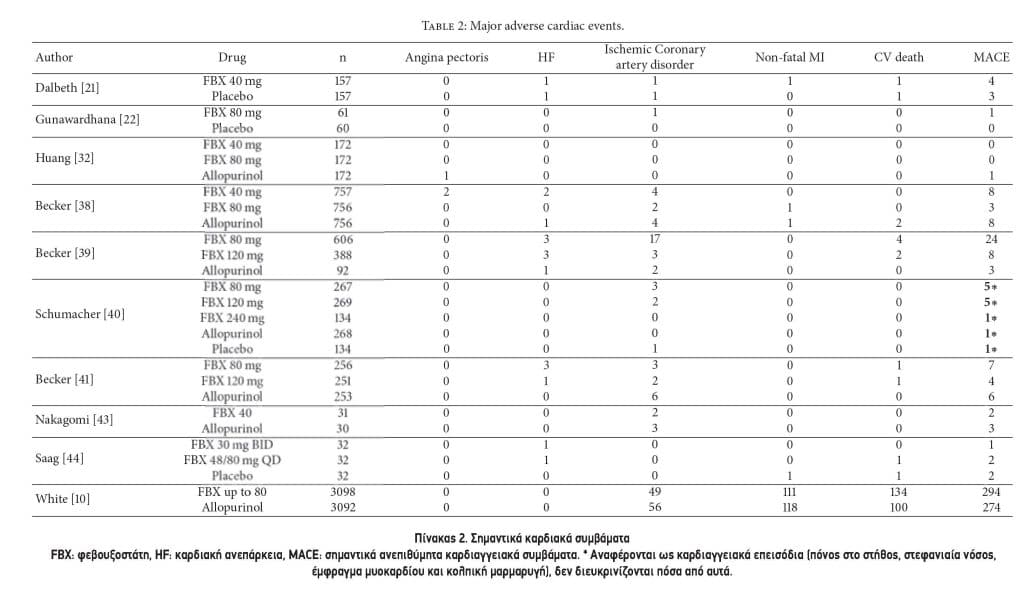
3.4. Σύνδεση Μεταξύ Φεβουξοστάτης και MACE. Δέκα μελέτες (Πίνακας 2) ανέφεραν τη σχέση μεταξύ φεβουξοστάτης και MACE.10,21,22,32,38-41,43,44 Εννέα από αυτές τις μελέτες περιελάμβαναν ασθενείς με ιστορικό είτε υπέρτασης, καρδιακής ανεπάρκειας είτε διαταραχής στεφανιαίας αρτηρίας, ενώ η μελέτη CARES είχε το υψηλότερο ποσοστό. Το Σχήμα 2 δείχνει τη σχέση μεταξύ της φεβουξοστάτης και του MACE σε σύγκριση με τις ομάδες ελέγχου. Το RR της MACE για οποιαδήποτε δόση φεβουξοστάτης ήταν 1,06, 95% CI 0.92-1.23 (p=0.42) με Ι- square 0%. To RR του MACE για οποιαδήποτε δόση φεβουξοστάτης όταν η ομάδα ελέγχου ήταν εικονικό φάρμακο ήταν 1.81, 95% CI 0.72-4.53 (p=0.20). Το RR του MACE για χαμηλή δόση φεβουξοστάτης ήταν 1.03, 95% CI 0,65-1,66 (p=0,43). Το RR της MACE για υψηλή δόση φεβουξοστάτης ήταν 0,98. 95% CI 0,47-2,04 (p=0,97). Μόνο δύο μελέτες ανέφεραν το χρονοδιάγραμμα των καρδιαγγειακών συμβάντων και οι περισσότερες από αυτές συνέβησαν εντός 24 μηνών από την έκθεση στο φάρμακο.
3.5. Σύνδεση Μεταξύ Φεβουξοστάτης και Δευτερογενούς Αποτελέσματος. Έξι μελέτες ανέφεραν τη δευτερογενή έκβαση.10,21,38,39,41,44 Το RR του καρδιαγγειακού θανάτου για τη φεβουξοστάτη ήταν 1.29, 95% CI 1,01-1,66, p=0,03. Όταν αποκλείστηκε η μεγαλύτερη μελέτη (CARES)10, το RR του καρδιαγγειακού θανάτου για τη φεβουξοστάτη ήταν 0.73, 95% CI 0.24-2.25, p=0.64.
3.6. Ανάλυση Υποομάδων. Για την πρωτογενή έκβαση, είχαμε τα ακόλουθα: η επαναξιολόγηση των βήτα-coefficients για την ουρική αρθρίτιδα (1,63), ο αριθμός των εξάρσεων της ουρικής αρθρίτιδας (1,00), η στεφανιαία νόσος (1,00), ο χρόνος παρακολούθησης (1,00) η ασπιρίνη (1,00), όλα με τιμή p>0,05. Για τη δευτερογενή έκβαση, ισχύουν τα ακόλουθα: οι επαναξιολογήσεις συντελεστές-βήτα για τη στεφανιαία νόσο (1,70), ο αριθμός των εξάρσεων ουρικής αρθρίτιδας (1,00), ο χρόνος παρακολούθησης (1,00), το NSAID (1,02) και η ασπιρίνη (0,98) όλα με τιμή p>0,05.
4. Συζήτηση
Η μελέτη μας διαπίστωσε ότι η φεβουξοστάτη δεν αυξάνει τον συνολικό κίνδυνο σημαντικών δυσμενών καρδιαγγειακών συμβαμάτων σε ασθενείς με ουρική αρθρίτιδα και υπερουριχαιμία. Ωστόσο, η ανάλυσή μας έδειξε επίσης αυξημένο κίνδυνο καρδιαγγειακού θανάτου με φεβουξοστάτη. Δεν απεδείχθει ότι η χρήση CAD, NSAID ή ασπιρίνης, ο αριθμός των flares ουρικής αρθρίτιδας ή μόνο οι ασθενείς με ουρική αρθρίτιδα ήταν παράγοντες που σχετίζονταν με τον καρδιαγγειακό θάνατο.
Το αυξημένο ουρικό οξύ συσχετίζεται με την αύξηση της συχνότητας καρδιακής ανεπάρκειας48,49, της θνησιμότητας της καρδιακής ανεπάρκειας4, της περιστασιακής υπέρτασης50, της περιστασιακής κολπικής μαρμαρυγής3 και της ισχαιμικής καρδιοπάθειας.51. Αυτό το εύρημα κατέστησε το ουρικό οξύ ως έναν θεραπευτικό στόχο για τη βελτίωση των καρδιαγγειακών αποτελεσμάτων τροποποιώντας την ισορροπία νιτροζο / οξειδοαναγωγής. Ωστόσο, η αλλοπουρινόλη δεν έχει βελτιώσει τα αποτελέσματα στην καρδιακή ανεπάρκεια.6,52 Ως εκ τούτου, υπάρχει ανάγκη για νεότερα φάρμακα που μπορούν να επηρεάσουν την ισορροπία νιτροζο / οξειδοαναγωγής.
Το FDA απαίτησε από την Takeda Pharmaceuticals9 να διεξαγάγει μια κλινική μελέτη καρδιαγγειακής ασφάλειας βασισμένη σε αποτελέσματα κλινικών δοκιμών39,40 και παρατηρητικά δεδομένα53 που δείχνουν πιθανή υπέρβαση των καρδιαγγειακών συμβαμάτων πριν εγκριθούν το 2009. Τον Νοέμβριο του 2017 το FDA δημοσίευσε μια προειδοποίηση ασφάλειας με βάση τα αποτελέσματα της καρδιαγγειακής ασφάλειας της φεβουξοστάτης ή της αλλοπουρινόλης σε ασθενείς με ουρική αρθρίτιδα (μελέτη CARES). Η μελέτη είχε τυχαιοποιημένο, διπλό, τυφλό σχεδιασμό και περιελάμβανε ασθενείς με ουρική αρθρίτιδα και ιστορικό μείζονος καρδιαγγειακής νόσου και δεν βρήκε αύξηση στην πρωτογενή έκβαση του MACE και ο οποίος ορίστηκε σε αυτό το RCT ως καρδιαγγειακά σχετιζόμενος θάνατος, μη θανατηφόρο ΕM, μη θανατηφόρο αγγειακό εγκεφαλικό επεισόδιο και ασταθής στηθάγχη και τα οποία απαιτούν επείγουσα επαναγγείωση, αλλά διαπίστωσαν αύξηση του κινδύνου των δευτερογενών καταληκτικών σημείων καρδιαγγειακού θανάτου και θανάτου από όλες τις αιτίες πρόθεσης θεραπείας και ανά πρωτόκολλο αναλύσεις. Λόγω του ειδικού σχεδιασμού της CARES αλλά και επειδή ήταν το μοναδικό RCT που δημοσιεύθηκε με επικέντρωση στη μέτρηση της καρδιοαγγειακής ασφάλειας της φεβουξοστάτης, αποτέλεσε το 80% της συγκεντρωτικής ανάλυσης.
Υπάρχουν αρκετές πιθανές εξηγήσεις για τα ευρήματά μας και αυτά της μελέτης CARES. Πρώτον, η χρήση των NSAID έχει συσχετιστεί με αυξανόμενα ποσοστά καρδιαγγειακών συμβαμάτων54 και είναι πιθανό ότι η χρήση NSAID για την προφύλαξη από ουρική αρθρίτιδα και/ή τη θεραπεία μπορεί να διακινδυνεύσουν τα δεδομένα. Ενώ δεν παρατηρήσαμε αποτελέσματα από τη χρήση NSAID, αυτά δεν ήταν καλώς τεκμηριωμένα στις συμπεριλαμβανόμενες μελέτες και μπορεί να είχαν μη μετρήσιμα αποτελέσματα. Δεύτερον, οι τιμές ουρικής αρθρίτιδας και η δυσπιστία που συνεπάγεται έχουν συσχετιστεί με έμφραγμα του μυοκαρδίου.55 Ωστόσο, στη μελέτη CARES, η χρήση NSAID και οι εξάρσεις της ουρικής αρθρίτιδας ήταν παρόμοια μεταξύ εκείνων που χρησιμοποιούσαν φεβουξοστάτη και αλλοπουρινόλη. Η κολχικίνη, η οποία έχει προταθεί ότι μειώνει αντί να αυξάνει τον καρδιαγγειακό κίνδυνο, χρησιμοποιείται επίσης για την προφύλαξη από ουρική αρθρίτιδα και για την οξεία θεραπεία, αλλά τα διαθέσιμα δεδομένα στις μελέτες δεν επέτρεψαν την αυστηρή ανάλυση του κατά πόσο η χρήση κολχικίνης θα μπορούσε να έχει προκαλέσει τα αποτελέσματά μας. Τρίτον, η αναστολή της οξειδάσης της ξανθίνης θα μπορούσε να διαταράξει τη δραστηριότητα της σύνθεσης του νιτρικού οξειδίου56, η οποία με τη σειρά της μπορεί να ελαττώσει τη στεφανιαία αιματική ροή και να προκαλέσει ανεπάρκεια συστολής διέγερσης με μυοκαρδιακή σύζευξη.6,56 Παραδόξως, όμως, το ίδιο το ουρικό οξύ έχει επίσης αποδειχθεί ότι αναστέλλει την ικανότητα των ενδοθηλιακών κυττάρων να απεκκρίνουν το νιτρικό οξείδιο.57,58 Η φύση της μετα-ανάλυσής μας δεν μας επέτρεψε να εκτιμήσουμε την επίπτωση και την ισορροπία των σχετικών επιδράσεων της αναστολής του μονοξειδίου του αζώτου και της ελαττώσεως του ουρικού οξέος στη στεφανιαία ροή του αίματος.
Η μελέτη μας διαπίστωσε επίσης ότι αρκετές μελέτες διεξήχθησαν σε βιογραφικούς πληθυσμούς με διαφορετικό κίνδυνο για καρδιαγγειακά συμβάματα, αλλά οι οποίοι είχαν σύντομη παρακολούθηση και δεν κατέστη δυνατόν να εντοπίσουν τα καρδιαγγειακά συμβάματα. Όλες αυτές οι μελέτες χρηματοδοτήθηκαν από την εταιρεία παραγωγής της φεβουξοστάτης. Τυπικά, οι μελέτες φάσης 2 και 3 μπορούν να διαπιστώσουν κοινά θέματα ασφαλείας, αλλά ενδέχεται να μην έχουν επαρκές εύρος ή διάρκεια για να διαπιστώσουν σημαντικά αλλά λιγότερο συνήθη γεγονότα.
Η παρούσα μελέτη δεν μπόρεσε να διαπιστώσει ένα προφίλ κινδύνου δεδομένου ότι οι παράγοντες που συμπεριελήφθηκαν στην επαναξιολόγηση ήταν μη σημαντικοί. Ωστόσο, οι υψηλότεροι παράγοντες κινδύνου παρατηρήθηκαν με την παρουσία στεφανιαίας νόσου κατά την έναρξη και με εκείνες τις μελέτες που εξέταζαν αποκλειστικά τη φεβουξοστάτη σε ασθενείς με ουρική αρθρίτιδα.
Τα πλεονεκτήματα της μελέτης μας περιλαμβάνουν την εκτενή αναζήτηση καρδιαγγειακών συμβαμάτων, συμπεριλαμβανομένων μόνο των τυχαιοποιημένων κλινικών μελετών, τον αριθμό των μελετών αυτών και την αξιολόγηση πιθανών εξηγήσεων για τον υπερβολικό κίνδυνο.
Παρά τα δυνατά σημεία, η μελέτη μας έχει σημαντικούς περιορισμούς που αξίζει να αναφερθούν. Πρώτον, παρά το γεγονός ότι ο αριθμός των μελετών και των ασθενών ήταν σημαντικά μεγαλύτερος σε αυτές τις μελέτες, ο αριθμός του MACE ή οποιουδήποτε καρδιαγγειακού συμβάματος ήταν χαμηλός και στις δύο ομάδες. Αυτό μπορεί να εξηγηθεί από τη χαμηλή επίπτωση του κινδύνου ή από το γεγονός ότι η καρδιαγγειακή ασφάλεια δεν ήταν το κύριο τελικό σημείο σε όλες εκτός από μία από τις περιλαμβανόμενες μελέτες10, μαζί με τη σύντομη παρακολούθηση των περισσότερων μελετών. Δεύτερον, τα κριτήρια αποκλεισμού σε ορισμένες μελέτες εμπόδισαν τους ασθενείς με ιστορικό καρδιαγγειακής νόσου να συμμετάσχουν στις μελέτες τους, μειώνοντας έτσι τον αριθμό των ασθενών που διατρέχουν τον κίνδυνο να αναπτύξουν MACE. Τρίτον, όλες οι μελέτες δεν ανέφεραν με συνέπεια τα δεδομένα σχετικά με τη χρήση των ΜΣΑΦ, της ασπιρίνης και το καρδιαγγειακό επίπεδο κινδύνου των συμπεριληφθέντων ασθενών. Τέταρτον, τα ευρήματά μας σχετικά με την αυξανόμενη θνησιμότητα από καρδιαγγειακά συμβάματα οδηγείτο από το μεγάλο μέγεθος δείγματος και ποσοστό συμβαμάτων της μελέτης CARES.10 Τέλος, το δυνητικά σημαντικό ζήτημα που τέθηκε από τη μελετη CARES, το εάν η φεβουξοστάτη μπορεί ανεξάρτητα να αυξήσει ή να μειώσει τον κίνδυνο θανάτου που σχετίζεται με καρδιαγγειακά συμβάματα, αλλά σε μικρότερο βαθμό από ό,τι η αλλοπουρινόλη, δεν ήταν δυνατόν να προσδιοριστεί δεδομένης της μεθοδολογίας μας και των δεδομένων.
Συμπερασματικά, η μετα-ανάλυση των διαθέσιμων μελετών δείχνει ότι ενώ η φεβουξοστάτη δεν αυξάνει ούτε μειώνει τον κίνδυνο σοβαρών δυσμενών καρδιαγγειακών εκβάσεων σε υπερουριχαιμικούς ασθενείς, μπορεί να αυξήσει τον κίνδυνο καρδιαγγειακού θανάτου σε ασθενείς με ουρική αρθρίτιδα και ιστορικό προηγούμενων καρδιαγγειακών περιστατικών. Λόγω του υψηλού επιπολασμού και της χρόνιας φύσης της ουρικής αρθρίτιδας, συνιστάται προσοχή όταν αποφασίζεται εάν θα χρησιμοποιηθεί η φεβουξοστάτη σε ασθενείς υψηλού κινδύνου καρδιαγγειακών συμβαμάτων. Απαιτούνται περισσότερες μελέτες RCT οι οποίες θα μετρούν την καρδιαγγειακή ασφάλεια ως το κύριο αποτέλεσμα για την επαρκή αξιολόγηση του κινδύνου καρδιαγγειακής νόσου με τη φεβουξοστάτη.
ΒΙΒΛΙΟΓΡΑΦΙΑ
- H. K. Choi and G. Curhan. Independent impact of gout onmortality and risk for coronary heart disease. Circulation, vol.116, no. 8, pp. 894–900, 2007.
- L. Tamariz, F. Hernandez, A. Bush, A. Palacio, and J. M. Hare. Association between serum uric acid and atrial fibrillation: Asystematic review and meta-analysis. Heart Rhythm, vol. 11, no.7, pp. 1102–1108, 2014.
- L. Tamariz, S. Agarwal, E. Z. Soliman et al., “Associationof serum uric acid with incident atrial fibrillation (from theatherosclerosis risk in communities [ARIC] study),” AmericanJournal of Car- diology, vol. 108, no. 9, pp. 1272–1276, 2011.
- L. Tamariz, A. Harzand, A. Palacio, S. Verma, J. Jones, and J.Hare, “Uric acid as a predictor ofall- cause mortality in heartfailure: a meta-analysis,” Congestive Heart Failure, vol. 17, no. 1,pp. 25– 30, 2011.
- J. E. Jun, Y.-B. Lee, S.-E. Lee et al., “Elevated serum uricacid predicts the development of mod- erate coronary arterycalcification independent of conventional cardiovascular riskfactors,” Ath- erosclerosis, vol. 272, pp. 233–239, 2018.
- L. Tamariz and J. M. Hare, “Xanthine oxidase inhibitors in heartfailure: where do we go from here?” Circulation, vol. 131, no. 20,pp. 1741–1744, 2015.
- M. Bredemeier, L. M. Lopes, M. A. Eisenreich et al., “Xanthineoxidase inhibitors for prevention of cardiovascular events: Asystematic review and meta-analysis of randomized controlledtrials,” BMC Cardiovascular Disorders, vol. 18, no. 1, p. 24, 2018.
- L. I. Faruque, A. Ehteshami-Afshar, N. Wiebe, L. Tjosvold, J.Homik, and M. Tonelli, “A systematic review and meta-analysison the safety and efcacy of febuxostat versus allopurinol inchronic gout,” Seminars in Arthritis and Rheumatism, vol. 43,no. 3, pp. 367–375, 2013.
- U S Food and Drug Administration (FDA), “Uloric (febuxostat): Drug Safety Communication – FDA to Evaluate IncreasedRisk of Heart-related Death,” 2018.
- W. B. White, K. G. Saag, M. A. Becker et al., “Cardiovascularsafety of febuxostat or allopurinol in patients with gout,” TheNew England Journal of Medicine, vol. 378, no. 13, pp. 1200–1210,2018.
- C. Borghi and F. Perez-Ruiz, “Urate lowering therapies inthe treatment of gout: a systematic re- view and meta-analysis,”European Review for Medical and Pharmacological Sciences, vol.20, pp. 983–992, 2016.
- I. Castrejon, E. Toledano, M. P. Rosario, E. Loza, F. Perez-Ruiz,and L. Carmona, “Safety ofallopurinol compared with otherurate-lowering drugs in patients with gout: a systematic reviewand meta-analysis,” Rheumatology International, vol. 35, no. 7,pp. 1127–1137, 2015.
- S. Li, H. Yang, Y. Guo et al., “Comparative efficacy and safetyof urate-lowering therapy for the treatment of hyperuricemia:a systematic review and network meta-analysis,” ScientificReports, vol. 6, no. 1, Article ID 33082, 2016.
- J. H. Tayar, M. A. Lopez-Olivo, and M. E. Suarez-Almazor,“Febuxostat for treating chronic gout,” Cochrane Database ofSystematic Reviews, vol. 11, Article ID CD008653, 2012.
- P. Ye, S. Yang, W. Zhang et al., “Efcacy and tolerability offebuxostat in hyperuricemic patients with or without gout: asystematic review and meta-analysis,” Clinical therapeutics, vol.35, no. 2, pp. 180–189, 2013.
- T. Kanji, M. Gandhi, C. M. Clase, and R. Yang, “Urate loweringtherapy to improve renal outcomes in patients with chronickidney disease: systematic review and meta-analysis,” BMCNephrology, vol. 16, p. 58, 2015.
- S. Kim, H.-J. Kim, H.-S. Ahn et al., “Renoprotective effectsof febuxostat compared with allopuri- nol in patients withhyperuricemia: A systematic review and meta-analysis,” KidneyResearch and Clinical Practice, vol. 36, no. 3, pp. 274–281, 2017.
- X. X. Zeng, Y. Tang, K. Hu et al., “Efficacy of febuxostat inhyperuricemic patients with mild-to-moderate chronic kidneydisease,” Medicine (Baltimore), vol. 97, no. 13, p. e0161, 2018.
- L.-H. Qu, H. Jiang, and J.-H. Chen, “Effeect of uric acid-lowering therapy on blood pressure: sys- tematic review and meta-analysis,” Annals of Medicine, vol. 49, no. 2, pp. 142–156, 2017.
- T. Zhang and J. E. Pope, “Cardiovascular effects of urate-lowering therapies in patients with- chronic gout: A systematicreview and meta-analysis,” Rheumatology (Oxford), vol. 56, no.7, pp. 1144–1153, 2017.
- N. Dalbeth, K. G. Saag, W. E. Palmer et al., “Effects of febuxostatin early gout: a randomized, dou- ble-blind, placebo-controlledstudy,” Arthritis & Rheumatology, vol. 69, no. 12, pp. 2386– 2395,2017.
- L. Gunawardhana, L. McLean, H. A. Punzi et al., “Effectof febuxostat on ambulatory blood pressure in subjectswith hyperuricemia and hypertension: a phase 2 randomizedplacebo-controlled study,” Journal of the American Heart Association, vol. 6, no. 11, 2017.
- A. Sezai, K. Obata, K. Abe, S. Kanno, and H. Sekino, “Crossover trial of febuxostat and topiroxo- stat for hyperuricemia withcardiovascular disease (TROFEO trial),” CirculationJournal,vol. 81, no. 11, pp. 1707–1712, 2017.
- Y. Ohta, A. Ishizuka, H. Arima et al., “Effective uric acid-lowering treatment for hypertensive patients with hyperuricemia,” Hypertension Research, vol. 40, no. 3, pp. 259–263,2017.
- S. Beddhu, R. Filipowicz, B. Wang et al., “A randomized controlled trial of the effects of febuxo- stat therapy on adipokinesand markers of kidney fibrosis in asymptomatic hyperuricemicpa- tients with diabetic nephropathy,” Canadian Journal of KidneyHealth and Disease, vol. 3, no. 1, Article ID 2054358116675343,2016.
- K.-H. Yu, J.-H. Lai, P.-N. Hsu, D.-Y. Chen, C.-J. Chen, and H.-Y.Lin, “Safety and efficacy of oral febuxostat for treatment of HLAB*5801-negative gout: a randomized, open-label, multicen- ter,allopurinol-controlled study,” Scandinavian Journal of Rheumatology, vol. 45, no. 4, pp. 304– 311, 2016.
- D. Sircar, S. Chatterjee, R. Waikhom et al., “Efficacy of febuxostat for slowing the GFR decline in patients with CKD andasymptomatic hyperuricemia: a 6-month, double-blind, randomized, placebo-controlled trial,” American Journal of KidneyDiseases, vol. 66, no. 6, pp. 945–950, 2015.
- S. Tani, K. Nagao, and A. Hirayama, “Effect of febuxostat, axanthine oxidase inhibitor, on cardio- vascular risk in hyperuricemic patients with hypertension: a prospective, open-label,pilot study,” Clinical Drug Investigation, vol. 35, no. 12, pp. 823–831, 2015.
- K. Tanaka, M. Nakayama, M. Kanno et al., “Renoprotectiveeffects of febuxostat in hyperuricemic patients with chronickidney disease: a parallel-group, randomized, controlled trial,”Clinical and Experimental Nephrology, vol. 19, no. 6, pp. 1044–1053, 2015.
- Y. Tsuruta, K. Kikuchi, Y. Tsuruta et al., “Febuxostat improvesendothelial function in hemodialy- sis patients with hyperuricemia: a randomized controlled study,” Hemodialysis International, vol. 19, no. 4, pp. 514–520, 2015.
- S. Xu, X. Liu, J. Ming et al., “A phase 3, multicenter, randomized,allopurinol-controlled study as- sessing the safety and efficacy oforal febuxostat in Chinese gout patients with hyper- uricemia,”International Journal of Rheumatic Diseases, vol. 18, no. 6, pp.669–678, 2015.
- X. Huang, H. Du, J. Gu et al., “An allopurinol-controlled, multicenter, randomized, double-blind, parallel between-group,comparative study of febuxostat in Chinese patients withgout and hy- peruricemia,” International Journal of RheumaticDiseases, vol. 17, no. 6, pp. 679–686, 2004.
- A. Sezai, M. Soma, K.-I. Nakata et al., “Comparison of febuxostat and allopurinol for hyperuricemia in cardiac surgerypatients with chronic kidney disease (NU-FLASH trial forCKD),” Journal of Car- diology, vol. 66, no. 4, pp. 298–303, 2015.
- K. Naoyuki, F. Shin, H. Toshikazu et al., “An allopurinol-controlled, multicenter, randomized, open- label, parallelbetween-group, comparative study of febuxostat (TMX-67), anon-purine- selective inhibitor of xanthine oxidase, in patientswith hyperuricemia including those with gout in Japan: phase2 exploratory clinical study,” Journal of Clinical Rheumatology:Practical Reports on Rheumatic & Musculoskeletal Diseases, vol.17, no. 4, pp. S44–S49, 2011.
- N. Kamatani, S. Fujimori, T. Hada et al., “Placebo-controlleddouble-blind dose-response study of the non-purine-selectivexanthine oxidase inhibitor febuxostat (TMX-67) in patientswith hy- peruricemia (including gout patients) in Japan: latephase 2 clinical study,” Journal of Clinical Rheumatology: Practical Reports on Rheumatic & Musculoskeletal Diseases, vol. 17, no.4, pp. S35–S43, 2011.
- K. Naoyuki, F. Shin, H. Toshikazu et al., “Placebo-controlled,double-blind study of the non-purine- selective xanthine oxidase inhibitor Febuxostat (TMX-67) in patients with hyperuricemia includ- ing those with gout in Japan: phase 3 clinicalstudy,” Journal of Clinical Rheumatology: Practical Reports onRheumatic & Musculoskeletal Diseases, vol. 17, no. 4, pp. S19–26,2011.
- N. Kamatani, S. Fujimori, T. Hada et al., “An allopurinol-controlled, randomized, double-dummy, double-blind, parallelbetween-group, comparative study of febuxostat (TMX-67), anon-purine- selective inhibitor of xanthine oxidase, in patientswith hyperuricemia including those with gout in Japan: phase3 clinical study,” Journal of Clinical Rheumatology: PracticalReports on Rheu- matic & Musculoskeletal Diseases, vol. 17, no. 4,pp. S13–S18, 2011.
- M. A. Becker, H. R. Schumacher, L. R. Espinoza et al., “Theurate-lowering efficacy and safetyof febuxostat in the treatmentof the hyperuricemia of gout: The CONFIRMS trial,” ArthritisResearch &Therapy, vol. 12, no. 2, article no. R63, 2010.
- M. A. Becker, H. R. Schumacher, P. A. MacDonald, E. Lloyd,and C. Lademacher, “Clinical efficacy and safety of successfullong-term urate lowering with febuxostat or allopurinol insubjects with gout,” The Journal of Rheumatology, vol. 36, no.6, pp. 1273–1282, 2009.
- H. R. Schumacher Jr., M. A. Becker, R. L. Wortmann etal., “Effects of febuxostat versus allopuri- nol and placebo inreducing serum urate in subjects with hyperuricemia and gout:A 28-week, phase III, randomized, double-blind, parallel-grouptrial,” Arthritis Care & Research, vol. 59, no. 11, pp. 1540–1548,2008.
- M. A. Becker, H. R. Schumacher Jr., R. L. Wortmann etal., “Febuxostat compared with allopurinol in patients withhyperuricemia and gout,” The New England Journal of Medicine,vol. 353, no. 23, pp. 2450–2461, 2005.
- M. A. Becker, H. R. Schumacher Jr., R. L. Wortmann et al.,“Febuxostat, a novel non-purine selec- tive inhibitor of xanthineoxidase: a twenty-eight–day, multicenter, phase II, randomized,double- blind, placebo-controlled, dose-response clinical trialexamining safety and efficacy in patients with gout,” Arthritis& Rheumatism, vol. 52, no. 3, pp. 916–923, 2005.
- A. Nakagomi, Y. Saiki, S. Noma et al., “Effects of febuxostatand allopurinol on the inflammation and cardiac functionin chronic heart failure patients with hyperuricemia,” IJCMetabolic and En- docrine, vol. 8, pp. 46–55, 2015.
- K. G. Saag, A. Whelton, M. A. Becker, P. MacDonald, B. Hunt,and L. Gunawardhana, “Impact of febuxostat on renal functionin gout patients with moderate-to-severe renal impairment,”Arthri- tis & Rheumatology, vol. 68, no. 8, pp. 2035–2043, 2016.
- Critical Appraisal Skills Programme, “Critical Appraisal SkillsProgramme (2018). CASP Ran- domised Controlled Trial Checklist,” 2018.
- Coxib and traditional NSAID Trial lists’ (CNT) Collaboration,N. Bhala, J. Emberson, A. Merhi et al., “Vascular and upper gastrointestinal effects of non-steroidal anti-inflammatory drugs:meta- analyses of individual participant data from randomized trials,” Lancet, vol. 382, pp. 769–779, 2013.
- C. M. T. Greenwood, J. P. Midgley, A. G. Matthew, and A.G. Logan, “Statistical issues in a meta-re- gression analysis ofrandomized trials: Impact on the dietary sodium intake andblood pressure relationship,” Biometrics, vol. 55, no. 2, pp. 630–636, 1999.
- I. Holme, A. H. Aastveit, N. Hammar, I. Jungner, and G.Walldius, “Uric acid and risk of myocardial infarction, strokeand congestive heart failure in 417 734 men and women in theApolipoprotein- MOrtalityRISk study (AMORIS),” Journal ofInternal Medicine, vol. 266, no. 6, pp. 558–570, 2009.
- H. Huang, B. Huang, Y. Li et al., “Uric acid and risk ofheart failure: a systematic review and meta- analysis,” EuropeanJournal of Heart Failure, vol. 16, no. 1, pp. 15–24, 2014.
- J. Wang, T. Qin, J. Chen et al., “Hyperuricemia and risk ofincident hypertension: a systematic re- view and meta-analysisof observational studies,” PLoS ONE, vol. 9, no. 12, Article IDe114259, 2014.
- D. I. Feig, D. H. Kang, and R. J. Johnson, “Medical progress:uric acid and cardiovascular risk,” The New England Journal ofMedicine, vol. 359, no. 17, pp. 1811–1821, 2008.
- M. M. Givertz, K. J. Anstrom, M. M. Redfeld et al., “Effectsof xanthine oxidase inhibition in hyper- uricemic heart failurepatients: The xanthine oxidase inhibition for hyperuricemicheart failure pa- tients (EXACT-HF) study,” Circulation, vol. 131,no. 20, pp. 1763–1771, 2015.
- H. R. Schumacher Jr., M. A. Becker, E. Lloyd, P. A. MacDonald,and C. Lademacher, “Febuxostat in the treatment of gout: 5-yearfindings of the FOCUS efficacy and safety study,”Rheumatology(Ox- ford), vol. 48, no. 2, pp. 188–194, 2009.
- C. Patrono and C. Baigent, “Nonsteroidal anti-inflammatory drugs and the heart,” Circulation,vol. 129, no. 8, pp. 907–916,2014.
- E. Krishnan, “Inflammation, oxidative stress and lipids: the risktriad for atherosclerosis in gout,” Rheumatology, vol. 49, no. 7,pp. 1229–1238, 2010.
- J. M. Zimmet and J. M. Hare, “Nitroso-redox interactions inthe cardiovascular system,” Circula- tion, vol. 114, no. 14, pp. 1531–1544, 2006.
- C. Gersch, S. P. Palii, K. M. Kim, A. Angerhofer, R. J. Johnson,and G. N. Henderson, “Inactivation of nitric oxide by uric acid,”Nucleosides, Nucleotides and Nucleic Acids, vol. 27, no. 8, pp.967–978, 2008.
- Y.-J. Choi, Y. Yoon, K.-Y. Lee et al., “Uric acid induces endothelial dysfunction by vascular insulin resistance associated withthe impairment of nitric oxide synthesis,” The FASEB Journal,vol. 28, no. 7, pp. 3197–3204, 2014.









Άφησε σχόλιο