Περίληψη
Η αποτυχία του συστήματος αγωγιμότητας της καρδιάς είναι μια από τις πιο κοινές καταστάσεις στην καρδιολογική πρακτική, καθιστώντας την Ηλεκτροφυσιολογία τον ταχύτερα αναπτυσσόμενο τομέα της Καρδιολογίας. Η θεραπεία των αρρυθμιών και η αποκατάσταση της φυσιολογικής καρδιακής δραστηριότητας έχει αυξήσει σημαντικά τη διάρκεια ζωής των ασθενών. Η πρόοδος της ιατρικής τεχνολογίας έχει φέρει επανάσταση στον καρδιακό ρυθμό με τη χρήση μικρότερων, πιο εξελιγμένων και πλήρως εμφυτεύσιμων συσκευών. Οι Εμφυτεύσιμες Καρδιολογικές Ηλεκτρονικές Συσκευές έχουν σχεδιαστεί για τη διάγνωση και τη θεραπεία ασθενών με ανεπάρκεια αγωγιμότητας σήματος και καρδιακή ανεπάρκεια. Αυτές οι συσκευές περιλαμβάνουν: α) Βηματοδότες, β) Εμφυτεύσιμους Απινιδωτές Καρδιομετατροπής (ICDs), γ) Συσκευές Θεραπείας Καρδιακού Επανασυγχρονισμού και δ) Εμφυτεύσιμους Καταγραφείς Βρόχου (ILR). Οι βηματοδότες χρησιμοποιούνται για τη θεραπεία της συμπτωματικής βραδυκαρδίας χωρίς αναστρέψιμες αιτίες, ενώ τα ICDs τερματίζουν τις επικίνδυνες και θανατηφόρες ταχυαρρυθμίες. Ασθενείς με σοβαρή καρδιακή ανεπάρκεια και κοιλιακή ασυγχρονία είναι υποψήφιοι για θεραπεία καρδιακού επανασυγχρονισμού με αμφικοιλιακή βηματοδότηση προκειμένου να αποκατασταθεί η φυσιολογική συστολική λειτουργία του καρδιακού μυός. Οι νεοεισαχθέντες ILR καταγράφουν τον καρδιακό ρυθμό με συνεχή ΗΚΓ καταγραφή έως και 14 ημέρες και παίζουν σημαντικό ρόλο στον εντοπισμό βραχυχρόνιων, συμπτωματικών αρρυθμιών ή ακόμα και στη διερεύνηση αιτιών επεισοδίων συγκοπής και κρυπτογενών εγκεφαλικών επεισοδίων. Αναμφίβολα, οι Εμφυτεύσιμες Συσκευές έχουν βελτιώσει την ποιότητα ζωής των ασθενών με προβλήματα αγωγιμότητας. Η περαιτέρω ερευνητική ανάπτυξη νέων, ακριβέστερων και πιο ανθεκτικών συσκευών θα αποτελέσει τον ακρογωνιαίο λίθο της θεραπείας των αρρυθμιών.
Implantable Heart Rate Management Devices
Abstract
Heart’s conduction system failure is one of the most common conditions in cardiology practice, making Electrophysiology the fastest growing field of Cardiology. Treatment of arrhythmias and restoration of normal cardiac activity has significantly increased the lifespan of patients. Advances in medical technology have revolutionized cardiac pacing with the use of smaller, more sophisticated and totally implantable devices. The Implantable Cardiac Electronic Devices are designed to diagnose and treat patients with signal conduction failure and heart failure. These devices include: a) Pacemakers, b) Implantable Cardioverter Defibrillators (ICDs), c) Cardiac Resynchronization Therapy devices and d) Implantable Loop Recorders (ILRs). Pacemakers are used to treat symptomatic bradycardias with no reversible causes, while ICDs terminate dangerous and lethal tachyarrhythmias. Patients with severe heart failure and ventricular asynchrony are candidates for cardiac resynchronization therapy with biventricular pacemakers in order to restore the normal systolic function of the cardiac muscle. The newly introduced ILRs record the heart rhythm with continuous ECGs up to 14 days and play an important role in identifying short-lasting, symptomatic arrhythmias or even to investigate causes of syncope episodes and cryptogenic strokes. Undoubtedly, Implantable Devices have improved the quality of life of patients with conduction problems. Further research development of new, more accurate and more resilient devices will be the cornerstone of arrhythmias treatment.
Εισαγωγή
Οι εμφυτεύσιμες καρδιακές ηλεκτρονικές συσκευές (Ε.Κ.Η.Σ.) σχεδιάσθηκαν και χρησιμοποιούνται στη διάγνωση και στη θεραπεία ασθενών με συγκεκριμένες διαταραχές του καρδιακού ρυθμού. Οι διαταραχές του ρυθμού αφορούν αρρώστους με προβλήματα στη φυσιολογική παραγωγή ή στην αγωγή του ηλεκτρικού ερεθίσματος, ασθενείς με ιστορικό καρδιακής ανεπάρκειας (ή άλλης οργανικής καρδιακής νόσου), ασθενείς με συγκεκριμένα συστηματικά νοσήματα ή με κάποια «διαυλοπάθεια» (δηλαδή κάποια ιδιαιτερότητα στη γένεση του ερεθίσματος) στους οποίους υπάρχει αυξημένος κίνδυνος πρόκλησης κακοήθους κοιλιακής ταχυαρρυθμίας. Στη συνέχεια θα αναφερθούμε αναλυτικά στους βηματοδότες, τους απινιδωτές, τους αμφικοιλιακούς βηματοδότες (με ή χωρίς απινιδωτή) αλλά και στους εμφυτεύσιμους καταγραφείς (Holters) μακράς διάρκειας (Εικόνα 1).

Βηματοδότες
Η εμφύτευση βηματοδότη αποτελεί ένα από τα σπουδαιότερα κεφάλαια της καρδιολογίας αλλά και της ηλεκτροφυσιολογίας ειδικότερα. Υπολογίζεται ότι κάθε χρόνο, ένα εκατομμύριο ασθενείς (το 80% των οποίων ξεπερνάει το 65οέτος της ηλικίας του) υποβάλλονται παγκοσμίως σε επέμβαση εμφύτευσης βηματοδότη1. Οι πρώτοι βηματοδότες εμφυτεύθηκαν σε ασθενείς με σημαντική βραδυκαρδία στα τέλη της δεκαετίας του 1960 και η μπαταρία τους είχε διάρκεια ζωής λίγων ωρών. Οι σύγχρονες συσκευές – με πολύ μικρότερο μέγεθος – διαρκούν περίπου 10-12 έτη πριν γίνει αναγκαία η αντικατάσταση της γεννήτριας.
Ο βηματοδότης είναι μία συσκευή η οποία δημιουργήθηκε με σκοπό την αντιμετώπιση συμπτωματικών επεισοδίων σοβαρής βραδυκαρδίας – οι οποίες δεν οφείλονται σε αντιστρεπτά αίτια. Τα συνηθέστερα αίτια είναι το σύνδρομο του νοσούντος φλεβοκόμβου2 (διαταραχή στην παραγωγή του ηλεκτρικού ερεθίσματος) και οι υψηλού βαθμού Κολποκοιλιακοί αποκλεισμοί3 (συνήθως 2ου και 3ου βαθμού, όπου το πρόβλημα αφορά στην αγωγή του ηλεκτρικού ερεθίσματος).
Τα βασικά τμήματα ενός βηματοδότη είναι :
α) η ηλεκτρική γεννήτρια που αποτελεί την πηγή ενέργειας και
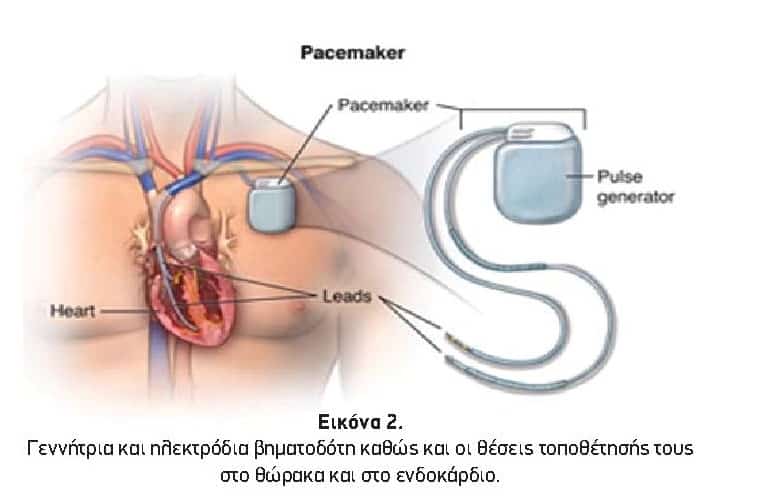
β) τα ηλεκτρόδια που ξεκινούν από τη γεννήτρια και καταλήγουν στο ενδοκάρδιο όπου και καθηλώνονται, με σκοπό τόσο την αίσθηση (ανίχνευση) της ενδογενούς καρδιακής δραστηριότητας όσο και την εκπόλωση (διέγερση) του καρδιακού μυός.
Επομένως, ο βηματοδότης πρέπει να διεγείρει το μυοκάρδιο όταν αυτό είναι απαραίτητο – εξίσου σημαντικό είναι να ανιχνεύει την αυτόχθονη ηλεκτρική δραστηριότητα (αν και όταν υπάρχει) και να αναστέλλει τη βηματοδότηση. Η καθήλωση των ηλεκτροδίων επιτυγχάνεται είτε παθητικά (η άκρη του καλωδίου φέρει προσεκβολές, που καθηλώνονται στις δοκίδες του ενδοκαρδίου) είτε ενεργητικά (στην άκρη του ηλεκτροδίου υπάρχει βίδα που καθηλώνεται ελικοειδώς). Το υλικό κατασκευής του είναι συνήθως τιτάνιο ή πλατίνα ενώ το εξωτερικό του περίβλημα (μονωτικό) είναι συνήθως σιλικόνη ή πολυουρεθάνη. Σημειώνεται, ότι τα υλικά κατασκευής είναι φιλικά προς το σώμα και ο ανθρώπινος οργανισμός δεν τα απορροφά μετά την εμφύτευση.
Οι μονοεστιακοί βηματοδότες φέρουν ένα ηλεκτρόδιο, το οποίο και καταλήγει στην κοιλότητα της δεξιάς κοιλίας. Οι διπλοεστιακοί βηματοδότες φέρουν δύο ηλεκτρόδια, ένα για το δεξιό κόλπο και ένα για τη δεξιά κοιλία. Η επιλογή του τύπου βηματοδότη που θα εμφυτευθεί εξαρτάται από τη νόσο και το ιστορικό του ασθενή· στη μεγάλη πλειοψηφία των ασθενών εμφυτεύεται διπλοεστιακός βηματοδότης. Τα τελευταία χρόνια, ιδιαίτερα σε ασθενείς με προβλήματα στην αγγειακή προσπέλαση, χρησιμοποιούνται βηματοδότες χωρίς ηλεκτρόδια (leadless)4.
Ο συνηθέστερος τρόπος εμφύτευσης ενός βηματοδότη είναι μέσω της διαφλέβιας οδού. Στο αιμοδυναμικό εργαστήριο, η επέμβαση ξεκινά με τη χορήγηση τοπικής αναισθησίας πάνω από την περιοχή στην οποία θα τοποθετηθεί η γεννήτρια- συνήθως στο άνω και έξω αριστερό ημιθωράκιο (Εικόνα 2). Κατά τη διάρκεια της επέμβασης ο ασθενής είναι ξύπνιος και έχει τη δυνατότητα επικοινωνίας με τους γιατρούς και το νοσηλευτικό προσωπικό. Ακολούθως, δημιουργείται η ειδική θήκη στο υποδόριο της περιοχής, μέσα στην οποία θα τοποθετηθεί η γεννήτρια. Στη συνέχεια, μέσω μιας φλέβας προωθούνται τα καλώδια (ή το καλώδιο) στην κατάλληλη θέση εντός των καρδιακών κοιλοτήτων. Αφού τοποθετηθούν τα ηλεκτρόδια, επιβεβαιώνεται η καταλληλότητα της θέσης με τη μέτρηση διαφόρων ηλεκτρικών παραμέτρων. Η γεννήτρια συνδέεται με το (ή τα) καλώδιο(α), τοποθετείται στη θήκη της και ακολουθεί η συρραφή του τραύματος. Η επέμβαση ολοκληρώνεται και την επόμενη ημέρα ο ασθενής επιστρέφει σπίτι του, με αναλυτικές οδηγίες.
Η περιοδικότητα παρακολούθησης της λειτουργίας του βηματοδότη καθορίζεται από το θεράποντα ιατρό. Συνήθως, οι ασθενείς ελέγχουν τη λειτουργία της συσκευής τους κάθε έξι μήνες. Στις ημέρες μας, αναπτύσσονται συστήματα ελέγχου των συσκευών από απόσταση. Σε κάθε επίσκεψη του αρρώστου προηγείται η κλινική εξέταση και το ιστορικό (κυρίως μας ενδιαφέρουν τα φάρμακα που λαμβάνονται και οι πιθανές μεταβολές σε σκευάσματα ή στη δοσολογία αυτών). Ακολουθεί ο αναίμακτος έλεγχος της λειτουργίας του βηματοδότη· στον ασθενή τοποθετείται η κεφαλή προγραμματιστή της συσκευής ελέγχου πάνω από την μπαταρία και ακολούθως στον προγραμματιστή λαμβάνονται όλες οι απαραίτητες πληροφορίες ενώ πληροφορούμαστε και για τη διάρκεια ζωής της γεννήτριας. Όταν η γεννήτρια πλησιάζει στα όρια της εξάντλησης της, τότε προγραμματίζεται η επέμβαση αντικατάστασης της. Με δεδομένο ότι τα καλώδια λειτουργούν καλά, αφαιρείται η παλαιά γεννήτρια και τοποθετείται στη θέση της η καινούρια μπαταρία.
Οι συνηθέστερες επιπλοκές μετά την επέμβαση είναι τοπικές (συνήθως μικρά αιματώματα). Οι πλέον σοβαρές αφορούν στην επιμόλυνση (πρώιμη ή όψιμη), την εξωτερίκευση της γεννήτριας5 κ.α. Όταν ένας βηματοδότης επιμολυνθεί, πρέπει να αφαιρεθεί όλο το σύστημα (καλώδια και γεννήτρια), να χορηγηθεί η κατάλληλη αντιβιοτική αγωγή και σε δεύτερο χρόνο να επανατοποθετηθεί η συσκευή στην αντίπλευρη θωρακική χώρα. Η κλινική εικόνα της επιμόλυνσης εκδηλώνεται συνήθως με την εμφάνιση σημείων φλεγμονής στην περιοχή της επέμβασης (πόνος, ερυθρότητα, οίδημα, εκροή πύου ή ακόμη και αποκάλυψη της γεννήτριας).
Απινιδωτές
Ο εμφυτεύσιμος-καρδιομετατροπέας απινιδωτής (Implantable Cardioverter Defibrillator- ICD) είναι μία συσκευή η οποία έχει τη δυνατότητα να τερματίζει απειλητικές κοιλιακές ταχυαρρυθμίες.
Ο απινιδωτής αποτελείται από δύο βασικά τμήματα, όπως και ο βηματοδότης:
- την ηλεκτρική γεννήτρια και
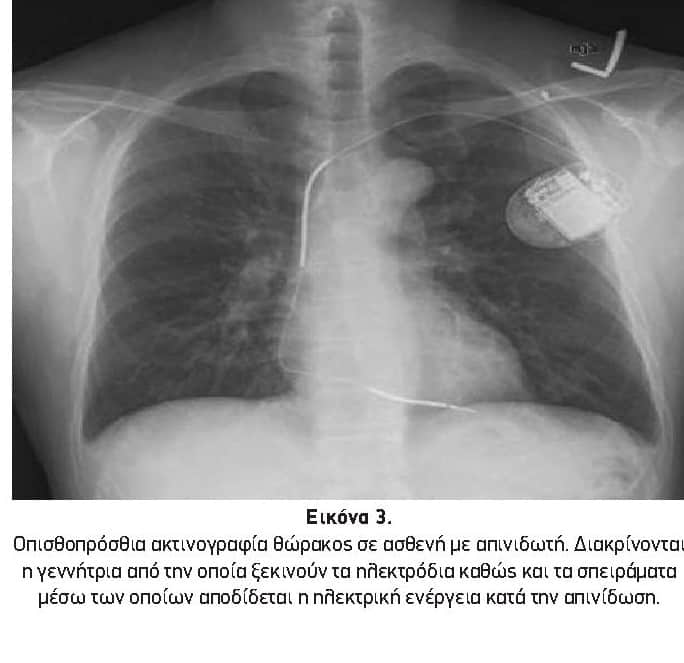
- τα καλώδια (Εικόνα 3).
Η γεννήτρια λαμβάνει τα ηλεκτρικά σήματα που προσλαμβάνει το ηλεκτρόδιο (ενδοκαρδιακό ηλεκτρόγραμμα) τα επεξεργάζεται και αφού ταυτοποιήσει την επικίνδυνη αρρυθμία, «αποφασίζει» για το είδος της θεραπείας που θα αποδώσει.
Οι θεραπείες του απινιδωτή διακρίνονται σε:
- Αντιταχυκαρδιακή βηματοδότηση (ΑΤΒ). Με βάση τη μορφολογία και -κυρίως- τη συχνότητα της ταχυκαρδίας, ο απινιδωτής βηματοδοτεί την καρδιά γρηγορότερα (με μικρότερο μήκος κύκλου από αυτό της ταχυαρρυθμίας)· ένας μηχανισμός που έχει αποδειχθεί εξαιρετικά αποτελεσματικός στην αντιμετώπιση πολλών ταχυκαρδιών
- Απινίδωση. Όταν η ταχυκαρδία έχει μεγάλη συχνότητα (είναι πολύ γρήγορη) ή σε περίπτωση που η ΑΤΒ αποτύχει, ο απινιδωτής προχωρά στην απόδοση ηλεκτρικής ενέργειας συγκεκριμένων joule – με τη μορφή σοκ. Οι μελέτες δείχνουν ότι περίπου το 75% των κακοήθων ταχυαρρυθμιών αντιμετωπίζονται επιτυχώς με ΑΤΒ.
Στο σημείο αυτό να υπογραμμίσουμε ότι:
α) Κάθε απινιδωτής έχει δυνατότητα καρδιακής διέγερσης – δηλ. βηματοδότησης
β) Οι παράμετροι λειτουργίας του απινιδωτή (το εύρος των συχνοτήτων που θα καθορίσει την επικινδυνότητα της ταχυκαρδίας, η μορφή της ΑΤΒ, ο αριθμός των αποδιδόμενων σοκ καθώς και η ποσότητα της ενέργειας που παρέχεται στο κάθε ένα από αυτά) καθορίζονται από το θεράποντα ιατρό μετά το τέλος της επέμβασης-εμφύτευσης και επανακαθορίζονται στην πορεία.
Ο πρώτος απινιδωτής εμφυτεύθηκε στις ΗΠΑ, στις αρχές της δεκαετίας του 1980 από το Δρ. Μαικλ Μιρόφσκι- ο οποίος ξεκίνησε να δουλεύει την ιδέα δημιουργίας μιας τέτοιας συσκευής, μετά το θάνατο ενός πολύ καλού φίλου (και δασκάλου του) από υποτροπιάζουσες κοιλιακές ταχυαρρυθμίες. Στις ημέρες μας, ένδειξη για τοποθέτηση απινιδωτή έχουν ασθενείς που υπάγονται σε 2 βασικές κατηγορίες νοσημάτων: α) άρρωστοι που κατά το παρελθόν είχαν επεισόδιο εξωνοσοκομειακής καρδιακής ανακοπής ή απειλητικής για τη ζωή κοιλιακής ταχυκαρδίας (δευτερογενής πρόληψη) και β) άρρωστοι που, παρόλο που δεν έχουν υποστεί κάποιο ανάλογο επεισόδιο, εμφανίζουν κάποια σοβαρή καρδιαγγειακή νόσο, στο έδαφος της οποίας μπορεί να εμφανισθούν επεισόδια επικίνδυνης ταχυαρρυθμίας (πρωτογενής πρόληψη)6. Με τον όρο σοβαρή καρδιαγγειακή νόσος αναφερόμαστε είτε σε κάποια δομική πάθηση του μυοκαρδίου (π.χ. παλαιό έμφραγμα, καρδιακή ανεπάρκεια κ.α.) είτε σε κάποια ομάδα γενετικά καθοριζόμενων διαταραχών του καρδιακού ρυθμού.
Όπως και στην περίπτωση των βηματοδοτών, ο συνηθέστερος τρόπος εμφύτευσης ενός απινιδωτή είναι μέσω της διαφλέβιας οδού. Τελευταία έχουν αναπτυχθεί τεχνικές όπου ο απινιδωτής ( σε συγκεκριμένες κατηγορίες ασθενών) εμφυτεύεται υποδόρια. Συνήθως, οι ασθενείς εκτιμούνται κάθε έξι μήνες- ενώ συνιστάται να επικοινωνούν με το γιατρό τους για περαιτέρω έλεγχο, σε περίπτωση απόδοσης σοκ (χτυπήματος) του απινιδωτή. Στον έλεγχο του απινιδωτή, εκτός από τις παραμέτρους ορθής λειτουργίας του (αίσθηση και δυνατότητα βηματοδότησης), καταγράφονται τα επεισόδια ταχυαρρυθμίας που έχουν συμβεί κατά το παρελθόν (μορφή, διάρκεια, θεραπεία που αποδόθηκε), γίνονται οι τυχόν απαραίτητες μετατροπές στις αποδιδόμενες θεραπείες ενώ πληροφορούμαστε και τη διάρκεια ζωής της γεννήτριας.
Οι σύγχρονοι απινιδωτές διαθέτουν πολύ αποτελεσματικά συστήματα προστασίας από τις διάφορες πηγές ηλεκτρομαγνητικών παρεμβολών (ΗΜΠ). Οι συνηθέστερες πηγές ΗΜΠ ανευρίσκονται κυρίως σε ενδονοσοκομειακό περιβάλλον -όπως η διαθερμία (ρεύμα) που χρησιμοποιείται κατά τη διάρκεια χειρουργικών πράξεων. Στις περιπτώσεις αυτές, προτιμάται η απενεργοποίηση όλων των θεραπευτικών πρωτοκόλλων, κατά τη διάρκεια του χειρουργείου. Παλαιότερα, οι ασθενείς με απινιδωτή δεν μπορούσαν να υποβληθούν σε μαγνητική τομογραφία- κάτι που στις ημέρες μας δεν ισχύει λόγω χρησιμοποίησης κατάλληλων συσκευών (MRI-compatible) Η χρήση των κινητών τηλεφώνων είναι ασφαλής. Οι φούρνοι μικροκυμάτων, οι ανιχνευτές μετάλλων και τα οικιακά συστήματα προστασίας δε φαίνεται να προκαλούν ιδιαίτερα προβλήματα. Οι ασθενείς που φέρουν απινιδωτή απαγορεύεται να οδηγούν επαγγελματικά. Για όσους φέρουν απινιδωτή στο πλαίσιο πρωτογενούς πρόληψης, συνιστάται η αποχή από την οδήγηση για δέκα ημέρες περίπου. Σε περίπτωση κοιλιακής ταχυαρρυθμίας που αντιμετωπίσθηκε με σοκ, ο ασθενής επαναξιολογείται και η οδήγηση απαγορεύεται για το επόμενο 6μηνο τουλάχιστον.
Συσκευές Καρδιακού Επανασυγχρονισμού (CRT)
Στο φυσιολογικό μυοκάρδιο, οι δύο κοιλίες (Αριστερή και Δεξιά) – καθώς και τα διαφορετικά τμήματα της Αρ. κοιλίας – συστέλλονται συγχρονισμένα. Σε ασθενείς με καρδιακή ανεπάρκεια σοβαρού βαθμού (σοβαρά επηρεασμένο κλάσμα εξώθησης της Αρ. κοιλίας, διαταραχές της ενδοκοιλιακής αγωγής στο ηλεκτροκαρδιογράφημα) διαταράσσεται ο συγχρονισμός στη συστολή των κοιλιών. Η αποκατάσταση του συγχρονισμού στην κοιλιακή συστολή επιτυγχάνεται με τις συσκευές καρδιακού επανασυγχρονισμού (CRTs), οι οποίες σε συνδυασμό με την κατάλληλη φαρμακευτική αγωγή έχουν ως αποτέλεσμα τόσο τη συμπτωματική βελτίωση όσο και την παράταση της επιβίωσης των αρρώστων μας7.
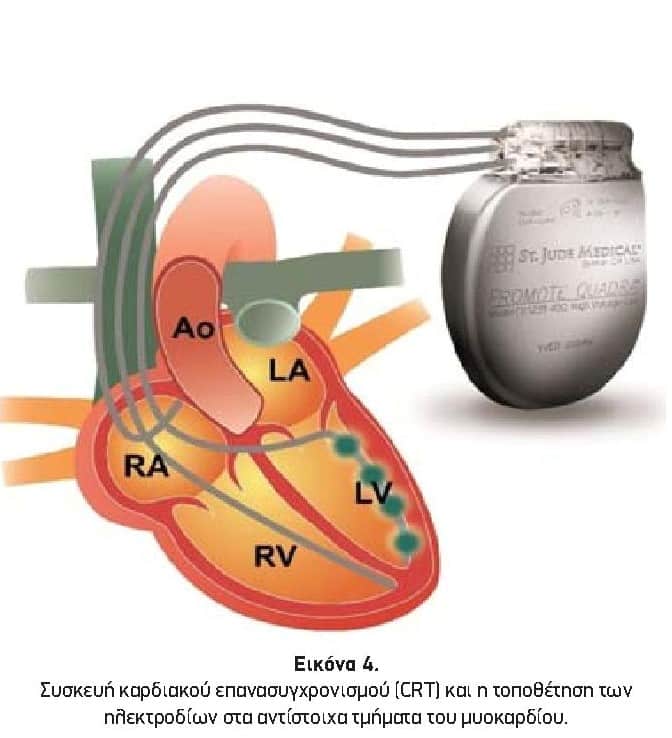
Οι CRTs έχουν ηλεκτρική γεννήτρια από την οποία ξεκινάνε τρία ηλεκτρόδια. Εκτός από τα ηλεκτρόδια του Δεξιού κόλπου και της Δεξιάς κοιλίας, το τρίτο ηλεκτρόδιο τοποθετείται στο επικάρδιο (εξωτερικό τμήμα) της Αριστερής κοιλίας, δια μέσω του φλεβικού δικτύου του Στεφανιαίου κόλπου (το βασικό φλεβικό σύστημα του μυοκαρδίου). Οι αισθητήρες (δίπολα) του ηλεκτροδίου τοποθετούνται στο κατάλληλο σημείο έτσι ώστε μέσω της ενδοκαρδιακής βηματοδότησης (από τη Δεξιά κοιλία) και της επικαρδιακής βηματοδότησης (από την Αριστερή κοιλία) να επιτυγχάνεται ο καλύτερος συγχρονισμός και να βελτιστοποιείται η καρδιακή απόδοση (Εικόνα 4).
Υπάρχουν δύο είδη συσκευών CRTs :
- Οι CRT-P για την αμφικοιλιακή βηματοδότηση και
- Οι CRT-D, για τους ασθενείς αυξημένου αρρυθμικού κινδύνου, οι οποίοι φέρουν και απινιδωτή8.
Πρέπει να τονίσουμε ότι ενώ στους συμβατικούς βηματοδότες, η λειτουργία βηματοδότησης προγραμματίζεται κατʼ επίκληση (όταν αυτό είναι απαραίτητο), στις συσκευές καρδιακού επανασυγχρονισμού το ποσοστό αμφικοιλιακής βηματοδότησης πρέπει να είναι το μεγαλύτερο δυνατό – κοντά στο 100% – ώστε οι ασθενείς να εισπράττουν το μέγιστο όφελος.
Εμφυτεύσιμοι Καταγραφείς Ρυθμού (ILR)
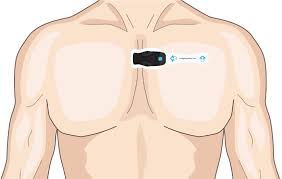
Η πολύωρη καταγραφή του καρδιακού ρυθμού γίνεται παραδοσιακά με τις γνωστές συσκευές (Holters), συνήθως 24ώρης ή και 48ώρης διάρκειας. Τα τελευταία χρόνια έχουν αναπτυχθεί συσκευές μακρόχρονης παρακολούθησης του ρυθμού (με καταγραφή έως και 14 ημερών)- είναι αυτοκόλλητες , χωρίς καλώδια και κερδίζουν συνεχώς έδαφος (ευκολία στην τοποθέτηση, ακρίβεια στην καταγραφή). Η μετάδοση των πληροφοριών γίνεται μέσω κινητών τηλεφώνων (smartphones) ενώ στα πιο εξελιγμένα μοντέλα δεν απαιτείται η χρήση κινητού καθώς η ενσωματωμένη μνήμη (και μπαταρία) που διαθέτουν επιτρέπει την αδιάλειπτη καταγραφή του ΗΚΓ και για τις 14 ημέρες καθιστώντας το πιο προσιτό και εύχρηστο ακόμη και για όσους δεν είναι εξοικειωμένοι με την τεχνολογία. Ασθενείς με συμπτωματολογία που εμφανίζεται σπανιότερα και περιοδικά (συνήθως για μικρό χρονικό διάστημα), άρρωστοι με ανεξήγητα εγκεφαλικά επεισόδια (στους οποίους υπάρχει το ερωτηματικό πιθανών παροξυσμών υποκλινικής κολπικής μαρμαρυγής) ή ασθενείς με υποτροπιάζονται επεισόδια ανεξήγητης συγκοπής έχουν ένδειξη τοποθέτησης εμφυτεύσιμων συσκευών ILR. Πρόκειται για πολύ μικρές συσκευές (Εικόνα 5), που τοποθετούνται υποδόρια (σε συνθήκες μικρού χειρουργείου) και καταγράφουν τον καρδιακό ρυθμό των ασθενών για χρονικό διάστημα 36 έως και 48 μηνών. Μετά την επέμβαση, ο κάθε ασθενής παραλαμβάνει μία συσκευή τηλεμετρίας (η οποία συνήθως συνδέεται με το τηλέφωνο) και τα δεδομένα από την καταγραφή του ρυθμού του μεταδίδονται αυτόματα στη βάση δεδομένων των θεραπόντων ιατρών. Ο έλεγχος των καταγραφών της συσκευής (με βάση τον προγραμματισμό) οδηγεί, σχεδόν πάντοτε, στην αποκάλυψη και την ορθή διάγνωση της ένοχης αρρυθμίας.

Συμπεράσματα
Οι Ε.Κ.Η.Σ. αποτελούν μια πραγματικότητα που έχει βελτιώσει τη ζωή – τόσο τη συμπτωματολογία όσο και το προσδόκιμο – εκατομμυρίων ασθενών ανά τον κόσμο. Η εμφύτευση αλλά και η διαχείριση- παρακολούθηση των ασθενών που φέρουν αυτές τις συσκευές πρέπει να γίνεται σε ειδικά κέντρα, από εξειδικευμένους ιατρούς με εμπειρία και γνώση του αντικειμένου. Με σύμμαχο την έρευνα και την τεχνολογία, στοχεύουμε στη δημιουργία ακόμα καλύτερων συσκευών, μικρότερων σε μέγεθος, περισσότερο έξυπνων και ανθεκτικών για να απλοποιήσουμε όσο γίνεται τη ζωή των ασθενών μας.
ΒΙΒΛΙΟΓΡΑΦΙΑ
- Mond HG, Proclemer A. The 11th world survey of cardiac pacing and implantable cardioverter-defibrillators: calendar year 2009—a World Society of Arrhythmia’s project. Pacing Clin Electrophysiol 2011; 34: 10131027.
- Sutton R, Kenny RA. The natural history of sick sinus syndrome. Pacing Clin Electrophysiol 1986; 9: 11101114.
- Edhag O, Swahn A. Prognosis of patients with complete heart block or arrhythmic syncope who were not treated with artificial pacemakers. A long-term follow-up study of 101 patients. Acta Med Scand 1976; 200: 457463.
- Burri H, Starck C, Auricchio A, et al. EHRA expert consensus statement and practical guide on optimal implantation technique for conventional pacemakers and implantable cardioverter-defibrillators: endorsed by the Heart Rhythm Society (HRS), the Asia Pacific Heart Rhythm Society (APHRS), and the Latin-American HeartRhythm Society (LAHRS). Europace 2021; 23: 983-1008. doi: 10.1093/europace/euaa367.
- Poole JE, Gleva MJ, Mela T, et al. REPLACE Registry Investigators. Complication rates associated with pacemaker or implantable cardioverter-defibrillator generator replacements and upgrade procedures: results from the REPLACE registry. Circulation 2010; 122: 15531561.
- Smith T, Jordaens L, Theuns DA, et al. The cost-effectiveness of primary prophylactic implantable defibrillator therapy in patients with ischaemic or non-ischaemic heart disease: a European analysis. Eur Heart J.2013; 34: 211–219.
- Leclercq C, Hare JM. Ventricular resynchronization: current state of the art. Circulation 2004; 109: 296299.
- Goldenberg I, Gillespie J, Moss AJ, et al. Executive Committee of the Multicenter Automatic Defibrillator Implantation Trial II. Long-term benefit of primary prevention with an implantable cardioverter-defibrillator: an extended 8-year follow-up study of the Multicenter Automatic Defibrillator Implantation Trial II. Circulation 2010; 122: 1265–1271.
CMJ 2022; 3: 138-144