Maria Pina Dore1, Giovanni Mario Pes1, Gabrio Bassotti2 and Paolo Usai-Satta3
1Dipartimento di Medicina Clinica e Sperimentale, Clinica Medica, University of Sassari, Viale San Pietro, No. 8, 07100 Sassari, Italy, 2 Dipartimento di Medicina, Sezione di Gastroenterologia, University of Perugia, Piazza Lucio Severi 1, San Sisto, 06132 Perugia, Italy, 3 Gastrointestinal Unit, P. Brotzu Hospital, 09124 Cagliari, Italy
Η δυσπεψία ορίζεται ως συμπτώματα που σχετίζονται με την ανώτερη γαστρεντερική οδό. Περίπου το 25% του Δυτικού πληθυσμού παραπονιούνται για συμπτώματα δυσπεψίας κάθε χρόνο. Το 70% από αυτούς δεν έχουν οργανική αιτία και τα συμπτώματα σχετίζονται με τη λεγόμενη λειτουργική δυσπεψία, η οποία χαρακτηρίζεται από επιγαστρικό άλγος, αίσθημα πρώιμου κορεσμού και/ή πληρότητας κατά τη διάρκεια ή μετά από ένα γεύμα και τα οποία συμβαίνουν τουλάχιστον σε εβδομαδιαία βάση και για τουλάχιστον 6 μήνες, σύμφωνα με τα κριτήρια ROME III. Προκειμένου να αποφευχθούν επεμβατικές διαδικασίες και ανεπιθύμητες ενέργειες, να ελαχιστοποιηθεί το κόστος, να επιταχυνθεί η διάγνωση και για την παροχή των πιο κατάλληλων θεραπειών, οι ιατροί της πρωτοβάθμιας περίθαλψης πρέπει να αναγνωρίζουμε την λειτουργική δυσπεψία. Επειδή τα συμπτώματα δεν είναι αξιόπιστα ούτως ώστε να γίνεται η διάκριση μεταξύ της οργανικής και λειτουργικής μορφής της νόσου, το οικογενειακό ιστορικό πεπτικού έλκους ή/και καρκίνου του στομάχου, ιστορικό φαρμακευτικής αγωγής, ειδικά για τα μη στεροειδή αντιφλεγμονώδη φάρμακα, ηλικία και φυσική εξέταση θα μπορούσαν να βοηθήσουν τον ιατρό ώστε να κάνει τη διάκριση μεταξύ της λειτουργικής δυσπεψίας και άλλων οργανικών αιτιών. Για τους ασθενείς χωρίς συμπτώματα συναγερμού η μη επεμβατική εξέταση για H. pylori, είτε με άνθρακα -13- γνωστή ως δοκιμή αναπνοής ουρίας ή η δοκιμή αντιγόνων κοπράνων συνιστάται ως στρατηγική πρώτης γραμμής. Στην παρούσα ανασκόπηση θα προβούμε σε συστάσεις για την καθοδήγηση των ιατρών πρωτοβάθμιας περίθαλψης για την κατάλληλη χρήση των διαγνωστικών εξετάσεων και για την αντιμετώπιση της λοίμωξης με H. pylori σε ασθενείς με δυσπεψία.
1. Εισαγωγή
Η δυσπεψία ορίζεται ως συμπτώματα που σχετίζονται με την ανώτερη γαστρεντερική οδό. Με περίπου 25% του Δυτικού πληθυσμού με δυσπεψία κάθε χρόνο, η δυσπεψία είναι μία από τις πιο κοινές αιτίες για την επίσκεψη σε ιατρό για γαστρεντερικά ενοχλήματα1,2. Τα συμπτώματα δυσπεψίας έχουν χωριστεί σε 3 κατηγορίες: δυσπεψία ομοιάζουσα με έλκος – στην οποία το κυρίαρχο σύμπτωμα είναι το άλγος που επικεντρώνεται στην άνω κοιλιακή χώρα (η πιο ενοχλητική), δυσπεψία ομοιάζουσα δυσκινησία – μια δυσάρεστη ή ενοχλητική δυσφορία εντοπιζόμενη στην άνω κοιλιακή χώρα και η οποία συνδέεται με αίσθημα πληρότητας και κορεσμού, μετεωρισμό και ναυτία και η μη καθορισμένη (μη ειδική) δυσπεψία η οποία ορίζεται ως η παρουσία των συμπτωμάτων που δεν πληρούν τα κριτήρια για ομοιάζουσα με έλκος δυσπεψία ή δυσπεψία ομοιάζουσα με δυσκινησία3. Οι πιο πρόσφατες ορισμός των κριτηρίων ROME ΙΙΙ αποκλείει τους ασθενείς με αναφερόμενο αίσθημα καύσου και περιλαμβάνουν τη διάρκεια των συμπτωμάτων για 6 μήνες πριν από τη διάγνωση και τη δυσπεψία ως ενεργό πρόβλημα για τους τελευταίους 3 μήνες1.
Η δυσπεψία δεν είναι ασθένεια αλλά μάλλον ένας συνδυασμός συμπτωμάτων που σχετίζονται με ένα ευρύ φάσμα ασθενειών. Στις περισσότερες περιπτώσεις δεν διαγιγνώσκεται κάποια οργανική πάθηση και το πρόβλημα θεωρείται ως λειτουργικό ή ιδιοπαθές. Τα πιο κοινά συμπτώματα σε ασθενείς με λειτουργική δυσπεψία είναι (i) αίσθημα πρώιμου κορεσμού (αδυναμία ολοκλήρωσης ενός κανονικού μεγέθους γεύματος), (ii) επιγαστρικό άλγος ή αίσθημα καύσους (χαρακτηριζόμενο ως σύνδρομο επιγαστρικού άλγους) και (iii) τη μεταγευματική πληρότητα (πρώιμος κορεσμός ο οποίος ταξινομείται ως σύνδρομο μεταγευματικής δυσφορίας)1. Ωστόσο, επειδή η δυσπεψία είναι ένα κοινό σύμπτωμα σοβαρών παθήσεων όπως το πεπτικό έλκος και ο καρκίνος του στομάχου είναι σημαντικό οι κλινικοί ιατροί να είναι σε θέση να αναγνωρίζουν τους ασθενείς με δυσπεψία σε σχέση με τον κίνδυνο των συμπτωμάτων που σχετίζονται με μια πιο σοβαρή κατάσταση. Αυτό απαιτεί μια λογική προσέγγιση στη διάγνωση και την αντιμετώπιση. Μέχρι την ολοκλήρωση της διαγνωστικής αξιολόγησης όλοι οι ασθενείς χαρακτηρίζονται ως έχοντες αδιερεύνητη δυσπεψία.
2. Αξιολόγηση της Αδιερεύνητης Δυσπεψίας
Κλασικά, η αξιολόγηση αρχίζει με τη λήψη του ιστορικού και τη φυσική εξέταση ούτως ώστε να πραγματοποιηθεί ο διαχωρισμός οργανικών και λειτουργικών αιτιών. Εδώ, αναζητείται η παρουσία των συμπτωμάτων και ευρημάτων ενδεικτικών οργανικής νόσου (π.χ., τα λεγόμενα συμπτώματα συναγερμού ή χαρακτηριστικάτης νόσου)2.
Τα συμπτώματα συναγερμού που προτρέπουν σε ενδοσκόπηση για την αξιολόγηση των ασθενών με δυσπεψία έχουν ως εξής:
- Έκδηλη γαστρεντερική αιμορραγία
- Αναιμία
- Ανεξήγητη απώλεια βάρους
- Προοδευτική δυσφαγία
- Οδυνοφαγία
- Συχνοί έμετοι
- Οικογενειακό ιστορικό γαστεντερικού καρκίνου
- Παρουσία κοιλιακής μάζας ή/και λεμφαδενοπάθεια
Συνολικά, τα περισσότερα συμπτώματα συναγερμού έχουν χαμηλή προγνωστική αξία για την παρουσία οργανικής νόσου4,5. Ωστόσο, η παρουσία τους παραπέμπει προς την έγκαιρη χρήση των πιο επεμβατικών διαγνωστικών χειρισμών, όπως η ενδοσκόπηση του ανώτερου γαστρεντερικού, ενώ η απουσία των συμπτωμάτων συναγερμού σε ένα νεαρό και κατά τα άλλα υγιές άτομο παραπέμπει προς μια αρχική δοκιμή ιατρικής θεραπείας. Η διάγνωση καρκίνου του στομάχου είναι πολύ πιθανή σε περιοχές με υψηλή συχνότητα εμφάνισης καρκίνου του στομάχου όπως η Ιαπωνία ή η Κορέα και η ηλικία των 45 ετών είναι το όριο. Όταν αποκλείεται ο γαστρικός καρκίνος συνιστάται η ενδοσκόπηση του ανώτερου γαστρεντερικού συνιστάται σε ασθενείς άνω των 55 ετών2,3,6,7. Μεταξύ των ασθενών με δυσπεψία, μόνο το 25% έχουν ορισμένη οργανική αιτία8 ενώ στο υπόλοιπο των ασθενών, η διάγνωση της λειτουργικής δυσπεψίας μπορεί να γίνει σύμφωνα με τα κριτήρια ROME III1.
3. Λοίμωξη με Helicobacter pylori και Δυσπεψία
Αν και η λοίμωξη με H. pylori σχετίζεται με ασθένειες που συνήθως εμφανίζονται με δυσπεψία (π.χ., πεπτικό έλκος και γαστρικός καρκίνος), η ίδια η λοίμωξη μπορεί να προκαλέσει δυσπεψία χωρίς μεγάλες εμφανείς δομικές αλλαγές. Η λοίμωξη με H. pylori προκαλεί προοδευτικά λειτουργική και δομική γαστροδωδεκαδακτυλική βλάβη η οποία μπορεί απρόβλεπτα να εξελιχθεί σε πεπτικό έλκος και στις επιπλοκές του, όπως ατροφική γαστρίτιδα ή γαστρικό καρκίνο.
Τα κλινικά αποτελέσματα που σχετίζονται με λοίμωξη από Helicobacter pylori είναι τα εξής:
- Ενεργός χρόνια γαστρίτιδα:
- Μειωμένη παραγωγή οξέων
- Μειωμένη απορρόφηση φαρμάκου
- Ατροφική γαστρίτιδα
- Μειωμένη απορρόφηση βιταμίνης Β12
- Μετάδοση της λοίμωξης σε άλλους, ιδίως στην οικογένεια.
- Δυσπεψία (μη-έλκος)
- Σιδηροπενική αναιμία
- Αυτοάνοση θρομβοπενία
- Πεπτικό έλκος:
- Επιπλοκές πεπτικού έλκους
- MALT λέμφωμα
- Γαστρικό αδενοκαρκίνωμα
Περίπου το 20% των ατόμων με λοίμωξη από H. pylori θα βιώσουν μια κλινική νόσο ομοιάζουσα με λοίμωξη που σχετίζεται με H.pylori6. Οι τυχαιοποιημένες ελεγχόμενες δοκιμές της θεραπείας εκρίζωσης του ελικοβακτηριδίου του πυλωρού συγκριτικά με την έκθεση σε εικονικό φάρμακο αναφέρουν ότι μόνο σε ένα ποσοστό (10 έως 12%) των ασθενών με λειτουργική δυσπεψία θα επιτευχθεί σημαντική βελτίωση των επίμονων συμπτωμάτων μετά την εκρίζωση του H. pylori2,8-12. Η ανακούφιση από τα συμπτώματα μπορεί επίσης να χρειαστεί από αρκετούς μήνες μέχρι ένα έτος.
Μια πρόσφατη τυχαιοποιημένη κλινική δοκιμή η οποία διεξήχθη σε ασθενείς πρωτοβάθμιας περίθαλψης με συμπτώματα δυσπεψίας ανέφερε ότι το 49% (94 από 192) βελτιώθηκαν σε σύγκριση με 36,5% (72 από 197) στην ομάδα ελέγχου (???? = 0,01. Αριθμός που απαιτείται για τη θεραπεία = 8). Παρόμοια αποτελέσματα έχουν παρατηρηθεί σε Ασιάτες ασθενείς με δυσπεψία13,14. Ένας πληθυσμός ασθενών με λοίμωξη με ελικοβακτηρίδιο του πυλωρού και δυσπεψία παρακολουθήθηκε για 7 χρόνια μετά την εκρίζωση του ελικοβακτηριδίου του πυλωρού και έδειξε μια μείωση κατά 25% στις αναζήτηση ιατρικών συμβουλών για συμπτώματα δυσπεψίας15. Επειδή η εκρίζωση του ελικοβακτηριδίου του πυλωρού θα εξαλείψει τη δυσπεψία μόνο σε ένα τμήμα των ασθενών με λοίμωξη, είναι επίσης σημαντικό να γνωρίζουμε τι πρέπει να λεχθεί στους ασθενείς σχετικά με τις βραχυπρόθεσμες και μακροπρόθεσμες προσδοκίες της εκρίζωσης του H. pylori. Γενικά, οι ασθενείς μπορούν να είναι σίγουροι ότι η θεραπεία της λοίμωξης από H. pylori θα οδηγήσει στη θεραπεία της γαστρίτιδας και ανάλογα με την αναστρεψιμότητα των βλαβών που έχουν προκληθεί στην επαναφορά της φυσιολογικής λειτουργίας. Ο κίνδυνος για πεπτικά έλκη από λοίμωξη με H. pylori εξαλείφεται και αν τα έλκη είναι παρόντα, θα ιαθούν. Ο κίνδυνος καρκίνου του στομάχου είναι επίσης μειωμένος και οι ασθενείς δεν μεταδίδουν πλέον τη νόσο σε άλλα μέλη της οικογένειας6. Είναι σημαντικό ότι η επίδραση στην ανακούφιση της δυσπεψίας είναι λιγότερο εξασφαλισμένη1,2. Επομένως, είναι σημαντικό για την αξιολόγηση της δυσπεψίας ο εντοπισμός των ασθενών και πότε θα πρέπει να πραγματοποιηθούν σε αυτούς οι διαγνωστικές δοκιμασίες για H. pylori και ποιές είναι οι κατάλληλες εξετάσεις. Επειδή δεν είναι προς το παρόν δυνατό να προσδιορισθεί ποιος ασθενής είναι σε κίνδυνο για κακή έκβαση, έχει προταθεί ότι όλοι οι ασθενείς με λοίμωξη με ελικοβακτηριδίου του πυλωρού θα πρέπει να λαμβάνουν θεραπεία εκρίζωσης του ελικοβακτηριδίου του πυλωρού7.
4. Προσέγγιση των Ασθενών με Συμπτώματα Συναγερμού
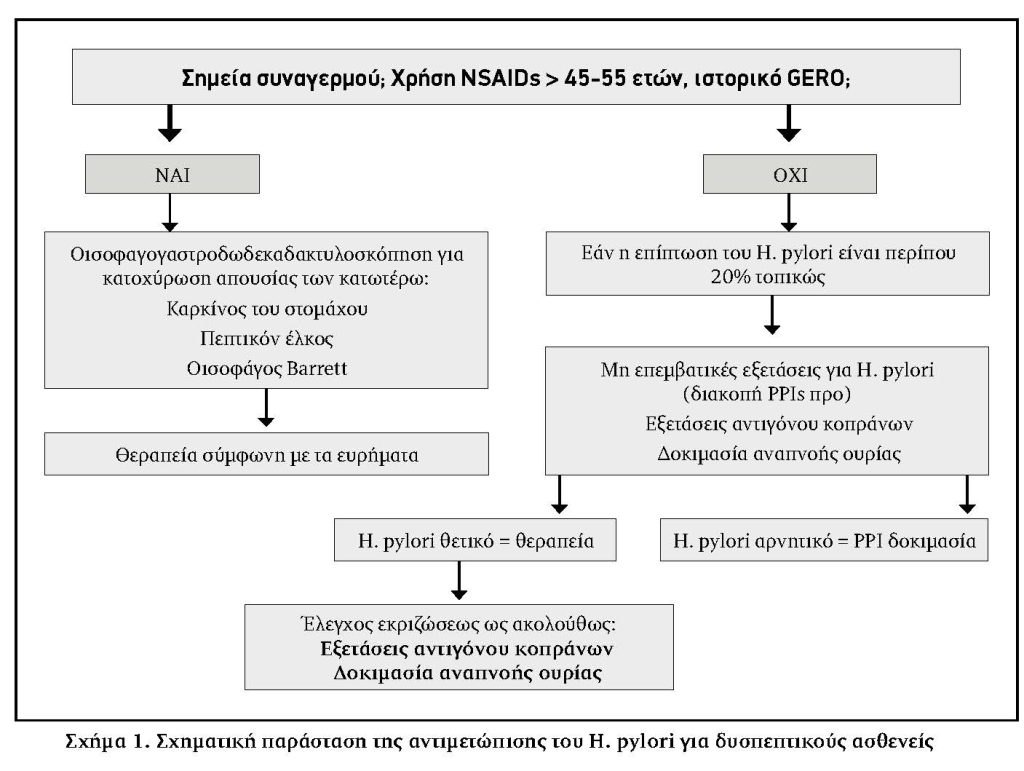
Για τους ασθενείς με συμπτώματα συναγερμού συνιστάται μια πρώιμη οισοφαγο-γαστροδωδεκαδακτυλική ενδοσκόπηση (Σχήμα 1). Για εκείνους που δεν έχουν συμπτώματα συναγερμού, το ερώτημα είναι εάν χρειάζεται μια δοκιμή της εμπειρικής θεραπεία με αναστολείς της αντλίας πρωτονίων (PPI) ή περαιτέρω διαγνωστικές εξετάσεις. Σε περιοχές όπου η λοίμωξη με H. pylori είναι συχνή (π.χ., ≥20%), οι εξετάσεις για λοίμωξη με το ελικοβακτηρίδιο του πυλωρού και η θεραπεία των μολυσμένων ατόμων προτιμώνται έναντι της θεραπείας με αναστολείς της αντλίας πρωτονίων. Σε αυτές τις περιοχές, η στρατηγική των εξετάσεων και η θεραπεία της λοίμωξης με H. pylori έχει αποδειχθεί οικονομικώς αποδοτική και μειώνει τον αριθμό των ενδοσκοπήσεων. Ωστόσο, ο έλεγχος για λοίμωξη με H. pylori ως στρατηγική πρώτης γραμμής είναι λογική, ακόμη και σε περιοχές με χαμηλό επιπολασμό της μόλυνσης, δεδομένου ότι οι διαθέσιμες εξετάσεις δεν είναι επεμβατικές. Μελέτες σχετικά με το οικονομικό σχεδιασμό και τη βελτίωση των συμπτωμάτων υποδηλώνουν ότι η θεραπεία εκρίζωσης είναι μια οικονομικά αποδοτική στρατηγική για τη διαχείριση της λειτουργικής δυσπεψίας και περισσότερα δεδομένα έδειξαν ότι η θεραπεία είναι ιδιαίτερα αποτελεσματική για τους ασθενείς με συμπτώματα ομοιάζοντα με πεπτικό έλκος1,2,16.
Σε εκείνους στους οποίους η δυσπεψία παραμένει παρά την εκρίζωση του ελικοβακτηριδίου του πυλωρού, η θεραπεία με PPI είναι ένα λογικό επόμενο βήμα. Αν τα συμπτώματα επιμένουν, θεραπεία με έναν προκινητικό παράγοντα, αντικαταθλιπτικά φάρμακα ή κάποια μορφή εναλλακτικών φαρμάκων, θα μπορούσε να εξεταστεί, αν και τα στοιχεία από προοπτικές μελέτες τα οποία να υποστηρίζουν αυτή την προσέγγιση είναι περιορισμένα17.
5. Διαγνωστικές Εξετάσεις για την Λοίμωξη με H. pylori
Η λοίμωξη με H. pylori σχετίζεται με έναν αριθμό ασθενειών (βλέπε τον κατάλογο των κλινικών αποτελεσμάτων που σχετίζονται με λοίμωξη από H.pylori). Υπάρχουν πολλές εξαιρετικές δοκιμές που διατίθενται σήμερα για τον εντοπισμό της ενεργούς λοίμωξης με H. pylori και είναι οι εξής:
- Μη επεμβατικές δοκιμές οι οποίες περιλαμβάνουν τα ακόλουθα:
- Ορολογικές:
- Ορολογικές IgG στο αίμα
- Δοκιμασία σιέλου
- Δοκιμασία IgG ούρων
- Έλεγχος ουρίας αναπνοής (UBT):
- Έλεγχος 13C-ουρίας αναπνοής
- Έλεγχος 14C-ουρίας αναπνοής
- Εξετάσεις ουρίας αίματος:
- Έλεγχος 13C-ουρίας αίματος
- Εξετάσεις για αντιγόνο κοπράνων:
- Πολυκλωνική εξέταση αντιγόνου κοπράνων
- Μονοκλωνική εξέταση αντιγόνου κοπράνων
- Ταχείες δοκιμές αντιγόνου κοπράνων
- Ορολογικές:
- Επεμβατικές εξετάσεις που απαιτούν ενδοσκόπηση περιλαμβάνουν τα ακόλουθα:
- Βιοψία ελέγχου ουρεάσης (ταχεία δοκιμασία ουρεάσης)
- Ιστολογία:
- Ανοσοχρώση
- Φθορισμός υβριδισμού in situ (FISH)
- Μοριακός έλεγχος ευαισθησίας
- Μοριακές εξετάσεις για λοιμώδεις παράγοντες (VacA-CagA)
- Κυτταρολογία τριβής
- Βακτηριακή καλλιέργεια:
- Δοκιμασία ευαισθησίας
Η επιλογή των εξετάσεων εξαρτάται από το κλινικό περιβάλλον, την τοπική διαθεσιμότητα και το κόστος και τη χρήση φαρμάκων (π.χ., χρήση αναστολέων αντλίας πρωτονίων, βισμούθιο ή αντιβιοτικά) που μειώνουν την πυκνότητα του ελικοβακτηριδίου του πυλωρού και ως εκ τούτου μειώνουν την ακρίβεια των εξετάσεων για την ενεργό λοίμωξη. Η παρουσία τέτοιων παραγόντων δεν αποτελεί απόλυτη αντένδειξη για τις εξετάσεις καθώς οι εξετάσεις μπορούν γενικά να καθυστερήσουν για το διάστημα κατά το οποίο τα φάρμακα θα έχουν διακοπεί. Η επιλογή μιας εξέτασης επηρεάζεται επίσης από την προβλεπόμενη πιθανότητα της μόλυνσης17.
5.1. Μη Επεμβατικές Εξετάσεις
5.1.1. Ορολογικές εξετάσεις. Οι λοιμώξεις με H. pylori σχετίζονται με μία ισχυρή χημική ανοσολογική αντίδραση και η παρουσία IgG αντισωμάτων ορού έναντι του H. pylori έχει αποδειχθεί ότι παρέχει μια αξιόπιστη εκτίμηση της τρέχουσας ή προηγούμενης μόλυνσης.
Ωστόσο, η παρουσία των αντισωμάτων μπορεί να παραμείνει για μεγάλο χρονικό διάστημα μετά τη μόλυνση. Έτσι, μια θετική ορολογική εξέταση σε έναν ασθενή δεν πρέπει να συνεπάγεται αυτομάτως την παρουσία ενεργούς λοίμωξης. Οι περισσότερες κοινές ορολογικές εξετάσεις βασίζονται σε τεχνολογικά ενζυμικά συνδεδεμένη – ανοσορροφητική δοκιμασία (ELISA). Μια μετα-ανάλυση 21 μελετών με εμπορικώς διαθέσιμη εξέταση ELISA έδειξε συνολική ευαισθησία και ειδικότητα 85% και 79%, αντίστοιχα18. Πρόσφατα, αρκετές δοκιμασίες αξιολογήθηκαν στην Ευρώπη και ένας αριθμός έδειξε υψηλή ευαισθησία19. Σαν γενικό κανόνα, πρέπει κανείς να χρησιμοποιήσει μόνο ό, τι έχει επικυρωθεί σε τοπικό ή περιφερειακό επίπεδο. Αν και οι εξετάσεις IgG, IgM, IgA είναι διαθέσιμες στο εμπόριο, μόνο οι IgG δοκιμασίες συνιστώνται καθώς οι άλλες έχουν γενικά κακή αξιοπιστία.
Όπως και με κάθε εξέταση, ο επιπολασμός της λοίμωξης από H. pylori και η πιθανότητα πρόβλεψης επηρεάζουν θετικά ή αρνητικά τις τιμές20,21. Συνολικά, όπου ο επιπολασμός της λοίμωξης από H. pylori και η πιθανότητα πρόβλεψης είναι χαμηλές η αρνητική προγνωστική αξία της ορολογικής εξετάσεως είναι υψηλή, ενώ ψευδώς θετικές είναι συχνότερες με το αντίθετο σε υψηλό επιπολασμό και πιθανότητα (δηλαδή, η θετική προγνωστική αξία είναι υψηλή αλλά υπάρχει αυξημένη επικράτηση ψευδών αρνητικών αποτελεσμάτων). Για παράδειγμα, ένας ασθενής με επιβεβαιωμένο πεπτικό έλκος θα έχει υψηλή πιθανότητα λοίμωξης και θα ήταν αποδεκτή η έναρξη της θεραπείας με βάση ένα θετικό ορολογικό έλεγχο, ενώ μια αρνητική εξέταση μπορεί να είναι ψευδώς αρνητική και θα πρέπει να γίνει επιβεβαίωση χρησιμοποιώντας μια εξέταση για την ενεργό λοίμωξη.
Σε αντίθεση, μια αρνητική εξέταση μπορεί να είναι ψευδώς αρνητική και θα πρέπει να απαιτηθεί επιβεβαίωση χρησιμοποιώντας μια εξέταση για ενεργό λοίμωξη. Από την άλλη πλευρά, μια θετική ορολογική εξέταση σε ασθενή με συμπτωματική γαστροοισοφαγική παλινδρόμηση σε περιοχές χαμηλής επικράτησης πιθανότατα θα είναι ψευδώς θετική και η επιβεβαίωση θα γίνει με μια εξέταση για την ενεργή λοίμωξη πριν την έναρξη της θεραπείας. Οι εξετάσεις αντισωμάτων δεν μπορούν να χρησιμοποιηθούν για την επιβεβαίωση της εξάλειψης. Ωστόσο, εάν μια γνωστή θετική εξέταση αντισωμάτων αρνητικοποιηθεί μετά από πολλούς μήνες, μπορεί κανείς να υποθέσει με αξιοπιστία την επιτυχή έκβαση της θεραπείας. Έχει αποδειχθεί ότι οι τίτλοι H. pylori μειώνονται κατά περίπου 50% σε 3 μήνες και η ορομετατροπή από ανιχνεύσιμα σε μη ανιχνεύσιμα επίπεδα στους 18 μήνες μετά τη θεραπεία είχε εξειδίκευση 100% αποδεικνύοντας ότι συσχετίζονται με αξιοπιστία με τη θεραπεία22. Ωστόσο, η ορομετατροπή δεν συμβαίνει συχνά. Ο ορολογικός έλεγχος μπορεί να είναι χρήσιμος όταν η πιθανότητα είναι υψηλή (π.χ., ενεργό πεπτικό έλκος) και οι εξετάσεις ενεργούς λοίμωξης είναι αρνητικοί, πιθανώς λόγω της παρουσίας των παραγόντων που μειώνουν το βακτηριακό φορτίο όπως η χρήση αντιβιοτικών ή βισμούθιου ή η διάχυτη γαστρική ατροφία όπως σε γαστρική ατροφία ή MALT λέμφωμα.
Υπάρχει ένας αριθμός ταχείας εξετάσεως στο ιατρείο που βασίζονται στις IgG. Περισσότερο προσβάσιμες είναι αυτές που χρησιμοποιούν μία σταγόνα πλήρους αίματος που λαμβάνεται από το δάκτυλο. Οι περισσότερες από αυτές τις εξετάσεις έχουν χαμηλότερη ευαισθησία και ειδικότητα από τις παραδοσιακές εξετάσεις ELISA και γενικά δεν συνιστώνται23. Παρά το γεγονός ότι το H. pylori διαφέρει σε λοιμογόνο δύναμη, καμία κλινική χρησιμότητα δεν έχει βρεθεί σε σχέση με την αξιολόγηση της παρουσίας των θεωρούμενων H. pylori λοιμογόνων παραγόντων, όπως CagA ή VacA9.
5.1.2. Εξέταση Σιέλου και Ούρων. Οι εξετάσεις αντισωμάτων οι οποίες χρησιμοποιούν σίελο και ούρα έχουν αναπτυχθεί επειδή τα δείγματα μπορούν εύκολα να ληφθούν, ειδικά από παιδιά. Οι μελέτες δείχνουν ότι οι IgG αναλύσεις του σιέλου δεν είναι τόσο ευαίσθητες όπως είναι οι ιστολογικές ή ορολογικές εξετάσεις24,25. Γενικά, λόγω του χαμηλού επιπολασμού της λοίμωξης στα παιδιά, όλες οι εξετάσεις θα συνδέονται με ένα υψηλό ποσοστό ψευδώς θετικών αποτελεσμάτων και ως γενικός κανόνας, μόνο τα παιδιά με δύο θετικές εξετάσεις που βασίζονται σε διαφορετικές μεθόδους θα πρέπει να θεωρούνται ότι έχουν λοίμωξη από H.pylori.
5.1.3. Εξέταση Αναπνοής Ουρίας (UBT). Η εξέταση αναπνοής ουρίας είναι η μη -επεμβατική εξέταση εκλογής για τη διάγνωση του H. pylori 26,27. Η μέθοδος βασίζεται στη δραστικότητα ουρεάσης του H.pylori, η οποία διασπά την ουρία σε αμμωνία και διοξείδιο του άνθρακα. Η εξέταση μπορεί να πραγματοποιηθεί με την ουρία σεσημασμένη με ραδιενεργό ισότοπο του άνθρακα 14C ή το μη ραδιενεργό φυσικό σταθερό ισότοπο 13C. Η σεσημασμένη ουρία με άνθρακα χορηγείται από του στόματος, συχνά σε συνδυασμό με ένα δοκιμαστικό γεύμα για την καθυστέρηση της γαστρικής κένωσης και την αύξηση του χρόνου επαφής με το βλεννογόνο. Το προτιμώμενο δοκιμαστικό γεύμα είναι το κιτρικό οξύ, το οποίο επίσης προκαλεί όξινση του στομάχου και αναστέλλει τη δραστηριότητα της μη – H. pylori ουρεάσης. Η εξέταση πραγματοποιείται στον ασθενή με νηστεία στερεάς τροφής για τουλάχιστον 1 ώρα. Η H. pylori ουρεάση ελευθερώνει το σεσημασμένο CO2 το οποίο ανιχνεύεται σε δείγματα αναπνοής τα οποία λαμβάνονται συνήθως 15 έως 20 λεπτά μετά από την κατάποση της ουρίας26,28. Ο 14C-UBT απαιτεί ένα μετρητή σπινθηρισμού και τεχνικούς οι οποίοι έχουν εκπαιδευτεί στη χρήση των ραδιενεργών χημικών ουσιών. Η 13C-UBT απαιτεί μια μάζα ή υπέρυθρο φασματόμετρο. Υπάρχουν αμφιβολίες όσον αφορά την πυρηνική ρύθμιση για τη χρήση της δοκιμής 13C σε παιδιά ή έγκυες γυναίκες. Γενικά, η χρήση ραδιοϊσοτόπων πρέπει να περιορίζεται σε αυτούς που έχουν ανάγκη.
Το UBT είναι μια ισχυρή εξέταση με υψηλή ευαισθησία (95%) και ειδικότητα (95% έως 100%) για την ανίχνευση των δραστικών λοιμώξεων με H. pylori αν και είναι λιγότερο ακριβής σε παιδιά ηλικίας κάτω των 6 ετών, εκτός εάν γίνει υπολογισμός του αποτελέσματος με τη χρήση του ποσοστού υδρόλυσης της ουρίας29. Ψευδώς θετικά αποτελέσματα δεν είναι συχνά εκτός από τις περιοχές όπου η ατροφική γαστρίτιδα είναι κοινή και η δοκιμασία δεν περιλαμβάνει κιτρικό οξύ28,30. Ψευδώς αρνητικά αποτελέσματα μπορεί να παρατηρηθούν σε ασθενείς που λαμβάνουν αντι-εκκριτική θεραπεία, βισμούθιο ή αντιβιοτικά και οσει ασθενείς με αιμορραγία του ανωτέρου γαστρεντερικού31. Για τη μείωση των ψευδώς αρνητικών αποτελεσμάτων ο ασθενής θα πρέπει να μην λαμβάνει αντιβιοτικά για τουλάχιστον τέσσερις εβδομάδες και PPIs για τουλάχιστον δύο εβδομάδες9.
5.1.4. 13C – Ουρία Αίματος. Μια έκδοση της εξέτασης 13C-ουρίας αίματος (Εz-ΗΒΤ, Metabolic Solutions Inc., Nashua, ΝΗ) εγκρίθηκε από το FDA ως ένα μη επεμβατικό εργαλείο για τη διάγνωση της λοίμωξης με H.pylori. Αυτή εκτελείται με τη μέτρηση των επιπέδων του 13C στο αίμα κατά την έναρξη και 60 λεπτά μετά την κατάποση της 13C ουρίας. Αν και η εξέταση απέδειξε εξαιρετική ευαισθησία της τάξεως του 92% έως 100% και ειδικότητα 96% έως 97%32, δεν χρησιμοποιείται στην κλινική πράξη.
5.1.5. Εξετάσεις αντιγόνου κοπράνων. Το H. pylori το οποίο ανιχνεύεται στον στόμαχο αποβάλλεται με τα κόπρανα. Τα διαθέσιμα εμπορικά κιτ ποιοτικής ανοσοδοκιμασίας ενζύμου έχει αποδειχθεί ότι είναι σε θέση να ανιχνεύσουν τα πρωτεϊνικά αντιγόνα H. pylori σε συγκέντρωση νανογραμμάρια ανά κ.εκ. κοπράνων. Μελέτες που αξιολογούν την ικανότητα των εξετάσεων αντιγόνου κοπράνων για τη διάγνωση της λοίμωξης από H. pylori είναι γενικά υποστηρικτικές. Οι πολυκλωνικές εξετάσεις αντιγόνων στα κόπρανα έχει αποδειχθεί ότι είναι λιγότερο ευαίσθητες και ειδικές συγκριτικά με τις εξετάσεις μονοκλωνικών αντισωμάτων και δεν συνιστώνται πλέον9,26,33,34. Η ευαισθησία και ειδικότητα των εξετάσεων που αναφέρθηκαν με βάση τα μονοκλωνικά αντισώματα είναι παρόμοια με εκείνα της εξέτασης αναπνοής ουρίας7,9 και άρα οι δοκιμές μπορούν να χρησιμοποιηθούν εναλλακτικά. Και οι δύο απαιτούν τις ίδιες προφυλάξεις για την αρχική διάγνωση της λοίμωξης από H. pylori και για την επιβεβαίωση της εξάλειψης μετά τη θεραπεία 35. Για ασθενείς που δεν μπορούν να διακόψουν τη θεραπεία με PPI δύο εβδομάδες πριν από την εξέταση αντιγόνων στα κόπρανα, τα θετικά αποτελέσματα μπορεί να θεωρηθούν ως αληθώς θετικά, ενώ τα αρνητικά αποτελέσματα μπορεί να θεωρηθούν ψευδώς αρνητικά και θα πρέπει να γίνει επιβεβαίωση με επαναληπτικές εξετάσεις δύο εβδομάδες μετά τη διακοπή της θεραπείας με PPI. Για τους ασθενείς που αναφέρουν σοβαρά συμπτώματα επιτρέπονται τα αντιόξινα ή οι ανταγωνιστές των υποδοχέων ισταμίνης-2 και τα οποία δεν αλληλεπιδρούν με τις δοκιμές36. Λόγω της παρατεταμένης απέκκρισης των αντιγόνων του ελικοβακτηριδίου του πυλωρού, έχει προταθεί ότι οι εξετάσεις επιβεβαίωσης της θεραπείας πρέπει να καθυστερήσουν μέχρι 6 εβδομάδες μετά το τέλος της θεραπείας.
5.1.6. Ταχείες Εξετάσεις αντιγόνου κοπράνων. Έχει αναπτυχθεί ένας αριθμός ταχείας (στο ιατρείο) εξέτασης αντιγόνου κοπράνων για H.pylori. Δύο μεγάλες μελέτες έδειξαν υψηλή ακρίβεια με ευαισθησία προ της θεραπείας στο 93% και 95% και της ειδικότητας στο 89% και 87%. Μετά την εκρίζωση, οι αναφερόμενες ευαισθησία και ειδικότητα ήταν 94% και 100%, 97% και 91%, αντίστοιχα37. Ωστόσο, υπάρχει μια σειρά από άλλες αναφορές και περιλήψεις που δείχνουν πολύ χαμηλότερη επιτυχία και η χρήση ταχείας εξέτασης αντιγόνου κοπράνων δεν συνιστάται9.
5.2. Επεμβατικές Εξετάσεις.
Οι επεμβατικές εξετάσεις τυπικά απαιτούν ενδοσκόπηση του ανώτερου γαστρεντερικού (EΑΓ). Η ΕΑΓ είναι ο χρυσός κανόνας για τα επιγαστρικά συμπτώματα επειδή επιτρέπει την άμεση επιθεώρηση του ανώτερου γαστρεντερικού βλεννογόνου και δίνει την ευκαιρία για λήψη δειγμάτων βιοψίας. Η ΕΑΓ είναι ευρέως διαθέσιμη στις ανεπτυγμένες χώρες. Ωστόσο, είναι ακριβή, δυσάρεστη, χρονοβόρα και δεν είναι ακίνδυνη. Η ΕΑΓ ενδείκνυται σε ασθενείς με συμπτώματα συναγερμού (δείτε τον κατάλογο συμπτωμάτων συναγερμού τα οποία ενθαρρύνουν την ενδοσκόπηση για την αξιολόγηση των ασθενών με δυσπεψία) ή σε άτομα ηλικίας ≥55 ετών, σύμφωνα με την Αμερικανική Γαστρεντερολογική Ένωση και τις κατευθυντήριες οδηγίες του Αμερικανικού Κολεγίου Γαστρεντερολογίας 2,5,38. Στην Ευρώπη, η προτεινόμενη ηλικία είναι τα 45 χρόνια για τους ασθενείς με επίμονη δυσπεψία9. Οι βιοψίες του στομάχου θα πρέπει να ληφθούν για να αποκλειστεί η ύπαρξη H. pylori και για την ιστολογική αξιολόγηση του γαστρικού βλεννογόνου9. Τα δείγματα μπορεί επίσης να χρησιμοποιηθούν για την βακτηριακή καλλιέργεια και τις δοκιμές ευαισθησίας στα αντιβιοτικά, ιδίως σε ασθενείς που έχουν προηγουμένως αποτυχημένη θεραπεία εκρίζωσης του ελικοβακτηριδίου. Άλλα ευρήματα πρέπει να θεραπεύονται σύμφωνα με την διάγνωση.
5.2.1. Εξέταση Βιοψίας Ουρεάσης.
Η δραστικότητα της βιοψίας ουρεάσης που συχνά αποκαλείται ταχεία δοκιμή ουρεάσης, βασίζεται στο γεγονός ότι το H. pylori περιέχει το ένζυμο ουρεάση και επομένως η παρουσία της λοίμωξης μπορεί εύκολα να ταυτοποιηθεί χρησιμοποιώντας μια χρωματομετρική δοκιμασία με βάση την αλλαγή του ρΗ όταν η ουρία υδρολύεται σε αμμωνία και CO2 . Ένας αριθμός εξετάσεων με βάση τη γέλη, με βάση τα υγρά και με βάση το χαρτί είναι εμπορικά διαθέσιμες με παρόμοια διαγνωστική ακρίβεια39. Μερικές από τα νεότερες εξετάσεις παρέχουν αξιόπιστα αποτελέσματα εντός μιας ώρας δίνοντας στον γαστρεντερολόγο την δυνατότητα παροχής θεραπεία εκρίζωσης του H. pylori στους ασθενείς πριν από την έξοδο από την ενδοσκοπική αίθουσα40. Φθηνή και αξιόπιστη ταχεία εξέταση ουρεάσης (ζωμός ουρίας συν μία σταγόνα 1% ερυθρού της φαινόλης ως δείκτη του pH) θα μπορούσε να γίνει σε οποιοδήποτε εργαστήριο. Η ευαισθησία και η ειδικότητα της εξέτασης βιοψίας ουρεάσης είναι περίπου 90% έως 95% και 95% έως 100%, αντίστοιχα38. Πρόσφατη γαστρεντερική αιμορραγία, χρήση αναστολέων αντλίας πρωτονίων και / ή αντιβιοτικά ή/και ενώσεις που περιέχουν βισμούθιο και η παρουσία της ατροφικής γαστρίτιδας ή / και διάχυτης εντερικής μεταπλασίας μπορεί να οδηγήσουν σε ψευδώς αρνητική εξέταση30,41. Με βάση την εμπειρία, το H. pylori εντοπίζεται συχνότερα στο άντρο και στο σώμα (80%), μόνο στο σώμα 10% και μόνο στο άντρο σε 8% των περιπτώσεων42.
Επειδή μια θετική εξέταση ταχείας ουρεάσης βασίζεται στο βακτηριακό φορτίο της γαστρικής βιοψίας, η λήψη δειγμάτων ιστού από το άντρου και το σώμα με τη χρήση μεγάλων λαβίδων ή με πολλαπλά δείγματα αυξάνει την ευαισθησία της εξέτασης21,28,43.
Ψευδώς θετικές εξετάσεις είναι ασυνήθιστες. Ωστόσο, η χλωρίδα της στοματικής κοιλότητας μπορεί να παράγει ουρεάση και να μολύνει τα δείγματα. Είναι σημαντικό για τον ενδοσκόπο να γίνει λήψη δειγμάτων από μακροσκοπικά φυσιολογικό βλεννογόνο καθώς το H. pylori αποικίζει υγιή γαστρικό ιστό και όταν η βιοψία λαμβάνεται από βλεννογόνο με μη φυσιολογική εμφάνιση (π.χ., εντερική μεταπλασία) ή από βλάβη είναι συχνά αρνητική.
5.2.2. Ιστολογία. Οι γαστρικές βιοψίες παρέχουν πληροφορίες σχετικά με την παρουσία και τον τύπο της γαστρίτιδας και αν επιπλέκεται από εντερική μεταπλασία, δυσπλασία, ατροφία, MALT λέμφωμα ή γαστρικό καρκίνο. Οι χρώσεις αιματοξυλίνης και ηωσίνης (Η&Ε) είναι εξαιρετικές στον καθορισμό της γαστρικής μορφολογίας αλλά είναι ανεπαρκείς για την ανίχνευση του ελικοβακτηριδίου του πυλωρού και έτσι συνιστάται μια ειδική χρώση η οποία είναι η τροποποιημένη χρώση Giemsa (2% αραιίωση).
Η αυξανόμενη χρήση των αναστολέων αντλίας πρωτονίων που προωθούν την παρουσία των κοκκοειδών μορφών του ελικοβακτηριδίου του πυλωρού 44 στο γαστρικό βλεννογόνο έχει οδηγήσει πολλά εργαστήρια στο να εγκαταλείψουν αυτές τις μη ειδικές χρώσεις και αντί αυτών να χρησιμοποιούν την ανοσοϊστοχημεία με ειδικά αντι-H.pylori αντισώματα για την τελική πιστοποίηση. Παρά την υψηλή ευαισθησία της ιστολογικής εξετάσεως, προβλήματα που σχετίζονται με τη δειγματοληψία, το χειρισμό και την επεξεργασία των δειγμάτων ιστού και τη διαφορετικότητα μεταξύ των παθολογοανατόμων θα μπορούσαν να επηρεάσουν τα αποτελέσματα45. Εξαιτίας του αποσπασματικού αποικισμού των βακτηρίων, είναι δυνατόν να αυξηθεί η ακρίβεια με πολλαπλές βιοψίες. Σε μια μελέτη, ο συνδυασμός τεσσάρων περιοχών βιοψίας (μικρότερη και μεγαλύτερη καμπυλότητα των μέσων του άντρου, μικρότερη και μεγαλύτερη καμπυλότητα των μέσων του σώματος) βρέθηκε να παρέχει μια καλή απόδοση για την ανίχνευση του ελικοβακτηριδίου του πυλωρού και την αξιολόγηση της έκτασης της ατροφικής γαστρίτιδας45.
5.2.3. Αξιολόγηση της Γαστρίτιδας. Φλεγμονώδη κύτταρα στον φυσιολογικό γαστρικό βλεννογόνο απουσιάζουν ή είναι σπάνια. Επειδή η λοίμωξη με το H. pylori έχει ως αποτέλεσμα την έντονη διείσδυση του βλεννογόνου με οξεία και χρόνια φλεγμονώδη κύτταρα, η ιστολογική εξέταση μπορεί έμμεσα να επισημάνει την παρουσία της λοίμωξης. Η οξεία ή ενεργός φλεγμονή αποτελείται από ουδετερόφιλα τα οποία διηθούν την επιφάνεια, το επιθήλιο και τον ίδιο τον υμένα. Αυτό χαρακτηριστικά συνοδεύεται από μία χρόνια φλεγμονή που αποτελείται από λεμφοκύτταρα, πλασματοκύτταρα και διάσπαρτα μακροφάγα. Αυτό το πρότυπο ονομάζεται συχνά οξεία – επί – χρόνια γαστρίτιδα (ή ενεργή χρόνια γαστρίτιδα) και είναι χαρακτηριστική των λοιμώξεων με το H.pylori. Λεμφαδένες είναι συχνά παρόντες.
Οι παθολογοανατόμοι χρησιμοποιούν συχνά ένα οργανωμένο σύστημα βαθμολόγησης για να περιγράψουν τα ευρήματά τους (π.χ., το Επικαιροποιημένο Σύστημα Σίδνεϊ)46. Το Σύστημα Sydney αξιολογεί την ιστολογία, την τοπογραφία, τη μορφολογία και την αιτιολογία και βαθμολογεί την ιστολογία με τη χρήση οπτικών αναλογικών κλιμάκων (π.χ., για την αξιολόγηση της πυκνότητας του ελικοβακτηριδίου του πυλωρού). Η προσέγγιση του Συστήματος Sydney χρησιμοποιείται στη συνέχεια σε συστήματα για τη σταδιοποίηση του γαστρικού κινδύνου για καρκίνου, όπως το σύστημα σταδιοποίησης OLGA (Λειτουργικό Σύστημα Αξιολόγησης Γαστρίτιδας)47.
Το H. pylori στη μορφολογική ανάλυση φαίνεται ως τυπικό σπειροειδούς ή καμπύλου σχήματος βακτήριο στην επιφάνεια του επιθηλίου και στο στρώμα του βλεννογόνου στο δείγμα της βιοψίας. Όπως σημειώνεται παραπάνω, η διαδεδομένη χρήση των αναστολέων αντλίας πρωτονίων οδηγεί συχνά σε μερικά μη – H. pylori βακτήρια ή κοκκοειδείς μορφές με ειδικές χρώσεις και έχει οδηγήσει πολλούς παθολόγους στη χρηση ανοσοϊστοχημικών χρώσεων για την επιβεβαίωση της λοίμωξης από H. pylori48.
5.2.4. Τεχνικές Ανοσοχρώσης. Η ανοσοϊστοχημεία χρησιμοποιώντας την τεχνική της ανοσοϋπεροξειδάσης μετά από θερμικά προκαλούμενη ανάκτηση του αντιγόνου για την ανίχνευση του H. pylori με τη γαστρική βιοψία έχει αποδειχθεί ότι είναι ιδιαίτερα ευαίσθητη, εύκολη στη χρήση και αξιόπιστη παρά το γεγονός ότι είναι ακριβή48.
5.2.5. BRUSH Κυτταρολογία. Στην τεχνική αυτή η επιφάνεια του βλεννογόνου δειγματοληπτείται χρησιμοποιώντας ένα ενδοσκόπιο ή ακόμη και από το στόμα με την κατάποση BRUSH και στη συνέχεια χρωνινται (π.χ., με Quick Diff) για οργανισμούς και H.pylori. Στην BRUSH κυτταρολογική εξέταση έχει αναφερθεί ευαισθησία 95% έως 98% και ειδικότητα 96%, αντίστοιχα49.
5.2.6. Μοριακές εξετάσεις. Η αλυσιδωτή αντίδραση πολυμεράσης (PCR), ο in situ υβριδισμός και η σε πραγματικό χρόνο PCR έχουν επίσης χρησιμοποιηθεί για την ανίχνευση του H.pylori, την αξιολόγηση της ευαισθησίας σε αντιβιοτικά ή την αξιολόγηση της παρουσίας των θεωρούμενων λοιμογόνων παραγόντων. Η ευαισθησία και η ειδικότητα για τη διάγνωση της λοίμωξης από H.pylori, χρησιμοποιώντας in situ υβριδισμό με βιοτινυλιωμένους ανιχνευτές, έχει αναφερθεί να είναι 95% έως 100%50. Το γονιδιακού DNA που προσδιορίζεται ως στόχος ενίσχυσης είναι 16S rRNA, ουρία, ureB, ureC, fiaA, CagA, VacA και πρωτεΐνες θερμικού σοκ51. Αποτελέσματα σε πραγματικό χρόνο μπορεί επίσης να ληφθούν συντομεύοντας σημαντικά το χρόνο για ένα αποτέλεσμα52.
Η PCR δεν χρησιμοποιείται συνήθως για τη διάγνωση διότι η ειδικότητα έχει παραμείνει ένα ζήτημα και τα ψευδώς θετικά αποτελέσματα συχνά σχετίζονται με την χλωρίδα του στόματος.
Η PCR έχει αποδειχθεί χρήσιμη για τη εξέταση της ευαισθησίας του H. pylori στην κλαριθρομυκίνη και βασίζεται στο γεγονός ότι η αντίσταση στην κλαριθρομυκίνη σχετίζεται με σημειακές μεταλλάξεις (Α-Gμετάβαση) στην 23S rRNA53. Η PCR έχει επίσης χρησιμοποιηθεί με επιτυχία σε γαστρικά δείγματα βιοψίας από ταχείες εξετάσεις ουρεάσης και ακόμη και από τα κόπρανα. Εναλλακτικά, ο φθορισμός in situ υβριδισμού (FISH) έχει χρησιμοποιηθεί σε τομές παραφίνης γαστρικού βλεννογόνου Η μέθοδος FISH είναι ταχεία και ακριβής (92,6%) και θα μπορεί να παράσχει στον κλινικό ιατρό σημαντικές πληροφορίες σχετικά με την επιλογή της θεραπείας54.
5.2.7. Καλλιέργειες. Ο χρυσός κανόνας για την παρουσία των μολυσματικών ασθενειών είναι οι καλλιέργειες του οργανισμού. Ωστόσο, η συνήθη καλλιέργεια του ελικοβακτηριδίου του πυλωρού δεν είναι σήμερα ευρέως διαθέσιμη και, το πιο σημαντικό, τυπικά απαιτεί μια επεμβατική μέθοδο (ΕΑΓ) για να ληφθούν γαστρικά δείγματα. Κάθε έμπειρο μικροβιολογικό εργαστήριο μπορεί γρήγορα να μάθει για τις καλλιέργειες του ελικοβακτηριδίου του πυλωρού.
Η βακτηριακή ανάπτυξη αναγνωρίζεται ως H. pylori με βάση τη μορφολογία των αποικιών, τη μορφολογία των κυττάρων, την χρώση Gram και θετικές βιοχημικές αντιδράσεις που αφορούν την καταλάση, ουρεάση, οξειδάση και για θέματα μεταφοράς στο εργαστήριο μικροβιολογίας. Σε έμπειρα εργαστήρια το ποσοστό θετικής εκβάσεως είναι 90% έως 95%. Το H. pylori έχει απομονωθεί από τα κόπρανα αλλά με την κακή συνολική επιτυχία η καλλιέργεια κοπράνων δεν είναι προς το παρόν πρακτική55.
5.2.8. Έλεγχος Ευαισθησίας. Οι καλλιέργειες γίνονται συνήθως για τον προσδιορισμό της ευαισθησίας στα αντιβιοτικά. Τα περισσότερα εργαστήρια χρησιμοποιούν το εψηλομετρική εξέταση (????-test) αν και η εξέταση αραίωσης άγαρ είναι η μέθοδος αναφοράς56. Το ????-τεστ μπορεί να εντοπίσει με ακρίβεια στελέχη ευαίσθητα στη μετρονιδαζόλη αλλά μια ανάγνωση των ανθεκτικών ατόμων έχει αποδειχθεί ότι είναι ψευδής σε περίπου 25% των περιπτώσεων.
Συνιστούμε ότι όλα τα ανθεκτικά στη μετρονιδαζόλη στελέχη (από ????-test) να επιβεβαιώνονται με αραίωση άγαρ. Λαμβάνοντας υπόψη το τρέχον υψηλό επιπολασμό της κλαριθρομυκίνης και της αντοχής στις φθοριοκινολόνες είναι συνετό να πραγματοποιείται η καλλιέργεια και η αντιμικροβιακή δοκιμή ευαισθησίας πριν από τη χρήση ενός σχήματος που περιέχει κλαριθρομυκίνη ή φθοριοκινολόνες, καθώς και για τη λήψη αποφάσεων σχετικά με τη θεραπεία μετά την αρχική αποτυχία της θεραπείας. Ωστόσο, υπάρχει ισχυρό επιχείρημα στους συγγραφείς για την καλλιέργεια προεπεξεργασίας και τις δοκιμές ευαισθησίας μετά την πρώτη αποτυχία της θεραπείας και σίγουρα μετά τη δεύτερη.
5.3. Η Θεραπεία των Λοιμώξεων από Ελικοβακτηριδίου του πυλωρού. Η εκρίζωση της λοίμωξης από H. pylori αλλάζει δραματικά τη φυσική ιστορία της γαστρίτιδας και αποτρέπει τα επακόλουθα αυτής6. Ωστόσο, λοίμωξη από H. pylori δεν είναι εύκολο να θεραπευθεί. Όσον αφορά τις άλλες βακτηριακές λοιμώξεις, τα αντιβιοτικά είναι αναγκαία και, επί του παρόντος, ένας συνδυασμός αντιβιοτικών με αντιεκκριτική θεραπεία είναι το πρότυπο της θεραπείας. Επιπλέον, η αύξηση της μικροβιακής αντοχής έχει καταστήσει την επιτυχή θεραπεία των λοιμώξεων με ελικοβακτηριδίου του πυλωρού μια πρόκληση καθώς η αποτελεσματικότητα πολλών συνήθων θεραπειών όπως η παραδοσιακή τριπλή θεραπεία έχει μειωθεί σε απαράδεκτα χαμηλά επίπεδα57. Το ιδανικό θεραπευτικό σχήμα θα πρέπει να βασίζεται στην αντιμικροβιακή ευαισθησία, αλλά, στην πραγματική ζωή, οι κλινικοί ιατροί πρέπει να επιλέξουν τη θεραπεία χωρίς αυτή την προσέγγιση. Ως εκ τούτου, οι κανόνες επιλογής της καταλληλότερης θεραπείας για τους ασθενείς είναι η ευαισθητοποίηση σχετικά με
- αντιβιοτικά που χρησιμοποιούνται ήδη από τον ασθενή και την παρουσία φαρμακευτικής αλλεργίας,
- το ποσοστό της αντίστασης στα πλέον χρησιμοποιούμενα αντιβιοτικά
- τι λειτουργεί καλύτερα σε τοπικό επίπεδο.
Σε αρκετές περιπτώσεις, η αποτυχία λήψης καλών αποτελεσμάτων εξαρτάται από την άγνοια του ιατρού όσον αφορά τα φτωχά αποτελέσματα που λαμβάνονται σε τοπικό επίπεδο με τις παραδοσιακές θεραπείες. Η επιβεβαίωση της εξάλειψης μετά τη θεραπεία είναι υποχρεωτική58. Γενικά, οι μη επεμβατικές εξετάσεις όπως αντιγόνο κοπράνων ή η αναπνοή ουρίας θα πρέπει να χρησιμοποιούνται, εκτός εάν η ενδοσκόπηση ενδείκνυται λόγω των κλινικών ευρημάτων. Η επιβεβαίωση της εκρίζωσης του ελικοβακτηριδίου θα πρέπει να πραγματοποιείται τουλάχιστον τέσσερις εβδομάδες μετά τη θεραπεία. Αυτό θα πρέπει να καθυστερήσει εκτός εάν λαμβάνονται αντιβιοτικά για άλλους λόγους. Η χρήση των αναστολέων αντλίας πρωτονίων πρέπει να σταματήσει, τουλάχιστον 2 εβδομάδες πριν από τις εξετάσεις, για να μειωθεί η πιθανότητα ψευδών αρνητικών αποτελεσμάτων36. Μια θετική UBT εξέταση και η οποία πραγματοποιήθηκε ενωρίτερα είναι μια αξιόπιστη ένδειξη της αποτυχίας της θεραπείας αλλά οι αρνητικές εξετάσεις θα πρέπει να είναι επιβεβαιωμένα. Η ενδοσκόπηση με βιοψία για καλλιέργεια μπορεί να ενδείκνυται μετά από αρκετές αποτυχίες για τη λήψη δειγμάτων για καλλιέργεια και εξετάσεις ευαισθησίας. Η εξέταση αντισωμάτων δεν πρέπει να χρησιμοποιείται για την επιβεβαίωση της εκρίζωσης αφού τα αντισώματα συνεχίζουν να είναι παρόντα για μήνες ή ακόμη και χρόνια μετά τη θεραπεία εκρίζωσης.
6. Περίληψη
Για τους ασθενείς που παρουσιάζουν συμπτώματα δυσπεψίας ο πρώτος στόχος είναι ο διαχωρισμός αυτών με οργανικά αίτια (περίπου 25%) από εκείνους με λειτουργική δυσπεψία (περίπου 75%). Ένα λεπτομερές ιστορικό και η φυσική εξέταση είναι υποχρεωτικά προκειμένου να επιβεβαιωθεί ή να αποκλειστεί η παρουσία των συμπτωμάτων συναγερμού (δείτε τον κατάλογο των συμπτωμάτων συναγερμού που προτρέπουν σε ενδοσκόπηση για την αξιολόγηση των ασθενών με δυσπεψία). Οι ασθενείς με τα χαρακτηριστικά συναγερμού ή/και ≥45-55 ετών (με βάση τη συχνότητα του καρκίνου του στομάχου στη συγκεκριμένη γεωγραφική περιοχή) θα πρέπει να υποβάλλονται σε πρώιμη γαστροσκόπηση και/ή υπερηχογράφημα κοιλίας, σύμφωνα με τα συμπτώματα συναγερμού (Σχήμα 1). Σε ασθενείς ηλικίας μικρότερης των 55 ετών με συμπτώματα δυσπεψίας που προκαλούνται από ΜΣΑΦ, η θεραπεία πρέπει να διακόπτεται και να προτείνεται η θεραπεία με αναστολείς αντλίας πρωτονίων για οκτώ εβδομάδες. Οι ασθενείς με δυσπεπτικά συμπτώματα που υποδηλώνουν καθυστερημένη γαστρική κένωση (πρώιμο αίσθημα κορεσμού, γαστρική πληρότητα και έμετος) θα μπορούσαν να λάβουν μια εμπειρική θεραπεία με προκινητικούς παράγοντες. Σε περίπτωση επίμονων συμπτωμάτων, θα πρέπει να ληφθεί υπόψη η μελέτη της γαστρικής λειτουργίας (σπινθηρογράφημα, εξέταση αναπνοής, κλπ). Ασθενείς ηλικίας <55 ετών χωρίς συμπτώματα συναγερμού πρέπει να ελέγχονται και να αντιμετωπίζονται για λοίμωξη από H.pylori, όποιος και αν είναι ο επιπολασμός, ειδικά εκείνοι με οικογενειακό ιστορικό πεπτικού έλκους ή καρκίνο του στομάχου. Μη επεμβατική εξέταση επιλογής είναι η 13C-UBT ή η δοκιμασία αντιγόνου κοπράνων. Η εκρίζωση του H. pylori πρέπει να επιβεβαιωθεί με μη επεμβατικές εξετάσεις (13C-UBT ή δοκιμασία αντιγόνου κοπράνων). Για τους ασθενείς με θετικό οικογενειακό ιστορικό καρκίνου του στομάχου συνιστάται ο έλεγχος της εξάλειψης με EΑΓ και βιοψία. Η ενδοσκοπική αξιολόγηση ενδείκνυται σε ασθενείς με δυσπεψία που δεν έχει διερευνηθεί και χωρίς συμπτώματα ανακούφισης από την εμπειρική θεραπεία ή την εκρίζωση του ελικοβακτηριδίου του πυλωρού. Περαιτέρω αξιολογήσεις θα πρέπει να εξετάζονται με βάση τα συμπτώματα του ασθενούς.
ΒΙΒΛΙΟΓΡΑΦΙΑ
- J. Tack, N. J. Talley, M. Camilleri et al., “Functional gastroduodenal disorders,” Gastroenterology, vol. 130, no. 5, pp. 1466–1479, 2006.
- N. J. Talley, “American Gastroenterological Association medical position statement: evaluation of dyspepsia,” Gastroenterology, vol. 129, no. 5, pp. 1753–1755, 2005.
- D. A. Drossman, E. Corazziari, N. J. Talley, W. G. Thompson, and W. E. Whitehead, Eds., ROME II. The Functional Gastrointestinal Disorders. Diagnosis, Pathophysiology and Treatment: A Multinational Consensus, Degnon Associates, McLean, Va, USA, 2nd edition, 2000.
- M. B. Wallace, V. L. Durkalski, J. Vaughan et al., “Age and alarm symptoms do not predict endoscopic findings among patients with dyspepsia: a multicentre database study,” Gut, vol. 49, no. 1, pp. 29–34, 2001.
- N. J. Talley, N. B. Vakil, and P. Moayyedi, “American gastroenterological association technical review on the evaluation of dyspepsia,” Gastroenterology, vol. 129, no. 5, pp. 1756–1780, 2005.
- D. Y. Graham, “History of Helicobacter pylori, duodenal ulcer, gastric ulcer and gastric cancer,” World Journal of Gastroenterology, vol. 20, no. 18, pp. 5191–5204, 2014.
- K. Sugano, J. Tack, E. J. Kuipers et al., “Kyoto global consensus report on Helicobacter pylori gastritis,”Gut, vol. 64, no. 9, pp. 1353–1367, 2015.
- N. J. Talley and A. C. Ford, “Functional dyspepsia,” The New England Journal of Medicine, vol. 373, no. 19, pp. 1853–1863, 2015.
- P. Moayyedi, J. Deeks, N. J. Talley, B. Delaney, and D. Forman, “An update of the cochrane systematic review of Helicobacter pylori eradication therapy in nonulcer dyspepsia: resolving the discrepancy between systematic reviews,” American Journal of Gastroenterology, vol. 98, no. 12, pp. 2621–2626, 2003.
- P. Malfertheiner, F. Megraud, C. A. O’Morain et al., “Management of Helicobacter pylori infection—the Maastricht IV/ Florence consensus report,” Gut, vol. 61, no. 5, pp. 646–664, 2012.
- L. E. Mazzoleni, G. B. Sander, C. F. D. M. Francesconi et al., “Helicobacter pylori eradication in functional dyspepsia: HEROES trial,” Archives of Internal Medicine, vol. 171, no. 21, pp. 1929–1936, 2011.
- G. Maconi, M. Sainaghi, M. Molteni et al., “Predictors of long-term outcome of functional dyspepsia and duodenal ulcer after successful Helicobacter pylori eradication—a 7-year follow-up study,” European Journal of Gastroenterology and Hepatology, vol. 21, no. 4, pp. 387–393, 2009.
- K.-A. Gwee, L. Teng, R.-K. M. Wong, K.-Y. Ho, D.-S. Sutedja, and K.-G. Yeoh, “The response of Asian patients with functional dyspepsia to eradication of Helicobacter pylori infection,” European Journal of Gastroenterology and Hepatology, vol. 21, no. 4, pp. 417–424, 2009.
- X. Jin and Y.-M. Li, “Systematic review and meta-analysis from Chinese literature: the association between helicobacter pylori eradication and improvement of functional dyspepsia,” Helicobacter, vol. 12, no. 5, pp. 541–546, 2007.
- R. F. Harvey, J. A. Lane, P. Nair, et al., “Clinical trial: prolonged beneficial effect of Helicobacter pylorieradication on dyspepsia consultations —the Bristol Helicobacter Project,” Alimentary Pharmacology & Therapeutics, vol. 32, no. 3, pp. 394–400, 2010.
- P. Malfertheiner, F. Megraud, C. O’Morain, et al., “Current concepts in the management of Helicobacter pylori infection: the Maastricht III consensus report,” Gut, vol. 56, pp. 772–781, 2007.
- B. E. Lacy, N. J. Talley, G. R. Locke III et al., “Review article: current treatment options and management of functional dyspepsia,” Alimentary Pharmacology and Therapeutics, vol. 36, no. 1, pp. 3–15, 2012.
- C. T. Loy, L. M. Irwig, P. H. Katelaris, and N. J. Talley, “Do commercial serological kits for Helicobacter pylori infection differ in accuracy? A meta-analysis,” American Journal of Gastroenterology, vol. 91, no. 6, pp. 1138–1144, 1996.
- C. Burucoa, J.-C. Delchier, A. Courillon-Mallet et al., “Comparative evaluation of 29 commercialHelicobacter pylori serological kits,” Helicobacter, vol. 18, no. 3, pp. 169–179, 2013.
- T. J. Vecchio, “Predictive value of a single diagnostic test in unselected populations,” The New England Journal of Medicine, vol. 274, no. 21, pp. 1171–1173, 1966.
- T. Uotani and D. Y. Graham, “Diagnosis of Helicobacter pylori using the rapid urease test,” Annals of Translational Medicine, vol. 3, no. 1, article 9, 2015.
- M. Feldman, B. Cryer, E. Lee, and W. L. Peterson, “Role of seroconversion in confirming cure ofHelicobacter pylori infection,” The Journal of the American Medical Association, vol. 280, no. 4, pp. 363–365, 1998.
- P. Moayyedi, A. M. Carter, A. Catto, R. M. Heppell, P. J. Grant, and A. T. R. Axon, “Validation of a rapid whole blood test for diagnosing Helicobacter pylori infection,” The British Medical Journal, vol. 314, article 119, 1997.
- A. E. Simor, E. Lin, F. Saibil et al., “Evaluation of enzyme immunoassay for detection of salivary antibody to Helicobacter pylori,” Journal of Clinical Microbiology, vol. 34, no. 3, pp. 550–553, 1996.
- D. Y. Graham and S. Reddy, “Rapid detection of anti-Helicobacter pylori IgG in urine using immunochromatography,” Alimentary Pharmacology and Therapeutics, vol. 15, no. 5, pp. 699–702, 2001.
- X. Calvet, J. Sanchez-Delgado, A. Montserrat et al., “Accuracy of diagnostic tests for Helicobacter pylori: a reappraisal,” Clinical Infectious Diseases, vol. 48, no. 10, pp. 1385–1391, 2009.
- J. P. Gisbert and J. M. Pajares, “Review article: 13C-urea breath test in the diagnosis of Helicobacter pyloriinfection—a critical review,” Alimentary Pharmacology and Therapeutics, vol. 20, no. 10, pp. 1001–1017, 2004.
- A. Shiotani, M. P. Dore, and D. Y. Graham, “Urea breath test and rapid urease test,” in Helicobacter Pylori, H. Sazuki, R. Warren, and B. Marshall, Eds., chapter 9, Springer, Berlin, Germany, 2016.
- P. D. Klein, H. M. Malaty, S. J. Czinn, S. C. Emmons, R. F. Martin, and D. Y. Graham, “Normalizing results of 13C-urea breath testing for CO2 production rates in children,” Journal of Pediatric Gastroenterology and Nutrition, vol. 29, no. 3, pp. 297–301, 1999.
- T. Osaki, K. Mabe, T. Hanawa, and S. Kamiya, “Urease-positive bacteria in the stomach induce a false-positive reaction in a urea breath test for diagnosis of Helicobacter pylori infection,” Journal of Medical Microbiology, vol. 57, no. 7, pp. 814–819, 2008.
- J. P. Gisbert, C. Esteban, I. Jimenez, and R. Moreno-Otero, “13C-urea breath test during hospitalization for the diagnosis of Helicobacter pylori infection in peptic ulcer bleeding,” Helicobacter, vol. 12, no. 3, pp. 231–237, 2007.
- F. Ahmed, U. K. Murthy, W. D. Chey, P. P. Toskes, and D. A. Wagner, “Evaluation of the Ez-HBT Helicobacter blood test to establish Helicobacter pylori eradication,” Alimentary Pharmacology and Therapeutics, vol. 22, no. 9, pp. 875–880, 2005.
- F. Parente, G. Maconi, G. B. Porro, and M. Caselli, “Stool test with polyclonal antibodies for monitoringHelicobacter pylori eradication in adults: a critical reappraisal,” Scandinavian Journal of Gastroenterology, vol. 37, no. 7, pp. 747–749, 2002.
- M. P. Dore, R. Negrini, V. Tadeu et al., “Novel monoclonal antibody-based Helicobacter pylori stool antigen test,” Helicobacter, vol. 9, no. 3, pp. 228–232, 2004.
- L. E. Bravo, J. L. Realpe, C. Campo, R. Mera, and P. Correa, “Effects of acid suppression and bismuth medications on the performance of diagnostic tests for Helicobacter pylori infection,” The American Journal of Gastroenterology, vol. 94, no. 9, pp. 2380–2383, 1999.
- L. Gatta, N. Vakil, C. Ricci et al., “Effect of proton pump inhibitors and antacid therapy on 13C urea breath tests and stool test for Helicobacter pylori infection,” The American Journal of Gastroenterology, vol. 99, no. 5, pp. 823–829, 2004.
- L. Veijola, E. Myllyluoma, R. Korpela, and H. Rautelin, “Stool antigen tests in the diagnosis ofHelicobacter pylori infection before and after eradication therapy,” World Journal of Gastroenterology, vol. 11, no. 46, pp. 7340–7344, 2005.
- W. D. Chey, B. C. Y. Wong, and Practice Parameters Committee of the American College of Gastroenterology, “American College of Gastroenterology guideline on the management of Helicobacter pylori infection,” The American Journal of Gastroenterology, vol. 102, no. 8, pp. 1808–1825, 2007.
- L. Laine, D. Lewin, W. Naritoku, R. Estrada, and H. Cohen, “Prospective comparison of commercially available rapid urease tests for the diagnosis of Helicobacter pylori,” Gastrointestinal Endoscopy, vol. 44, no. 5, pp. 523–526, 1996.
- E. L. Young, T. K. Sharma, and A. F. Cutler, “Prospective evaluation of a new urea-membrane test for the detection of Helicobacter pylori in gastric antral tissue,” Gastrointestinal Endoscopy, vol. 44, no. 5, pp. 527–531, 1996.
- P. Saniee, S. Shahreza, and F. Siavoshi, “Negative effect of proton-pump inhibitors (PPIs) on Helicobacter pylori growth, morphology, and urease test and recovery after PPI removal—an in vitro study,”Helicobacter, vol. 21, no. 2, pp. 143–152, 2016.
- S. W. Moon, T. H. Kim, H. S. Kim, et al., “United rapid urease test is superior than separate test in detecting Helicobacter pylori at the gastric antrum and body specimens,” Clinical Endoscopy, vol. 45, no. 4, pp. 392–396, 2012.
- S. Olmez, M. Aslan, R. Erten, et al., “The prevalence of gastric intestinal metaplasia and distribution of helicobacter pylori infection, atrophy, dysplasia, and cancer in its subtypes,” Gastroenterology Research and Practice, vol. 2015, Article ID 434039, 6 pages, 2015.
- L. Cellini, R. Grande, E. Di Campli et al., “Dynamic colonization of Helicobacter pylori in human gastric mucosa,” Scandinavian Journal of Gastroenterology, vol. 43, no. 2, pp. 178–185, 2008.
- H. Ota and R. M. Genta, “Morphological characterization of the gastric mucosa during infection with H. pylori,” in The Immunobiology of H. pylori from Pathogenesis to Prevention, P. Ernst, P. Michetti, and P. D. Smith, Eds., pp. 15–28, Lippincott-Raven, Philadelphia, Pa, USA, 1997.
- J. J. Misiewicz, G. N. J. Tytgat, C. S. Goodwin, et al., “The Sydney system: a new classification of gastritis,” in Working Party Reports, pp. 1–10, World Congress of Gastroenterology, Sydney, Australia, 1990.
- M. Rugge, J. G. Kim, V. Mahachai et al., “OLGA gastritis staging in young adults and country-specific gastric cancer risk,” International Journal of Surgical Pathology, vol. 16, no. 2, pp. 150–154, 2008.
- L. Marzio, D. Angelucci, L. Grossi, M. G. Diodoro, E. Di Campli, and L. Cellini, “Anti-Helicobacter pylori specific antibody immunohistochemistry improves the diagnostic accuracy of Helicobacter pylori in biopsy specimen from patients treated with triple therapy,” The American Journal of Gastroenterology, vol. 93, no. 2, pp. 223–226, 1998.
- A. A. Mostaghni, M. Afarid, S. Eghbali, and P. Kumar, “Evaluation of brushing cytology in the diagnosis of Helicobacter pylori gastritis,” Acta Cytologica, vol. 52, no. 5, pp. 597–601, 2008.
- H. Liu, A. Rahman, C. Semino-Mora, S. Q. Doi, and A. Dubois, “Specific and sensitive detection of H. pylori in biological specimens by real-time RT-PCR and in situ hybridization,” PLoS ONE, vol. 3, no. 7, Article ID e2689, 2008.
- Y. Yamaoka, T. Kodama, O. Gutierrez, J. G. Kim, K. Kashima, and D. Y. Graham, “Relationship betweenHelicobacter pylori iceA, cagA, and vacA status and clinical outcome: studies in four different countries,”Journal of Clinical Microbiology, vol. 37, no. 7, pp. 2274–2279, 1999.
- K. A. Kreuzer, U. Lass, A. Bohn, et al., “LightCycler technology for the quantitation of bcr/abl fusion transcripts,” Cancer Research, vol. 59, no. 13, pp. 3171–3174, 1999.
- J. Versalovic, M. S. Osato, K. Spakovsky et al., “Point mutations in the 23S rRNA gene of Helicobacter pylori associated with different levels of clarithromycin resistance,” Journal of Antimicrobial Chemotherapy, vol. 40, no. 2, pp. 283–286, 1997.
- Ö. Yilmaz, E. Demiray, S. Tümer, et al., “Detection of H. pylori and determination of clarithromycin susceptibility using formalin-fixed, paraffin-embedded gastric biopsy specimens by fluorescence in situ hybridization,” Helicobacter, vol. 12, pp. 136–141, 2007.
- M. P. Dore, M. S. Osato, H. M. Malaty, and D. Y. Graham, “Characterization of a culture method to recover Helicobacter pylori from the feces of infected patients,” Helicobacter, vol. 5, no. 3, pp. 165–168, 2000.
- F. Mégraud and P. Lehours, “Helicobacter pylori detection and antimicrobial susceptibility testing,”Clinical Microbiology Reviews, vol. 20, no. 2, pp. 280–322, 2007.
- D. Y. Graham, “Hp-normogram (normo-graham) for assessing the outcome of H. pylori therapy: effect of resistance, duration, and CYP2C19 genotype,” Helicobacter, vol. 21, no. 2, pp. 85–90, 2016.
- D. Y. Graham, “The only good Helicobacter pylori is a dead Helicobacter pylori,” The Lancet, vol. 350, pp. 70–71, 1997.










Άφησε σχόλιο