Εισαγωγή
Μεταγευματική Υπερτριγλυκεριδαιμία
Η μεταγευματική υπερτριγλυκεριδαιμία αποτελεί έναν ανεξάρτητο παράγοντα κινδύνου για την εμφάνιση καρδιαγγειακών συμβαμάτων. Ο Zilversmit ήταν ο πρώτος που υπέθεσε πως η αθηρογένεση είναι ένα μεταγευματικό φαινόμενο και επισήμανε την ανάγκη να διερευνηθούν τα επίπεδα των λιποπρωτεϊνών μετά από την κατανάλωση ενός λιπαρού γεύματος. Η κύρια διαταραχή στα λιπίδια μεταγευματικά είναι η υπερτριγλυκεριδαιμία1.
Η αύξηση στο πλάσμα των τριγλυκεριδίων λίγες ώρες μετά από την κατανάλωση ενός γεύματος προέρχεται από δυο κύριες πηγές: τα τριγλυκερίδια που απορροφώνται από το λεπτό έντερο με τη μορφή των χυλομικρών (CMs) και τα τριγλυκερίδια που παράγονται στο ήπαρ με τη μορφή των πολύ χαμηλής πυκνότητας λιποπρωτεϊνών (VLDL)2. Τα χυλομικρά συντίθεται στο λεπτό έντερο και μεταφέρουν τη χοληστερόλη και τα τριγλυκερίδια του γεύματος από το σημείο της απορρόφησής τους στο εντερικό επιθήλιο σε άλλα κύτταρα του σώματος. Το λίπος πέπτεται και απορροφάται κατά τη διάρκεια των γευμάτων και “πακετάρεται” στα χυλομικρά. Τα τελευταία διέρχονται μέσω της λεμφικής οδού στη συστηματική κυκλοφορία. Τα τριγλυκερίδια στην κυκλοφορία υδρολύονται μέσω του ενζύμου λιποπρωτεϊνική λιπάση (LPL), που βρίσκεται στην ενδοθηλιακή επιφάνεια των τριχοειδών.
Μετά την υδρόλυση σχηματίζονται τα υπολείμματα των χυλομικρών (CM remnants). Τα τελευταία έχουν δυο διαφορετικούς δρόμους απομάκρυνσης από την κυκλοφορία. Ο ένας δρόμος είναι μέσω του μυϊκού και του λιπώδους ιστού, όπου τα υπολείμματα των χυλομικρών αποδομούνται μέσω της λιποπρωτεϊνικής λιπάσης (LPL) με συμπαράγοντα την απολιποπρωτεϊνη C-II ( apo C-II)3. Ο άλλος δρόμος είναι μέσω του ήπατος, με τη διαδικασία της ενδοκύττωσης. Έχουν αναγνωριστεί δύο δρόμοι μέσω των οποίων γίνεται η ενδοκύττωση των υπολειμμάτων των χυλομικρών. Ο ένας είναι μέσω του LDL υποδοχέα, ενώ ο δεύτερος μέσω της πρωτεΐνης που σχετίζεται με τον LDL υποδοχέα (LDL – receptor related protein – LRP). Κατά τη διάρκεια του φυσιολογικού μεταβολισμού τα υπολείμματα των χυλομικρών δεσμεύονται στους υποδοχείς των LDL στο ήπαρ. Σε καταστάσεις ινσουλινοαντίστασης, όπως στην παχυσαρκία και στον σακχαρώδη διαβήτη τύπου ΙΙ, καθώς και σε αυξημένη σύνθεση χοληστερόλης και σε γενετικά προδιατεθειμένες καταστάσεις, οι υποδοχείς των LDL υφίστανται κορεσμό. Τότε τα υπολείμματα των χυλομικρών δεσμεύονται στην πρωτεΐνη που σχετίζεται με τον υποδοχέα της LDL (LRP)4.
Η δεύτερη πηγή τριγλυκεριδίων είναι οι VLDL. Η παραγωγή τους εξαρτάται από την ποσότητα του υποστρώματος για τη σύνθεση χοληστερόλης στο ήπαρ, η οποία ρυθμίζει την έκφραση των LDL υποδοχέων. Η παραγωγή των VLDL εξαρτάται επίσης από την παροχή ελευθέρων λιπαρών οξέων στο ήπαρ και την ποσότητα των αποθηκευμένων στο ήπαρ τριγλυκεριδίων. Η μεταγευματική υπερτριγλυκεριδαιμία μετά από κατανάλωση λιπαρού γεύματος είναι ένα πολυπαραγοντικό φαινόμενο. Φαίνεται πως υπάρχει ένα όριο για την ποσότητα του προσλαμβανόμενου λίπους, για το οποίο δεν υπερβαίνεται η ικανότητα κάθαρσης των τριγλυκεριδίων από το ήπαρ και συνεπώς δε μεταβάλλεται μεταγευματικά η ποσότητα των λιποπρωτεϊνών5.Οι μεταβολές στις λιποπρωτεΐνες μεταγευματικά, αφορούν κυρίως την αύξηση των λιποπρωτεϊνών που είναι πλούσιες σε τριγλυκερίδια. Οι τελευταίες είναι ετερογενείς και περιλαμβάνουν τα υπολείμματα των χυλομικρών και των VLDL. Η μεταγευματική υπερτριγλυκεριδαιμία είναι πιθανόν το αποτέλεσμα του συναγωνισμού μεταξύ των υπολειμμάτων των χυλομικρών και των VLDL για την λιποπρωτεϊνική λιπάση και τους ηπατικούς υποδοχείς6,7.
Αξιολόγηση του Μεταβολισμού των Τριγλυκεριδίων Μεταγευματικά
Η τιμή των τριγλυκεριδίων σε κατάσταση όχι νηστείας μπορεί να αποτελέσει έναν καλό δείκτη, ο οποίος αντιπροσωπεύει τον κίνδυνο για διαταραχή του μεταβολισμού των τριγλυκεριδίων (μεταγευματικού δυσμεταβολισμού)8,9.Μια δημοσίευση από μια ομάδα ειδικών (Expert Panel Statement) αναφέρει πως η τιμή τριγλυκεριδίων σε κατάσταση μη νηστείας όταν είναι μικρότερη από 180mg/dl, θεωρείται επιθυμητή. Αντίθετα, αν η τιμή των τριγλυκεριδίων σε κατάσταση μη νηστείας είναι μεγαλύτερη από 200mg/dl, τότε συνιστάται περαιτέρω έλεγχος με μέτρηση των τριγλυκεριδίων σε κατάσταση νηστείας ή διενέργεια δοκιμασίας ανοχής λίπους (Oral Fat Tolerance Test- OFTT).
Η δοκιμασία ανοχής λίπους χρησιμοποιείται για να μελετήσει τη δυναμική του μεταγευματικού μεταβολισμού των λιποπρωτεϊνών σε αντιστοιχία με τη δοκιμασία ανοχής στη γλυκόζη (OGTT), που αξιολογεί την ανοχή στη γλυκόζη. Οι κύριοι παράγοντες που καθορίζουν τη μεταγευματική αύξηση των τριγλυκεριδίων μετά από ένα λιπαρό γεύμα είναι η ποσότητα του προσλαμβανόμενου λίπους που περιέχεται στο γεύμα, καθώς και η τιμή των τριγλυκεριδίων νηστείας. Με βάση μια συστηματική μετα- ανάλυση 119 μελετών έγινε η σύσταση στη δοκιμασία ανοχής λίπους να καταναλώνονται 75gr λίπους, αφού έχει προηγηθεί νηστεία 8 ωρών. Σε φυσιολογικά άτομα η τιμή των τριγλυκεριδίων αυξάνει για περισσότερες από 3-4 ώρες μετά το γεύμα και παραμένει αυξημένη για 6 έως 8 ώρες. Η μεταγευματική αύξηση των τριγλυκεριδίων είναι υπερβολική και παρατεταμένη σε άτομα με διάφορες μεταβολικές διαταραχές όπως ο Σακχαρώδης Διαβήτης ή σε περιπτώσεις υπερτριγλυκεριδαιμίας που οφείλεται σε γενετικά αίτια. Η αύξηση των τριγλυκεριδίων μετά από τη δοκιμασία ανοχής λίπους αξιολογείται από τις τιμές των τριγλυκεριδίων σε δείγματα αίματος που λαμβάνονται κάθε 1 ή 2 ώρες και για 6 έως 8 ώρες συνολικά. Η έλλειψη ενός τυποποιημένου γεύματος καθώς και η έλλειψη επίσημων συστάσεων σε ότι αφορά τα μεσοδιαστήματα μεταξύ των αιμοληψιών για τη λήψη δειγμάτων για τον προσδιορισμό των τριγλυκεριδίων δυσκολεύουν λίγο την αξιολόγηση της μεταγευματικής λιπαιμικής απάντησης. Επίσης, δεν υπάρχουν τυποποιημένες τιμές αναφοράς για τις AUG των τιμών των τριγλυκεριδίων10 . Δεδομένα από μια μετα-ανάλυση μελετών για την αξιολόγηση της μεταγευματικής λιπαιμίας συστήνουν μια μόνο μέτρηση των τριγλυκεριδίων μεταγευματικά στις 4 ώρες μετά από την κατανάλωση του λιπαρού γεύματος. Η επιθυμητή τιμή για την τελευταία είναι μικρότερη από 220mg/dl. Αυτό προτάθηκε ομόφωνα από ομάδα ειδικών στα λιπίδια ( Consensus Expert Panel )11.
CETP (Cholesterol Ester Transfer Protein)
Οι καταστάσεις με αυξημένα τριγλυκερίδια φαίνεται να ευνοούν την ανταλλαγή εστεροποιημένης χοληστερόλης μεταξύ των λιποπρωτεϊνών μέσω της πρωτεΐνης CETP (Cholesterol Ester Tranfer Protein)12.H CETP είναι μια υδρόφοβη γλυκοπρωτεΐνη που παράγεται κυρίως από το ήπαρ13,14 και προωθεί την ανακατανομή εστεροποιημένης χοληστερόλης, τριγλυκεριδίων και φωσφολιπιδίων μεταξύ των λιποπρωτεϊνών. Επίσης, συμβάλλει στην μεταφορά λιπιδίων μεταξύ των λιποπρωτεϊνών, με τέτοιο τρόπο, ώστε να αποκαθίσταται ισορροπία στα λιπίδια μεταξύ των λιποπρωτεϊνών15 .
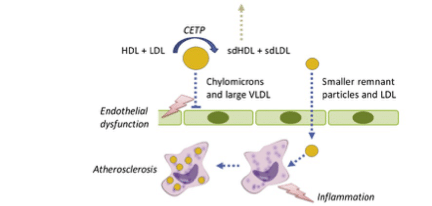
Όταν το επίπεδο των VLDL είναι φυσιολογικό, τότε γίνεται μεταφορά εστεροποιημένης χοληστερόλης από την HDL στην LDL16. Όταν η συγκέντρωση των VLDL είναι αυξημένη, η εστεροποιημένη χοληστερόλη της HDL μεταφέρεται μέσω της πρωτεΐνης CETP στις μεγάλες VLDL λιποπρωτεΐνες. Έτσι, οι HDL εμπλουτίζονται με τριγλυκερίδια και αποτελούν υπόστρωμα για την ηπατική λιπάση με αποτέλεσμα να καθαίρονται γρήγορα από την κυκλοφορία. Με αυτόν τον τρόπο τα επίπεδα της HDL μειώνονται17,18. Η HDL εκτός από την αντίστροφη μεταφορά χοληστερόλης, έχει πλειοτροπικές δράσεις, όπως αντιοξειδωτικές και αντιφλεγμονώδεις ιδιότητες19,20.
Μηχανισμοί μέσω των οποίων οι λιποπρωτεϊνες που είναι πλούσιες σε τριγλυκερίδια προκαλούν καρδιαγγειακή νόσο 21 .
Η Σημασία της Γενετικής Μεταγευματικής Υπερτριγλυκεριδαιμίας.
Οι λιποπρωτεΐνες στο πλάσμα υφίσταται μια σειρά από αλλαγές στη σύνθεση και στη συγκέντρωσή τους κατά τη διάρκεια της μεταγευματικής περιόδου. Η ικανότητα ενός ατόμου να ανταποκρίνεται επαρκώς στην πρόσληψη λίπους, δηλαδή η ικανότητά του να καταβολίζει αποτελεσματικά τα τριγλυκερίδια που συσσωρεύονται κατά τη διάρκεια της μεταγευματικής περιόδου, εξαρτάται από περιβαλλοντικούς και γενετικούς παράγοντες που εξηγούν την εξατομικευμένη μεταβλητότητα που παρατηρείται στη μεταγευματική λιπιδαιμική απάντηση22.
Σε ότι αφορά το σκέλος της γενετικής συνιστώσας παλαιότερες μελέτες που έχουν διεξαχθεί έχουν εξετάσει πολυμορφισμούς ενός νουκλεοτιδίου (Single-nucleotide polymorphisms, SNPs) σε συγκεκριμένα γονίδια που σχετίζονται με ειδικά και χαρακτηριστικά γνωρίσματα. Οι πιο σύγχρονες μελέτες έχουν επεκταθεί στη μελέτη συνδυασμού αλληλόμορφων που τείνουν να μεταβιβάζονται μαζί.
Έχουν μελετηθεί διάφοροι πολυμορφισμοί γονιδίων που φαίνεται να τροποποιούν τον μεταβολισμό των λιπιδίων μεταγευματικά.
Σκοπός Μελέτης – Υλικό Και Μέθοδος
Η επίδραση των πολυμορφισμών Taq1b και I405V της πρωτεΐνης CETP στην μεταγευτική κατανομή των τριγλυκεριδίων δεν έχει μελετηθεί σε άτομα με σακχαρώδη διαβήτη.
Στη μελέτη συμμετείχαν 51 άνδρες με σακχαρώδη διαβήτη τύπου 2 , υπό αγωγή με δισκία, καλή γλυκαιμική ρύθμιση HbA1c <7%, με BMI £ 30 Kg/m2 χωρίς ιστορικό στεφανιαίας νόσου και τριγλυκερίδια νηστείας έως 150mg/dl. Η τιμή των τριγλυκεριδίων νηστείας δύναται να είναι έως 180mg/dl, για να υποβληθεί το άτομο στη δοκιμασία φόρτισης με λίπος με βάση νεότερες μελέτες13. Άτομα με τριγλυκερίδια νηστείας μεγαλύτερα από 180mg/dl είναι ακατάλληλα να υποβληθούν στη δοκιμασία ανοχής λίπους γιατί παρουσιάζουν παρατεταμένη μεταγευματική λιπαιμία στην πλειοψηφία τους και δεν δύναται να ωφεληθούν από αυτήν την δοκιμασία.
Από τη μελέτη εξαιρέθηκαν άτομα που λαμβάνουν οποιαδήποτε υπολιπιδαιμική αγωγή, άτομα με δευτεροπαθή αίτια δυσλιπιδαιμίας, όπως άτομα με ΣΔ που δεν είναι καλά ρυθμισμένα (HbA1c>7%), άτομα με υποθυρεοειδισμό, λήψη φαρμάκων που προκαλούν δυσλιπιδαιμία, όπως οι β-αναστολείς, τα διουρητικά, τα οιστρογόνα, τα κορτικοειδή, η αμιοδαρόνη. Στη μελέτη δεν συμμετείχαν επίσης αλκοολικοί, άτομα με νεφρωσικό σύνδρομο ή στάδιο 4 ή 5 χρόνια νεφρικής νόσου (Clearance Creat <30ml/min), άτομα με δυσλιπιδαιμία που σχετίζεται με HIV λοίμωξη καθώς και άτομα με φλεγμονώδη νοσήματα του εντέρου και γαστρεντερικές διαταραχές (αργή κένωση στομάχου).
Τα άτομα της υπό μελέτης ομάδας υποβλήθηκαν σε δοκιμασία ανοχής λίπους. Το λιπαρό γεύμα ήταν μια παραλλαγή αυτού που χρησιμοποίησαν ο Patsch και οι συνεργάτες του23 . Η ποσότητα του χορηγούμενου γεύματος υπολογίζεται με βάση την επιφάνεια σώματος (350 gr/2m2).
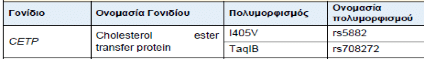
Προσδιορίστηκαν τα επίπεδα των τριγλυκεριδίων νηστείας 2, 4, 6 και 8 ώρες μετά την κατανάλωση λιπαρού γεύματος. Ταυτόχρονα, μελετήθηκαν οι πολυμορφισμοί Taq1b και I405V της πρωτεΐνης μεταφέρουσας εστέρων χοληστερόλης (CETP).
Η μελέτη των πολυμορφισμών των διαφόρων γονιδίων έγινε μετά την απομόνωση του DNA, με τη μέθοδο της αλυσιδωτής αντίδρασης πολυμεράσης και εν συνεχεία με τη χρήση περιοριστικών ενδονουκλεασών.
Για τη στατιστική ανάλυση χρησιμοποιήθηκε το Mann Whitney U test για τη σύγκριση ποσοτικών μεταβλητών μεταξύ 2 ομάδων. Το Kruskal Wallis H test χρησιμοποιήθηκε για τη σύγκριση ποσοτικών μεταβλητών μεταξύ 3 ομάδων. Η επιφάνεια υπό την καμπύλη (Area Under the Curve- AUC) για τις τιμές των τριγλυκεριδίων νηστείας και μεταγευματικά υπολογίστηκε με τον τραπεζοειδή κανόνα. Για να αξιολογήσουμε την επίδραση των αλληλίων στις μεταγευματικές τιμές των τριγλυκεριδίων εφαρμόστηκε ανάλυση πολλαπλής γραμμικής παλινδρόμησης με προσαρμογή για την ηλικία και το δείκτη μάζας σώματος όπου η TG AUC ήταν η εξαρτημένη μεταβλητή.
Η στατιστική σημαντικότητα ορίστηκε ως p<0.05. Τα δεδομένα αναλύθηκαν με το σύστημα SPSS (SPSS 20.0, Chicago, IL, USA).
Αποτελέσματα
Η συχνότητα του Taq1b πολυμορφισμού για την CETP είναι 38% Β1Β1, 48% Β1Β2, 14% Β2Β2. Η συχνότητα εμφάνισης του πολυμορφισμού I405V για την CETP είναι 48% ΙΙ, 40% ΙV και 12% VV.
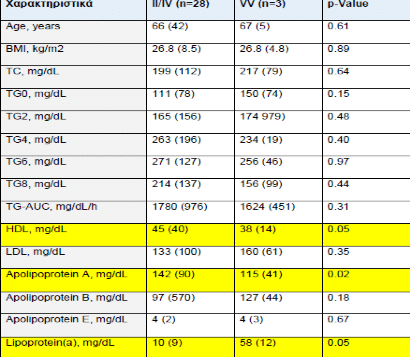
Σχετικά με τον πολυμορφισμό Taq1b, οι φορείς των αλληλίων Β1 και Β2 δεν φάνηκε να εμφάνισαν στατιστικά σημαντική διαφορά στα επίπεδα των τριγλυκεριδίων μετά το λιπαρό γεύμα. TG-AUC 1776 για το αλλήλιο Β1 και 1795 για το αλλήλιο Β2 (p=0.68). Για τον πολυμορφισμό I405V οι φορείς των αλληλίων I και V δεν εμφάνισαν στατιστικά σημαντική διαφορά στα επίπεδα των τριγλυκεριδίων μετά το λιπαρό γεύμα εκτός από τα επίπεδα της HDL-c, της ApoA και της Lp(a). Οι φορείς του αλλήλιου V εμφάνισαν υψηλότερα επίπεδα Lp(a) ( p= 0.05) και χαμηλότερα επίπεδα HDL-c (p=0.05) και ApoA (p= 0.02) σε σχέση με τους φορείς του αλλήλιου Ι στην ομάδα με τη θετική καμπύλη.
Κλινικά Και Μεταβολικά Χαρακτηριστικά στα Άτομα με τη Θετική Καμπύλη σε Σχέση με τον Πολυμορφισμό Cetp Taq 1b
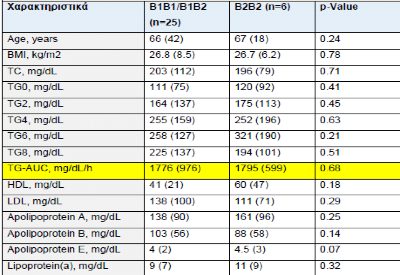
Κλινικά και Μεταβολικά Χαρακτηριστικά στα Άτομα με την Θετική Καμπύλη σε Σχέση με τον Πολυμορφισμό CETP I405V
Τα Αποτελέσματα της Πολλαπλής Παλινδρόμησης Φαίνονται στον Παρακάτω Πίνακα.
| Ανεξάρτητες μεταβλητές | Συντελεστής συσχέτισης | Σταθερό σφάλμα | P value ( πιθανότητα) |
| Ολικό δείγμα | |||
| Β1 vs B2 | 0.236 | 146.353 | 0.153 |
| I vs V | -0.202 | 153.331 | 0.203 |
| ΟΜΑΔΑ ΘΕΤΙΚΗΣ ΚΑΜΠΥΛΗΣ | |||
| Β1 vs B2 | -0.033 | 104.769 | 0.872 |
| I vs V | -0.102 | 157.495 | 0.593 |
| ΟΜΑΔΑ ΑΡΝΗΤΙΚΗΣ ΚΑΜΠΥΛΗΣ | |||
| Β1 vs B2 | 0.010 | 194.948 | 0.970 |
| I vs V | -0.387 | 122.074 | 0.187 |
Συμπεράσματα
Οι πολυμορφισμοί της CETP Taq1b καθώς και I405V δεν φαίνεται να συσχετίζονται με την μεταγευματική κατανομή των τριγλυκεριδίων στους διαβητικούς ασθενείς μετά από κατανάλωση λιπαρού γεύματος.
ΒΙΒΛΙΟΓΡΑΦΙΑ
- Zilversmit DB. Atherogenesis: a postprandial phenomenon. Circulation 1979; 60(3):473-485.
- Cohn JS, Johnson E J, Millar JS et al. Contribution of apoB-48 and apoB-100 triglyceride-rich lipoproteins (TRL) to postprandial increases in the plasma concentration of TRL triglyceride and retinyl esters. J Lipid Res 1993; Dec 34(12): 2033-40.
- Cooper A D. Hepatic uptake of chylomicron remnants. J Lipid Res 1997 Nov; 38(11): 2173-2192.
- Yu K C, Chen W, Cooper AD. LDL receptor- related protein mediates cell surface clustering and hepatic sequestration of chylomicron remnants in LDLR-deficient mice. J Clin Invest 2001 Jun; 107(11): 1387-1394.
- Dubois C, Beaumier G, Juhel C, et al. Effects of graded amounts (0- 50) gr of dietary fat on postprandial lipemia and lipoproteins in normolipidemic adults. Am J Clin Nutr 1998 Jan; 67(1): 31-38.
- Cassader M, Gambino R, Musso G et al. Postprandial triglyceride- rich lipoprotein metabolism and insulin sensitivity in nonalchoolic steatohepatitis patients. Lipids 2001 Oct; 36(10) : 1117-1124.
- Herd SL, Kiens B, Boobis LH et al. Moderate Exercise, postprandial lipemia and skeletal muscle lipoprotein lipase activity. Metabolism 2001 Jul; 50(7): 756-762.
- Langsted A, Freinberg JJ, Nordestgaard BG. Fasting and non-fasting lipid levels: influence of normal food intake on lipids, lipoproteins, apolipoproteins and cardiovascular risk prediction. Circulation 2008;118:2047-2056.
- Nakajima K, Saito T, Tamura A, et al. Cholesterol in remnant-like lipoproteins in human serum using monoclonal anti apoB-100 and anti apo A-I immunoaffinity mixed gels. Clin Chim Acta Int Clin Chem 1993; 223: 53-71.
- Mihas C, Kolovou GD, Mikhailidis DP, ET AL. Diagnostic value of postprandial triglyceride testing in healthy subjects: a meta- analysis. Curr Vasc Pharmacol 2011;9:302-308.
- Kolovou GD, Mikhailidis DP, Kovar J, et al. Assessment and clinical relevance of non-fasting and postprandial triglycerides: an expert panel statement. Curr Vasc Pharmacol 2011;9:258-270.
- Freeman DJ, Caslake M J, Griffin BA, et al. The effect of smoking on post-heparin lipoprotein and hepatic lipase, cholesterol ester transfer protein and lecithin cholesterol acytransferase activities in human plasma. Eur J Clin Invest 1998 Jul; 28(7):584-591.
- Barter P J, Brewer HB Jr, Chapman M J, et al. Cholesteryl ester transfer protein: a novel target for rising HDL and inhibiting atherosclerosis. Atheroscler Thromb Vasc Biol 2003 Feb 1; 23(2):160-167.
- Talk A R,. Plasma cholesteryl ester transfer protein. J Lipid Res 1993 Aug; 34(8):1255-1274.
- Barter P J, Hopkins G J, Calvert G D. Transfers and exchanges of esterified cholesterol between plasma lipoproteins. Biochem J 1982 Oct 15;208(1):1-7.
- Guerin M, Le Goff W, Lassel TS, et al. Atherogenic role of elevated CE transfer from HDL to VLDL (1) and dense LDL in type 2 diabetes: impact of the degree of triglyceridemia. Arterioscler Thromb Vasc Biol 2001;21(2):282-288.
- Brunzell JD, Hokanson JE. Low-density and high density lipoprotein subspecies and risk for premature coronary artery disease. Am J Med 1999, 23; 107(2A):165-185.
- Ginsberg HN, Huang LS. The insulin resistance syndrome: impact on lipoprotein metabolism and atherothrombosis. J Cardiovasc Risk 2000;7(5):325-331.
- Assmann G, Nofer J R. Atheroprotective effects of high-density lipoproteins. Annu Rev Med 2003; 5:321-341 Epub 2001 Dec 3.
- Kolovou G, Anagnostopoulou K, Daskalopoulou S, et al. Clinical Relevance of Postprandial Lipaemia. Current Medicinal Chemistry 2005;12:1931-1945.
- Boren J, Matikainen N, Adiels M, et al. Postprandial hypertriglyceridemia as a coronary risk factor. Clinica Chimica Acta 2014;431:131-142.
- Lopez-Miranda J, Perez- Martinez P, Marin C et al. Postprandial lipoprotein metabolism, genes and risk of cardiovascular disease. Curr Opin Lipidol 2006;17:132-138.
- Kolovou GD, Daskalova DCh, Iraklianou SA et al. Postprandial lipemia in hypertension. J Am Coll Nutr 2003;22(1):80-78.









Άφησε σχόλιο