Mohammed Nadeem Shaikh1, Brahma Reddy Malapati1, Ruchi Gokani2, Bhavita Patel,3 and Mitul Chatriwala4
1Department of Biochemistry, Parul Institute of Medical Science and Research (PIMSR), Limda, Waghodia, Gujarat 391760, India, 2Department of Biochemistry, C.U. Shah Medical Collage, Surendranagar, Gujarat, India, 3Department of Biochemistry, S.B.K.S MI & RC, Piparia, Vadodara, Gujarat 391760, India, 4Department of Biochemistry, Pramukhswami Medical College, Karamsad, Gujarat, India
Ιστορικό. Τα επίπεδα μαγνησίου στον ορό επηρεάζουν τη συγκέντρωση της κυκλοφορούσας βιταμίνης D στο αίμα και στη συνέχεια επηρεάζουν την ανοσία. Επομένως παίζουν σημαντικό ρόλο στην παθογένεση του άσθματος. Το άσθμα, στους ενήλικες, είναι λιγότερο μελετημένο και η υπομαγνησιαιμία μαζί με την ανεπάρκεια και την έλλειψη της βιταμίνης D είναι συχνά σε άτομα με άσθμα, γεγονός που προκαλεί συχνές κρίσεις άσθματος, αναπνευστικές λοιμώξεις, σοβαρές παροξύνσεις και κακή ανταπόκριση στα βρογχοδιασταλτικά.
Σκοπός. Η ανίχνευση του μεγέθους της ανεπάρκειας και έλλειψης της βιταμίνης D και των επιπέδων μαγνησίου στον ορό μεταξύ ασθενών με άσθμα και η συσχέτισή τους με τη σοβαρότητα του άσθματος.
Υλικά και μέθοδοι. Πρόκειται για μια διασταυρούμενη μελέτη που περιλαμβάνει 60 ασθενείς με χρόνιο σταθερό άσθμα και 60 υγιείς μάρτυρες. Μετά τη λήψη του κλινικού ιστορικού και τη συστηματική εξέταση, διερευνήθηκε η πνευμονική λειτουργία. Τα επίπεδα μαγνησίου ορού, 25-υδροξυχοληκαλσιφερόλης [25(ΟΗ)D] και ασβεστίου μετρήθηκαν σε όλα τα άτομα.
Αποτελέσματα. Σημαντική συσχέτιση διαπιστώθηκε μεταξύ ανεπάρκειας της βιταμίνης D, υπομαγνησιαιμίας και σοβαρότητας του άσθματος. Τα επίπεδα ασβεστίου στον ορό δεν επηρεάστηκαν από αυτό.
Συμπέρασμα. Η ανεπάρκεια της βιταμίνης D και μαγνησίου του ορού ανευρίσκονται σε υψηλή συχνότητα σε ασθενείς με άσθμα. Η αυξημένη σοβαρότητα του άσθματος, η συχνότητα των προσβολών και οι παροξύνσεις σχετίζονται με χαμηλότερα επίπεδα ενός ή και των δύο. Τα επίπεδα 25(OH)D και μαγνησίου μπορούν να χρησιμεύσουν ως σημαντικοί δείκτες της σοβαρότητας του άσθματος.
1. Εισαγωγή
Το βρογχικό άσθμα είναι μια χρόνια κατάσταση που χαρακτηρίζεται από υποτροπιάζοντα βρογχόσπασμο που προκύπτει από αναστρέψιμη βρογχική υπεραντιδραστικότητα ως αντίδραση σε ερεθίσματα ενός συγκεκριμένου επιπέδου ή έντασης, που συνήθως δεν προκαλεί σημαντική στένωση στα περισσότερα άτομα1. Το βρογχικό άσθμα παγκοσμίως είναι μία από τις πιο κοινές νόσους που πλήττουν περίπου 334 εκατομμύρια ανθρώπους. Έχει μεγάλο κοινωνικό αντίκτυπο με επιπολασμό περίπου 10-12% στους ενήλικες και 15% στα παιδιά. Μπορεί να ανευρεθεί σε οποιαδήποτε ηλικία2.
Το άσθμα είναι ευρέως διαδεδομένο σε όλο τον κόσμο, συμπεριλαμβανομένων των τροπικών χωρών όπως η Ινδία, αλλά έχει πολύ μεταβλητό επιπολασμό μεταξύ των διαφόρων πληθυσμών. Στην Ινδία, ο επιπολασμός είναι περίπου 2%1,2. Λόγω του ενδεχόμενου ρόλου της στην πρόληψη των αναπνευστικών λοιμώξεων, η ανεπάρκεια της βιταμίνης D αποτελεί σημαντικό ζήτημα δημόσιας υγείας. Η βασική λειτουργία της βιταμίνης D είναι η ρύθμιση της ομοιόστασης του ασβεστίου και του φωσφόρου και με τη σειρά του ο μεταβολισμός της βιταμίνης D ρυθμίζεται από παράγοντες που ανταποκρίνονται στη συγκέντρωση ασβεστίου, φωσφόρου και μαγνησίου στο πλάσμα.
Η καλσιτριόλη (δραστική μορφή της βιταμίνης D) εμπλέκεται στην έκκριση ινσουλίνης, στην αναστολή της παραγωγής ιντερλευκίνης από τα Τ-λεμφοκύτταρα και της ανοσοσφαιρίνης από τα Β-λεμφοκύτταρα, στην διαφοροποίηση προδρόμων μονοκυττάρων και στην διαμόρφωση του κυτταρικού πολλαπλασιασμού. Τα κύτταρα του ανοσοποιητικού συστήματος όπως τα Τ-λεμφοκύτταρα, τα ενεργοποιημένα Β-λεμφοκύτταρα και τα δενδριτικά κύτταρα εκφράζουν τους υποδοχείς της βιταμίνης D (VDRs)3. Τα δενδριτικά κύτταρα εκφράζουν επίσης την 1α-υδροξυλάση, γεγονός που υποδηλώνει ότι η 25-υδροξυχοληκαλσιφερόλη (Calcitriol) μπορεί να μετατραπεί σε ενεργό μορφή (Calcitriol) τοπικά και έτσι συμμετέχει στην ανοσοαπόκριση. Επιπλέον, η βιταμίνη D έχει βρεθεί ότι παίζει ρόλο στην έμφυτη ανοσία έναντι διαφόρων μικροβιακών παραγόντων. Προετοιμάζει την σύνθεση της καθελιδίνης και των ανοσοσφαιρινών4. Αυτό μπορεί να είναι ο πιθανός λόγος πίσω από τις θεραπευτικές επιδράσεις του ηλιακού φωτός στη φυματίωση και άλλες λοιμώξεις5. Έτσι, η βιταμίνη D είναι ένας από τους σημαντικούς ρυθμιστές της ανοσίας. Η ανεπάρκεια και η διέγερση των ερεθισμάτων μπορεί να αυξήσουν τον κίνδυνο άσθματος, αλλεργιών και επιδείνωσης των νόσων6.
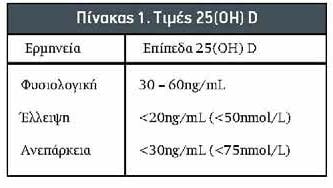
Με βάση λίγες προηγούμενες αναφορές, η ανεπάρκεια μαγνησίου (Mg) σχετίζεται με αυξημένη τραχειοβρογχική υπεραντιδραστικότητα, πνευμονική αγγειακή υστέρηση και κοιλιακή αρρυθμία7,8. Η θεραπεία με β2-αγωνιστές μπορεί να μειώσει τα επίπεδα μαγνησίου στον ορό με ενδοκυτταρική μετατόπιση ή απώλεια ούρων8. Το μαγνήσιο προκαλεί χάλαση των λείων βρογχικών μυών και διαστολή των αεραγωγών, πιθανότατα μεταβάλλοντας την μετακίνηση των ιόντων ασβεστίου. Αντίθετα, η υπομαγνησιαιμία μπορεί να προκαλέσει βρογχοσυστολή. Μπορεί να διαταράξει το νευρομυϊκό μηχανισμό σε τέτοιο βαθμό σε ορισμένα άτομα, γεγονός που μπορεί να οδηγήσει σε βρογχικούς σπασμούς9. Το μαγνήσιο (Mg) ως το δεύτερο πιο άφθονο ενδοκυττάριο κατιόν και σημαντικό μέρος της οστεοποίησης των οστών έχει ζωτική λειτουργία στη σύνθεση και τον μεταβολισμό της βιταμίνης D. Χαμηλότερα επίπεδα μαγνησίου ορού συσχετίζονται με την υποβιταμίνωση D10,11. Η υπομαγνησιαιμία μειώνει τη συγκέντρωση της βιταμίνης D στο σώμα, η οποία μπορεί να επιδεινώσει την κλινική κατάσταση του άσθματος από την τραχειοβρογχική υπερδραστηριότητα και αυξάνοντας την ευαισθησία στις αναπνευστικές λοιμώξεις4,5,7,9,10(Πίνακας 1).
Ως εκ τούτου, η μελέτη αυτή σχεδιάστηκε για την ανίχνευση του επιπολασμού της υπομαγνησιαιμίας με ανεπάρκεια και έλλειψη της βιταμίνης D στους ασθενείς με άσθμα στην Ινδία. Η μελέτη αυτή είχε ως στόχο επίσης στην αξιολόγηση της σχέσης των επιπέδων Mg ορού και βιταμίνης D με τη σοβαρότητα του άσθματος.
2. Υλικά και μέθοδοι
2.1. Σχεδιασμός Μελέτης. Πρόκειται για μια cross-sectional case-control μελέτη που διεξήχθη από τον Μάιο του 2014 μέχρι τον Ιούλιο του 2015. Η μελέτη περιελάμβανε 60 περιπτώσεις χρόνιου σταθερού άσθματος ως ομάδα Ι και 60 υγιή άτομα (μάρτυρες) σε συνδυασμό με ηλικία, φύλο και εθνοτική ομάδα ως ομάδα ΙΙ. Ασθενείς με φυματίωση ή οποιαδήποτε άλλη σχετιζόμενη αναπνευστική / συστηματική νόσο που υποβάλλονται σε διουρητική θεραπεία και ηλικίας <18 ετών εξαιρέθηκαν από τη μελέτη. Η επιλογή και η ταξινόμηση των ασθενών ήταν σύμφωνα με τις “κατευθυντήριες γραμμές GINA” της παγκόσμιας πρωτοβουλίας για το άσθμα12. Μια γραπτή ενημερωμένη συγκατάθεση δόθηκε από όλους τους συμμετέχοντες στη μελέτη πριν από την ένταξή τους. Η επιτροπή δεοντολογίας Sumandeep ενέκρινε τη μελέτη. Η ομάδα Ι (Ασθματικοί ασθενείς) περιελάμβανε 60 ασθενείς, 38 (63,3%) άνδρες και 22 (36,7%) γυναίκες. Οι ηλικίες τους κυμαίνονταν από 19 έως 71 έτη με μέση τιμή 40 ± 13 έτη. Η ομάδα II (ομάδα έλεγχου) περιελάμβανε 60 υγιείς ασθενείς, 45 (75%) άνδρες και 15 (25%) γυναίκες. Οι ηλικίες τους κυμαίνονταν μεταξύ 18 και 70 ετών με μέση τιμή 42 ± 11 έτη. Όλοι οι ασθενείς που συμμετείχαν στη μελέτη υποβλήθηκαν σε λήψη κλινικού ιστορικού, συμπεριλαμβανομένων των φαρμάκων και υπεβλήθησαν σε πλήρη συστηματική εξέταση. Τα δείγματα αίματος συλλέχθηκαν (με ενεργοποιητή θρόμβου) υπό άσηπτες συνθήκες για τη μέτρηση των επιπέδων μαγνησίου, βιταμίνης D(25(ΟΗ) D) και ασβεστίου ορού. Τέλος, πραγματοποιήθηκε δοκιμή πνευμονικής λειτουργίας (PFT) με σπιρομέτρηση σε κάθε ασθενή για να επιτευχθεί ο δυναμικά εκπνεόμενος όγκος (FEV1), ο FVC και ο PEF για τον προσδιορισμό της σοβαρότητας (ή του σταδίου) άσθματος.
2.2. Αναλυτικές Μέθοδοι. Τα επίπεδα 25(ΟΗ)D του ορού μετρήθηκαν με ανοσοπροσδιορισμό Chemiluminescent (CLIA) σε συσκευή Beckman Coulter, Access-2.
2.2.1. Αρχές Εξέτασης. Το κιτ δοκιμής είναι ένας ανοσοενισχυτικός προσδιορισμός ανταγωνιστικής δέσμευσης δύο σταδίων. Το δείγμα προστίθεται σε ένα δοχείο αντίδρασης με παράγοντα απελευθέρωσης DBP (πρωτεΐνη δέσμευσης βιταμίνης D) και με αντίσωμα αντι-25(ΟΗ)D από πρόβατα με παραμαγνητικά σωματίδια. Η DBP απελευθερώνει 25(ΟΗ) D η οποία δεσμεύεται με το σταθερό μονοκλωνικό αντι-25(ΟΗ)D. Στη συνέχεια προστίθεται ανάλογο 25(ΟΗ)D και συζευγμένης αλκαλικής φωσφατάσης και συνδέετε με σταθερό μονοκλωνικό αντι-25(ΟΗ)D. Τα μόρια που δεσμεύονται στα παραμαγνητικά σωματίδια συγκεντρώνονται σε ένα μαγνητικό πεδίο, ενώ τα μη δεσμευμένα υλικά απομακρύνονται. Στη συνέχεια, προστίθεται LumiPhos 530 (υπόστρωμα χημειοφωταύγειας) και το φωτόμετρο μετρά το φως που εκπέμπεται από την αντίδραση. Η παραγωγή φωτός είναι αντιστρόφως ανάλογη προς τη συγκέντρωση 25(ΟΗ)D στο δείγμα. Το εύρος αναφοράς της 25-υδροξυχοληκαλσιφερόλης παρουσιάζεται στον Πίνακα 1.
2.2.2. Ασβέστιο και Μαγνήσιο Ορού. Τα επίπεδα μαγνησίου ορού και ολικού ασβεστίου μετρήθηκαν φασματοφωτομετρικά με τη χρήση πλήρως αυτοματοποιημένου αναλυτή ERBA-EM200 και αντιδραστηρίων ERBA:
Εύρος αναφοράς μαγνησίου ορού: 1,7-2,5mg/dL
Εύρος αναφοράς ασβεστίου ορού: 8.6-10.3mg/dL
2.3. Στατιστικές Μέθοδοι. Τα αποτελέσματα καταλογοποιήθηκαν σε φύλλο MS Excel και πραγματοποιήθηκαν στατιστικές αναλύσεις χρησιμοποιώντας τις ακόλουθες μεθόδους:
- Χρησιμοποιήθηκαν περιγραφικά στατιστικά στοιχεία: για τη συνεχή μεταβλητή περιοχή, υπολογίστηκε η μέση τιμή (????) και η τυπική απόκλιση (sd) και υπολογίστηκαν τα ποσοστά της κατηγορία των μεταβλητών.
- Η σύγκριση μεταξύ δύο αναλογικών δειγμάτων έγινε με τη χρήση των 2 δειγμάτων ????-test και υπολογίσθηκαν οι τιμές p.
- Για να συγκριθούν μεταβλητές τριών ή περισσοτέρων ομάδων εφαρμόστηκε η μέθοδος ANOVA.
3. Αποτελέσματα
Ο Πίνακας 2 δείχνει τη δημογραφία και των δύο ομάδων. Μεταξύ των ασθματικών ασθενών (ομάδα Ι), 14 (23,3%) είχαν ήπιο επίμονο άσθμα, 27 (45%) είχαν μέτριο επίμονο άσθμα και 19 (31,7%) είχαν σοβαρό επίμονο άσθμα. Η σοβαρότητα της νόσου κατηγοριοποιήθηκε σύμφωνα με τις κατευθυντήριες γραμμές GINA, 201612. Οι μέσες τιμές ορού της βιταμίνης D και του μαγνησίου ήταν σημαντικά χαμηλότερες στους ασθενείς με άσθμα, σε σύγκριση με τους υγιείς μάρτυρες. Επιπλέον, τα αποτελέσματα δείχνουν σταδιακή πτώση των επιπέδων ορού τόσο της βιταμίνης D όσο και του μαγνησίου με την αυξημένη σοβαρότητα του άσθματος. Όπως φαίνεται στον Πίνακα 6 και στην Εικόνα 1, υπήρξε αρνητική συσχέτιση μεταξύ των επιπέδων της βιταμίνης D και του μαγνησίου ορού με τους βαθμούς σοβαρότητας του άσθματος. Δεν υπήρξε σημαντική διαφορά στα επίπεδα ασβεστίου στον ορό μεταξύ των ασθενών με άσθμα (9,51 ± 0,54mg/dL) και μάρτυρες (9,62 ± 0,35mg/dL).
Πίνακας 2. Κατανομή Ασθενών και Ομάδων Ελέγχου
Εικόνα 1: Επίπεδα Βιταμίνης D3 στα διάφορα στάδια άσθματος
Περιπτώσεις άσθματος
- Ήπιο
- Μέτριο
- Σοβαρό
- Ομάδα Ελέγχου
Όπως φαίνεται στον Πίνακα 3, 63,3% ασθματικοί ασθενείς είχαν ανεπάρκεια βιταμίνης D (<50nmol/L) ενώ 100% των ασθενών είχαν έλλειψη (<75nmol/L). Όσον αφορά τα επίπεδα μαγνησίου στον ορό, 58,8% ασθματικοί ασθενείς είχαν υπομαγνησιαιμία (<1,7mg/dL).

Ο Πίνακας 4 δείχνει τα επίπεδα μαγνησίου στον ορό σε διαφορετικές κατηγορίες χρόνιου σταθερού άσθματος. Ήπιο επίμονο: 1,86 ± 0,07mg/dL, μέτριο επίμονο: 1,70 ± 0,07mg/dL και σοβαρό επίμονο: 1,53 ± 0,09mg/dL. Αυτά τα δεδομένα δείχνουν σαφώς ότι τα επίπεδα του μαγνησίου στον ορό μειώνονται με την αύξηση της σοβαρότητας του άσθματος.
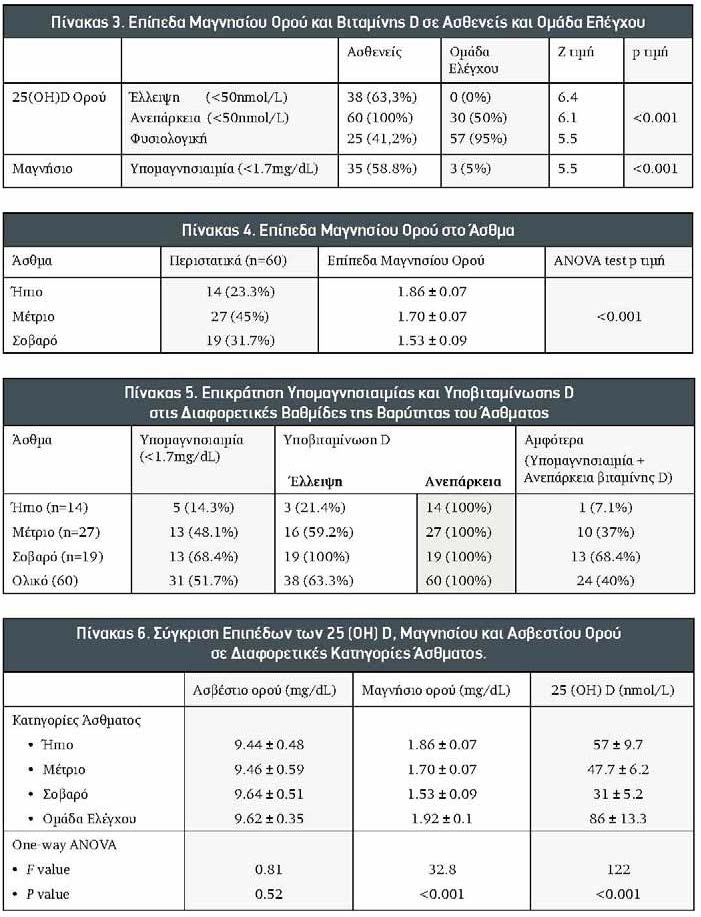
Όπως φαίνεται στον Πίνακα 5, ο επιπολασμός της υπομαγνησιαιμίας και της ανεπάρκειας της βιταμίνης D αυξάνεται με την αύξηση της σοβαρότητας της νόσου.
Ο Πίνακας 6 δείχνει ότι τα επίπεδα του μαγνησίου και της 25(OH)D μειώνονται με την αύξηση της σοβαρότητας της νόσου καθώς τα επίπεδα τους είναι υψηλότερα σε ήπια μορφή άσθματος, ενώ χαμηλότερα στο σοβαρό επίμονο άσθμα (???? <0,001). Τα επίπεδα ασβεστίου στον ορό δεν επηρεάστηκαν από τη μείωση σε άλλα δύο επίπεδα ανάλυσης και έτσι δεν επηρέασαν τη σοβαρότητα του άσθματος (???? = 0,52).
4. Συζήτηση
Η μελέτη μας αναγνωρίζει τη συχνότητα εμφάνισης ανεπάρκειας βιταμίνης D όσον αφορά την 25(OH)D <75nmol/L (<30ng/mL) και ανεπάρκεια <50nmol/L (<20ng/mL)13,14. Η μελέτη αυτή δείχνει ότι 63,3% των ασθενών είχαν ανεπάρκεια βιταμίνης D και το 100% είχε έλλειψη, ενώ, μεταξύ των ελέγχων το 50% είχε ανεπάρκεια και το 0% είχε έλλειψη. Το μέσο επίπεδο της 25(ΟΗ)D σε ασθενείς με άσθμα της ομάδας Ι (44,9 ± 12nmol/L) ήταν σημαντικά χαμηλότερο από τους ελέγχους της ομάδας II (86 ± 13,3nmol/L).
Η κατάσταση της βιταμίνης D στους ασθενείς με άσθμα έχει μελετηθεί από πολλούς ερευνητές. Ο Bener και συνεργάτες6 ανέφεραν τον επιπολασμό της έλλειψης της βιταμίνης D και της υπομαγνησιαιμίας σε παιδιά με άσθμα και κατέληξαν στο συμπέρασμα ότι η βιταμίνη D είναι ισχυρός προγνωστικός παράγοντας για το άσθμα. Ο Columbo και συνεργάτες15 έδειξε ότι το 79% των ηλικιωμένων ασθενών με άσθμα είχαν χαμηλότερη από τη φυσιολογική βιταμίνη D στον ορό κατά την έναρξη. Αυτά επιβεβαιώνουν ότι η ανεπάρκεια και η έλλειψη της βιταμίνης D είναι εξαιρετικά συχνή σε ηλικιωμένους ασθενείς με άσθμα και αναπνευστικά νοσήματα. Μια άλλη μελέτη από τους Ginde και συνεργάτες16 προσδιορίζει τη συσχέτιση των επιπέδων χαμηλής βιταμίνης D με υψηλότερη συχνότητα αναπνευστικών λοιμώξεων και αυξημένη σοβαρότητα του άσθματος. Ο Brehm και συνεργάτες17 στην ανάλυσή τους βρήκαν παρόμοια συσχέτιση και βρήκαν επίσης υψηλότερο επιπολασμό αλλεργικής ρινίτιδας με ανεπάρκεια βιταμίνης D. Οι λόγοι για τις εκτεταμένες ανεπάρκειες της βιταμίνης D σε διάφορους πληθυσμούς δεν είναι πλήρως κατανοητοί. Ωστόσο, η υψηλή κοινωνικοοικονομική κατάσταση και ο δυτικός τρόπος ζωής (καθεστηκυία και λιγότερη έκθεση σε ήλιο) μπορεί να συμβάλει στην ανεπάρκεια της βιταμίνης D, η οποία αυξάνει την ευαισθησία σε αλλεργικές παθήσεις, συμπεριλαμβανομένου του βρογχικού άσθματος. Στην τρέχουσα μελέτη, οι ασθενείς είχαν μειωμένα επίπεδα μαγνησίου στον ορό από τους μάρτυρες. Αυτό μπορεί να εξηγηθεί από την υπομαγνησιαιμία που προκαλείται από την επανειλημμένη χρήση των β2-αγωνιστών δια εισπνοής ή νεφελοποιητή18,19 η οποία εν συνεχεία προκαλεί ανεπάρκεια της βιταμίνης D20.
Η παρούσα μελέτη δείχνει τη σχέση μεταξύ ανεπάρκειας της βιταμίνης D, υπομαγνησιαιμίας και σοβαρότητας άσθματος. Αυτό αποδείχθηκε με βάση τα επίπεδα του ορού της 25(ΟΗ)D σε ασθματικούς ασθενείς με ήπιο επίμονο άσθμα: 57 ± 9,7nmol/L, μέτριο επίμονο άσθμα: 47,7 ± 6,2nmol/L και σοβαρό επίμονο άσθμα: 31 ± 5,2nmol/L και η οποία είναι σε συμφωνία με τους Brehm και συν.17, Sandhu και Casale21, οι οποίοι ανέφεραν ότι η υποβιταμίνωση D αυξάνει τον κίνδυνο σοβαρής επιδείνωσης του άσθματος στα παιδιά. Η μελέτη μας δείχνει την επικράτηση της υπομαγνησιαιμίας σε διαφορετικές κατηγορίες άσθματος: ήπιο επίμονο άσθμα: 1,86 ± 0,07mg/dL (23,3%), μέτριο επίμονο άσθμα: 1,70 ± 0,07mg/dL (45%) και σοβαρό επίμονο άσθμα: 1.53 ± 0.09mg/dL (31,7%). Αυτά τα δεδομένα δείχνουν ότι τα επίπεδα μαγνησίου και 25(ΟΗ)D στον ορό μειώνονται με την αύξηση της σοβαρότητας της νόσου. Τα επίπεδα τους είναι υψηλότερα σε ήπια μορφή άσθματος, ενώ είναι χαμηλότερα στο σοβαρό επίμονο άσθμα.
5. Συμπέρασμα
Η ανεπάρκεια της βιταμίνης D επικρατεί στους ασθματικούς ασθενείς. Επιπλέον, η σοβαρότητα, ο κακός έλεγχος του άσθματος και οι συχνές παροξύνσεις σε ασθματικούς ασθενείς σχετίζονται με χαμηλότερα επίπεδα βιταμίνης D και μαγνησίου. Τα επίπεδα 25(OH)D και μαγνησίου μπορούν να χρησιμεύσουν ως δείκτες της σοβαρότητας του άσθματος. Επομένως, τα επίπεδα αυτών των αναλυτών θα πρέπει να παρακολουθούνται σε ασθενείς με άσθμα και θα πρέπει να διορθώνονται εάν ανευρεθούν χαμηλά επίπεδα.
ΒΙΒΛΙΟΓΡΑΦΙΑ
- [1] R. Agarwal, S. Dhooria, A. N. Aggarwal et al., “Guidelines for diagnosis and management of bronchial asthma: joint ICS/NCCP (I) recommendations,” Lung India, vol. 32, no. 7, S3–S42, 2015.
- The Global Asthma Report 2014, Global Asthma Network, Auckland, New Zealand, 2014.
- C. Aranow, “Vitamin D and the immune system,” Journal of Investigative Medicine, vol. 59, no. 6, 881–886, 2011.
- B. Prietl, G. Treiber, T. R. Pieber, and K. Amrein, “Vitamin D and immune function,” Nutrients, vol.5, no. 7, pp. 2502–2521, 2013.
- W. A. Wells, “Curing TB with sunlight,” The Journal of Cell Biology, vol. 172, no. 7, article 958a, 2006.
- A. Bener, M. S. Ehlayel, M. K. Tulic, and Q. Hamid, “Vitamin D deficiency as a strong predictor of asthma in children,” International Archives of Allergy and Immunology, vol. 157, no.2, pp. 168–175, 2012.
- A. A. Ahmad, M. B. Ramadan, Y. Maha, and E. F. Rania, “Assessment of serum magnesium level in patients with bronchial asthma,” Egyptian Journal of Chest Disease and Tuberculosis, vol.64, no.3, 535–539, 2015.
- G. Helmut and W. Christoph, “Magnesium in disease,” Clinical Kidney Journal, vol. 5, no. 1, pp. i25–i38, 2012.
- D. L. Kasper, E. Braunwald, A. S. Fauci, S. L. Hauser, D. L. Longo, and L. Jameson, “Asthma,” in Harrisons Principles of Internal Medicine, A. S. Fauci, Ed., pp. 1596–1599, Mcgraw-Hill Medical, New York, NY, USA, 17th edition, 2008.
- X. Deng, Y. Song, J. E. Manson et al., “Magnesium, vitamin D status and mortality: results from US National Health and Nutrition Examination Survey (NHANES) 2001 to 2006 and NHANES III,” BMC Medicine, vol. 11, no. 1, article 187, 2013.
- T. O. Carpenter, M. C. DeLucia, J. H. Zhang et al., “A randomized controlled study of effects of dietary magnesium oxide supplementation on bone mineral content in healthy girls,” The Journal of Clinical Endocrinology & Metabolism, vol. 91, no. 12, 4866–4872, 2006.
- Global Initiative for Asthma, Global Strategy for Asthma Management and Prevention, 2016, http://www.ginasthma.org.
- Q. J. Khan and C. J. Fabian, “How I treat vitamin D deficiency,” Journal of Oncology Practice, vol. 6, no. 2, pp. 97–101, 2010.
- R. Kuriacose and K. E. Olive, “Vitamin D insufficiency/deficiency management,” Southern Medical Journal, vol. 107, no. 2, 66–70, 2014.
- M. Columbo, R. A. Panettieri, and A. S. Rohr, “Asthma in the elderly: a study of the role of vitamin D,” Allergy, Asthma and Clinical Immunology, vol. 10, no. 1, article 48, 2014.
- A. A. Ginde, J. M. Mansbach, and C. A. Camargo Jr., “Association between Serum 25-hydroxyvitamin D level and upper respiratory tract infection in the Third National Health and Nutrition Examination Survey,” Archives of Internal Medicine, vol. 169, no. 4, 384–390, 2009.
- J. M. Brehm, J. C. Celedon, M. E. Soto-Quiros et al., “Serum´ vitamin D levels and markers of severity of childhood asthma in Costa Rica,” American Journal of Respiratory and Critical Care Medicine, vol. 179, no. 9,765–771, 2009.
- E. M. Skobeloff, W. H. Spivey, R. M. McNamara, and L. Greenspon, “Intravenous magnesium sulfate for the treatment of acute asthma in the emergency department,” The Journal of the American Medical Association, vol. 262, no. 9,1210–1213, 1989.
- J. Bodenhamer, R. Bergstrom, D. Brown, P. Gabow, J. A. Marx, and S. R. Lowenstein, “Frequently nebulized ????-agonists for asthma: effects on serum electrolytes,” Annals of Emergency Medicine, vol. 21, no. 11, pp. 1337–1342, 1992.
- A. Zittermann, “Magnesium deficit—overlooked cause of low vitamin D status?” BMC Medicine, vol. 11, no. 1, article 229, 2013.
- M. S. Sandhu and T. B. Casale, “The role of vitamin D in asthma,” Annals of Allergy, Asthma and Immunology, vol. 105, no. 3, 191–199, 2010.











Άφησε σχόλιο