Siu-Hin Wan, Paul M. McKie, and John P. Bois
Department of Cardiovascular Diseases, Mayo Clinic, Rochester, MN, USA
Η καρδιακή ανεπάρκεια με μειωμένο κλάσμα εξώθησης (HFrEF) είναι ένα εξελικτικό κλινικό σύνδρομο που συνοδεύεται συνήθως με τη διαστολή της αριστεράς κοιλίας και χαρακτηρίζεται από μειωμένη καρδιακή παροχή, δευτερογενή πνευμονική και συστηματική φλεβική συμφόρηση και ανεπαρκή παροχή περιφερικού οξυγόνου. Είναι συνηθισμένο αλλά πολύπλοκο και απαιτεί τη σύνταξη κατευθυντήριων οδηγιών βασισμένων σε αποδεικτικά στοιχεία μαζί με ισχυρή κλινική εμπειρία. Ακολουθεί ανασκόπηση μιας περίπτωσης που υπογραμμίζει τις σημαντικές κλινικές εκτιμήσεις στη διάγνωση, την αξιολόγηση και τη διαχείριση της HFrEF που απαντάται στην πράξη. Οι παρεχόμενες επεξηγήσεις αποτελούν το επίκεντρο της σχετικής παθοφυσιολογίας του HFrEF καθώς και λεπτομερείς εξηγήσεις για την ερμηνεία των εξετάσεων τόσο της μη επεμβατικής όσο και της επεμβατικής αξιολόγησης στην καρδιακή ανεπάρκεια. Το παράδειγμα που παρέχεται θα χρησιμεύει ενδεχομένως ως πιθανό σημείο αναφοράς για τους ασκούμενους καθώς και για τους επαγγελματίες της υγειονομικής περίθαλψης για ασθενείς με HFrEF.
1. Εισαγωγή και Επισκόπηση της Νόσου
1.1. Επίπτωση και Αιτιολογία. 5.1 εκατομμύρια Αμερικανοί πάσχουν από καρδιακή ανεπάρκεια με ετήσιες δαπάνες για την υγειονομική περίθαλψη που πλησιάζουν τα 30 δισεκατομμύρια δολάρια1. Η σοβαρότητα της καρδιακής ανεπάρκειας ταξινομείται στα στάδια Α έως D από το American College of Cardiology και την American Heart Association. Η καρδιακή ανεπάρκεια με μειωμένο κλάσμα εξώθησης (HFrEF) είναι ένα κλινικό σύνδρομο που ορίζεται από συστολική δυσλειτουργία με ανεπαρκή αιμάτωση και γενικά σχετίζεται με κλάσμα εξώθησης μικρότερο ή ίσο με 40%. Περίπου οι μισοί ασθενείς με καρδιακή ανεπάρκεια έχουν HFrEF και το ήμισυ εξ αυτών έχουν καρδιακή ανεπάρκεια με διατηρημένο κλάσμα εξώθησης (HFpEF). Η διαφορική διάγνωση για την αιτιολογία της HFrEF είναι ευρεία (Πίνακας 1) με τη στεφανιαία νόσο και την υπέρταση ως τις πιο συχνές αιτίες.
1.2. Παθοφυσιολογία. Η HFrEF προκύπτει από δυσλειτουργία του καρδιακού μυοκυττάρου η οποία οδηγεί σε μειωμένη συστολή. Τα νευροχημικά συστήματα όπως το σύστημα ρενίνης-αγγειοτενσίνης-αλδοστερόνης και το συμπαθητικό νευρικό σύστημα αντισταθμίζονται αυξάνοντας το προφορτίο και τον καρδιακό ρυθμό. Η προκύπτουσα κοιλιακή διαστολή χρησιμεύει για να διατηρεί τον όγκο παλμού και τελικά εξασφαλίζει επαρκή συστηματική διάχυση. Ωστόσο, η χρόνια ενεργοποίηση αυτών των νευροχημικών συστημάτων προδιαθέτει τα επιβιώσαντα μυοκύτταρα σε παθολογική αναδιαμόρφωση και περαιτέρω καρδιακή δυσλειτουργία2. Στα αρχικά στάδια της καρδιακής ανεπάρκειας, το νατριουρητικό πεπτιδικό σύστημα εξουδετερώνει τις επιβλαβείς επιδράσεις της μη προσαρμοστικής νευροχημικής ενεργοποίησης αλλά είναι δυσλειτουργικό στα τελικά στάδια καρδιακής ανεπάρκειας. Τελικά, η καρδιά φτάνει στο όριο της για να αντιρροπήσει και η καρδιακή παροχή δεν μπορεί να καλύψει τη ζήτηση.
2. Κλινική Παρουσίαση
2.1. Ιστορικό. Ένας Αφροαμερικανός άνδρας εβδομήντα τριών ετών με ιστορικό μακροχρόνιας παροξυσμικής κολπικής μαρμαρυγής υπό θεραπεία με βαρφαρίνη, υπέρταση, δυσλιπιδαιμία και χρόνια νεφρική νόσο σταδίου ΙΙΙ (GFR 52 mL / min) παρουσίασε προοδευτική δύσπνοια στην άσκηση προ δύο ετών. Τα συμπτώματα του ασθενούς εμφανίστηκαν αρχικά μετά τη βάδιση δύο μιλίων, αλλά τώρα εμφανίστηκε μετά τη βάδιση από μόνο μισό μίλι. Δεν ανέφερε βήχα, πυρετό, ορθόπνοια, η παροξυσμική νυκτερινή δύσπνοια ή στηθάγχη. Εμφάνισε ίχνη οιδήματος κάτω άκρων και περιστασιακό αίσθημα παλμών.
Δεν είχε γνωστό ιστορικό στεφανιαίας νόσου ή δομικής καρδιοπάθειας. Δεν υπήρχαν υποκείμενες πνευμονικές διαταραχές και δεν ήταν ποτέ καπνιστής. Δεν υπήρχε οικογενειακό ιστορικό καρδιαγγειακής νόσου και ο ασθενής είχε διατηρήσει ένα υγιές σωματικό βάρος και πρόγραμμα άσκησης, αν και τώρα με μειούμενη ανοχή.
Συγκεκριμένα καρδιαγγειακά φάρμακα περιλεάμβαναν βαρφαρίνη για αντιθρομβωτική προφύλαξη, διλτιαζέμη για τη διατήρηση του ελέγχου της καρδιακής συχνότητας και υδροχλωροθειαζίδη για τη διαχείριση της αρτηριακής πίεσης.
| Πίνακας 1: Διαφορική Διάγνωση Αιτιολογίας Καρδιακής Ανεπάρκειας με Μειωμένο Κλάσμα Εξώθησης (HFrEF). |
| Στεφανιαία νόσος Υπέρταση Διαβήτης Ιστορικό μυοκαρδιοπάθειας Μυοκαρδιοπάθεια που προκαλείται από ταχυκαρδία Μολυσματικοί παράγοντες: βακτηριακοί και ιογενείς Διηθητικές διαταραχές Τοξίνες Διατροφικές ανεπάρκειες Διαταραχές ηλεκτρολυτών Αγγειακές διαταραχές κολλαγόνου Ενδοκρινικές και μεταβολικές νόσοι Μυοκαρδιοπάθεια Peripartum Αποφρακτική άπνοια ύπνου Ιδιοπαθείς |
| Mayo Board Review Textbook, Table 93.5, σελίδα 862 |
2.2. Συζήτηση Ιστορικού. Η αρχική διαφορική διάγνωση για αυτή την περίπτωση είναι ευρεία και πρέπει να περιλαμβάνει πνευμονική παθολογία, αποκατάσταση και διάφορες καρδιακές αιτιολογίες.
Οι πιθανές καρδιακές αιτιολογίες περιλαμβάνουν αρρυθμίες, δομικές καρδιακές παθήσεις και στεφανιαία νόσο. Η καρδιακή ανεπάρκεια θα πρέπει να λαμβάνεται υπόψιν διατυπώνει κατά την προσέγγιση της διάγνωσης από τον κλινικό ιατρό. Το κλινικό ιστορικό είναι αξιόλογο για το αμφοτερόπλευρο οίδημα των κάτω άκρων που συνδυάζεται με την δύσπνοια κατά την άσκηση η οποία υποδηλώνει καρδιακή ανεπάρκεια. Το κλινικό ιστορικό είναι αρνητικό για την ορθόπνοια και την παροξυσμική νυκτερινή δύσπνοια, δύο συγκεκριμένα ευρήματα στην καρδιακή ανεπάρκεια σε 81% και 80%, αντίστοιχα. Ωστόσο, με μια ευαισθησία που κυμαίνεται από 20% έως 30%, η έλλειψη ορθόπνοιας ή παροξυσμικής δύσπνοιας δεν αποκλείει την πιθανότητα καρδιακής ανεπάρκεια3. Τέλος, δεδομένης της ηλικίας, του φύλου, της δυσλιπιδαιμίας και της χρόνιας νεφρικής νόσου, η στεφανιαία νόσος θα πρέπει να λαμβάνεται υπόψιν στην διαφορική διάγνωση της δύσπνοια κατά την άσκηση ως πιθανό αγγειακό ισοδύναμο. Ο κλινικός ιατρός θα πρέπει να γνωρίζει ότι η νεφρική νόσος μεταξύ των Αφρο-Αμερικανών σχεδόν διπλασιάζει τον κίνδυνο εμφάνισης στεφανιαίας αρτηριακής νόσου.
Οι σχετικές απόψεις του ιστορικού, όπως η διατήρηση ενός υγιούς σωματικού βάρους και κατάλληλων επιπέδων σωματικής δραστηριότητας, μειώνουν την πιθανότητα ότι η απλή αποκατάσταση ευθύνεται για την παρουσία του ασθενούς. Επιπλέον, η έλλειψη καπνίσματος σε συνδυασμό με ουδεμία προηγούμενη γνωστή πνευμονική νόσο μειώνει την πιθανότητα της πρωτογενούς πνευμονικής διαταραχής ως υπεύθυνη για την δύσπνοια του ασθενούς κατά την άσκηση.
2.3. Φυσική Εξέταση. Κατά την αρχική παρουσίαση, ο ασθενής εμφανίστηκε ήρεμος και καλή θρέψη. Ο καρδιακός ρυθμός ήταν ρυθμικός με 77 σφύξεις/λεπτό, η πίεση του αίματος ήταν 125/82mmHg, ο αναπνευστικός ρυθμός ήταν 12 αναπνοές/λεπτό με κορεσμό οξυγόνου 96% στον αέρα δωματίου και θερμοκρασία 36,90C. Ο δείκτης μάζας σώματος καταγράφηκε στα 25,85 kg/m2.
Κατά την επισκόπηση, υπήρχε φλεβική διάταση στη γωνία της κάτω γνάθου (~ 12 cm H2O). Η παλμική απόκλιση αποκάλυψε ότι η καρδιακή κορυφή ήταν τόσο μεγεθυμένη όσο και μετατοπισμένη πλευρικά στη μεσοσπονδυλική γραμμή. Δεν υπήρξε παραστερνική ανέλκυση άνοδος και ο δεύτερος ήχος της καρδίας δεν ήταν αντιληπτός. Κατά την ακρόαση της καρδίας βρέθηκε ένας φυσιολογικός πρώτος και ένας έντονος δεύτερος καρδιακός ήχος με ευρύ διαχωρισμό που αυξήθηκε κατά τη διάρκεια της εισπνοής αλλά υπήρχε σε όλο τον αναπνευστικό κύκλο. Στην κορυφή παρατηρήθηκε ένα ολοσυστολικό φύσημα βαθμού ΙΙ / VI. Το φύσημα δεν αντανακλούσε ούτε μεταβάλλετο σε ένταση με την αναπνοή ή προκλητά μέτρα όπως ο χειρισμός Valsalva ή ο ελιγμός χειρός.
Η εξέταση της κοιλίας δεν έδειξε ενδείξεις ηπατομεγαλίας ή ασκίτου. Το ήπαρ δεν ήταν ψηλαφητό και δεν μπορούσε να προκληθεί ηπατοσφαγιτιδική παλινδρόμηση. Η εξέταση των άκρων δεν έδειξε σημεία συσπάσεων, σκλήρυνσης, φλεγμονής των αρθρώσεων ή εξανθήματος. Σημειώθηκε Βαθμού II εντύπωμα οιδήματος ακριβώς κάτω από τα γόνατα αμφοτερόπλευρα. Οι οπίσθιες σφύξεις της κνήμης και της ράχεος του ποδός ήταν εύκολα ορατοί αμφίπλευρα. Η δερματική και η αρθρική εξέταση δεν διαπίστωσε ένδειξη εξάνθημα, αλλοιώσεις ή οίδημα των αρθρώσεων.
Η πνευμονική εξέταση δεν διαπίστωσε αμβλύτητα κατά την επίκρουση και τα πνευμονικά πεδία ήταν καθαρά χωρίς καμία ανίχνευση ρόγχων ή ελάττωση των αναπνευστικών ήχων κατά την αναπνοή. Δεν διαπιστώθηκε λεμφαδενοπάθεια κατά την ψηλάφηση. Η εξέταση του στόματος αποκάλυψε υγρές βλεννώδεις μεμβράνες χωρίς άλλες ανωμαλίες.
2.4. Ερμηνεία Φυσικής Εξέτασης. Υπάρχουν διάφορα βασικά στοιχεία στη φυσική εξέταση που βοηθούν στην εστίαση της διαφορικής διάγνωσης. Το πιο σημαντικό είναι ότι η καρδιακή εξέταση υποδηλώνει μια διασταλτική μυοκαρδιοπάθεια, λαμβάνοντας υπόψιν τα ευρήματα μιας διογκομένης και παρεκτοπισμένης καρδιακής κορυφής.
Ο προεξέχων δεύτερος ήχος της καρδιάς σε συνδυασμό με την επίμονη διάσπαση υποδηλώνει πνευμονική υπέρταση. Ο έντονος S2 στην πνευμονική υπέρταση δημιουργείται από την αυξημένη πνευμονική πίεση που αποκλείει την πνευμονική βαλβίδα. Υπάρχει παρατεταμένος διαχωρισμός του δεύτερου ήχου της καρδιάς που αυξάνεται με την εκπνοή. Η αυξημένη πνευμονική πίεση παρατείνει τον χρόνο εξώθησης της δεξιάς κοιλίας, γεγονός που καθυστερεί το κλείσιμο της πνευμονικής βαλβίδας με αποτέλεσμα την αύξηση του διαχωρισμού του δεύτερου ήχου της καρδίας. Η αυξημένη επαναφορά φλεβικού αίματος στη δεξιά κοιλία κατά τη διάρκεια της εισπνοής αυξάνει περαιτέρω τον χρόνο εξώθησης της δεξιάς κοιλίας, οδηγώντας στην ακρόαση διαρκούς διαχωρισμού. Ο παρατεταμένος διαχωρισμός μπορεί επίσης να βρεθεί σε άλλες καταστάσεις που καθυστερούν την εκκένωση της δεξιάς κοιλίας κατά τη διάρκεια της συστολής, όπως ο αποκλεισμός του δεξιού σκέλους.
Η θέση, ο συγχρονισμός και η φύση του βαθμού ΙΙ / VI ολοσυστολικού φυσήματος στην κορυφή είναι σύμφωνες με την μιτροειδής παλινδρόμηση. Το μιτροειδικό φύσημα συνήθως εκτιμάται καλύτερα στην καρδιακή κορυφή και συχνά είναι παρόν σε όλη τη συστολή. Σε σοβαρή μιτροειδική παλινδρόμηση, το φύσημα θα αυξηθεί με αυξημένο φορτίο και θα μειωθεί με μειωμένο προφορτίο. Ωστόσο, αυτό το φύσημα δεν είναι μαλακό στην έντασή του, υποδηλώνοντας ήπια ή ήπια έως μέτρια παλινδρόμηση.
Ένας προτεινόμενος μηχανισμός για τη μιτροειδική παλινδρόμηση με βάση τα ευρήματα της φυσικής εξέτασης είναι η διαστολή του δακτυλίου της μιτροειδούς βαλβίδας με αποτέλεσμα την μειωμένη ικανότητά της για κλείσιμο με αποτέλεσμα τη δευτερογενή μιτροειδική παλινδρόμηση. Μια ανωμαλία της ίδιας της βαλβίδας που είναι γνωστή ως πρωτογενής μιτροειδική παλινδρόμηση μπορεί να παρατηρηθεί σε νόσους όπως η πρόπτωση της μιτροειδούς βαλβίδας. Εντούτοις, ένα φύσημα ήχου της πρόπτωσης της μιτροειδούς βαλβίδας θα περιλαμβάνει συχνά ένα ακουστικό συστολικό κλικ, το οποίο αντιστοιχεί στην πρόπτωση της βαλβίδας ακολουθούμενη από ένα φύσημα. Επιπλέον, οι προκλητικοί ελιγμοί που αυξάνουν την υπερφόρτωση ή μειώνουν το προφορτίο θα πρέπει να εντείνουν το ρήγμα της πρόπτωσης της μιτροειδούς βαλβίδας, που δεν εκτιμήθηκαν σε αυτή την περίπτωση.
Με την υποψία της διατατικής μυοκαρδιοπάθειας καθώς και της πνευμονικής υπέρτασης, ο επόμενος στόχος είναι να καθοριστεί αν άλλα ευρήματα εξέτασης υποδηλώνουν το βαθμό της φυσιολογικής αποκατάστασης του ασθενούς. Ο σφαγιτιδικός φλεβικός παλμός διευρύνθηκε και το 2+ περιφερικό οίδημα εκτιμήθηκε, υποδηλώνοντας μέτρια υπερφόρτωση ενδοαγγειακού όγκου. Ενώ τα πεδία των πνευμόνων ήταν κάθαρα κατά την ακρόαση, αυτό το εύρημα μπορεί να είναι λιγότερο ευαίσθητο στον προσδιορισμό της κλινικής κατάστασης του όγκου σε ασθενείς με χρόνια καρδιακή ανεπάρκεια, δεδομένης της ικανότητας του πνευμονικού λεμφικού συστήματος να διαστέλλεται με την πάροδο του χρόνου και να δέχεται την περίσσεια του υγρού.
Δεν υπάρχει εξέταση για να υποδηλώσει μια συστηματική αιτία της υποψίας διατατικής μυοκαρδιοπάθειας. Για παράδειγμα, δεν υπήρχε μακρογλωσσία που να εκτιμάται στην αμυλοείδωση, καμία αναφορά στον υπογοναδισμό που σχετίζεται με αιμοχρωμάτωση και καμία δερματική ανωμαλία όπως το οζώδες ερύθημα που παρατηρείται σε ένα τέταρτο των ασθενών με σαρκοείδωση.
Όσον αφορά την υποψία πνευμονικής υπέρτασης, υπάρχουν αρκετά βασικά ευρήματα εξέτασης που αποκαλύπτουν την κατάσταση της δεξιάς κοιλίας καθώς και πιθανές ενδείξεις ως προς μια υποκείμενη αιτιολογία. Πρώτον, ο ασθενής είχε κατάλληλο κορεσμό οξυγόνου στον αέρα του δωματίου και δεν υπήρχαν ενδείξεις περιφερικής κυάνωσης. Στη συνέχεια, διαπιστώθηκε στην εξέταση ότι δεν εκτιμήθηκε η παραστερνική ανύψωση. Ενώ η παρουσία της δεξιάς κοιλιακής ανύψωσης είναι ειδική για την υπερτροφία της δεξιάς κοιλίας (95,7%), δεν είναι ευαίσθητη (37,5%) και επομένως δεν μπορεί να αποκλειστεί η υπερτροφία της δεξιάς κοιλίας από την απουσία αυτού του ευρήματος4. Παρομοίως, η ηπατοσφαγιτιδική διάταση, η οποία δεν εκτιμήθηκε κατά την εξέταση, είναι ειδική (100%) αλλά όχι ιδιαίτερα ευαίσθητη (66%) για τη διάγνωση της καρδιακής ανεπάρκειας της δεξιάς κοιλίας5. Η εξέταση περιλαμβάνει ορισμένα αρνητικά στοιχεία ως προς την πιθανή αιτιολογία της πνευμονικής υπέρτασης. Για παραδείγμα, η αναφερθείσα κύφωση ήταν ήπια και συνεπώς ήταν απίθανο να προκαλέσει περιοριστική αποφρακτική νόσο. Η ακρόαση των πεδίων των πνευμόνων δεν έδειξε τυχόν ρόγχους που θα συνδέονταν με διάμεση πνευμονοπάθεια ούτε υπήρχαν ενδείξεις περιφερικής πληκτροδακτυλίας. Ο ασθενής δεν έχει ενδείξεις αρθρικής φλεγμονής ή δερματικού εξανθήματος που θα υποδήλωναν μια υποκείμενη αυτοάνοση νόσο που θα είχε ως αποτέλεσμα την πνευμονική υπέρταση. Μια σημαντική θετική συνάφεια είναι η ανακάλυψη διαστολής της αριστεράς κοιλίας που αυξάνει την υποψία μιας αυξημένης ενδοδιαστολικής πίεσης της αριστεράς κοιλίας που συμβάλλει σε αυξημένες πιέσεις στο πνευμονικό αγγειακό σύστημα (Πίνακας 2).
2.5. Περίληψη Παρουσίασης Περιπτώσεως. Ένας άνδρας ηλικίας εβδομήντα τριών ετών με ιστορικό παροξυσμικής κολπικής μαρμαρυγής, δυσλιπιδαιμίας και χρόνιας νεφρικής νόσου, σταδίου ΙΙΙ, παρουσίασε προοδευτική δύσπνοια. Η διαφορική διάγνωση ήταν ευρεία και περιελάμβανε πνευμονικές διαταραχές όπως περιοριστική ή αποφρακτική πνευμονοπάθεια, αποκατάσταση και ποικίλες καρδιακές παθήσεις όπως στεφανιαία νόσο, καρδιακή ανεπάρκεια ή επακόλουθα κολπικής μαρμαρυγής όπως ο κακός έλεγχος του καρδιακού ρυθμού.
Η κλινική εξέταση περιόρισε τη διαφορική διάγνωση με τα ευρήματα που υποδηλώνουν μια διαταραγμένη μυοκαρδιοπάθεια με ήπια έως μέτρια δευτερογενή μιτροειδική παλινδρόμηση και πνευμονική υπέρταση. Η επακόλουθη μη επεμβατική αξιολόγηση πρέπει να επικεντρωθεί στην επιβεβαίωση αυτών των κλινικών υποψιών και στον καθορισμό συγκεκριμένων αιτιολογιών για την καθοδήγηση των θεραπευτικών στρατηγικών.
2.6. Μη Επεμβατική Αξιολόγηση. Η εργαστηριακή αξιολόγηση ήταν η ακόλουθη (ευρήματα εκτός των κανονικών ορίων):
Αιμοσφαιρίνη: 13,3 (13,5-17,5g/dL)
Λευκοκύτταρα: 9,6 χ 109 (3,5-10,5 × 109 / L)
Μέσος όγκος κορμού (Mean corpuscular volume) : 83 (81,2-95,1 fL)
Αριθμός αιμοπεταλίων: 204 × 109 (150-450 × 109 / L)
Κρεατινίνη: 1,6 (0,8-1,3 mg/dL)
Νάτριο: 143 (135-145 mmol L)
Αζώτο ουρίας αίματος (BUN): 29 (8-24 mg/dL)
Κάλιο: 4.2 (3.6-5.2 mmol/L)
Αλκαλική φωσφατάση: 125 (45-115 U/L)
Ασπαρτική αμινοτρανσφεράση (AST): 29 (8-48 U/L)
Ουρικό οξύ: 25 (3.7-8.0 mmol/L)
Θυρεοειδοτρόπος ορμόνη (TSH): 2.0 (0.3-5.0 MIU/L)
Αμινο-τερματικό νατριουριτικό πεπτίδιο τύπου proB (NTproBNP): 9245 (<107 pg/mL)
Ολικός σίδηρος: 114 (50-150 mcg/dL)
Συνολική ικανότητα σύνδεσης σιδήρου (TIBC): 287 (250-400 mcg/dL)
Φερριτίνη: 112 (24-336 ng/ml)
Συνολική χοληστερόλη: 208 (<200 mg/dL)
Τριγλυκερίδια: 71 (<150 mg/dL)
Λιποπρωτεΐνη υψηλής πυκνότητας (HDL): 59 (> 40 mg/dL)
Λιποπρωτεΐνη χαμηλής πυκνότητας (LDL): 125 (<130 mg/dL)
Ηλεκτροφόρηση πρωτεϊνών ορού και ούρων (SPEP και UPEP) αρνητική για μονοκλωνική γαμοπάθεια
Πίνακας 2: Φυσικά Ευρήματα Εξέτασης Πνευμονικής Υπέρτασης.
| Σημεία | Επιπτώσεις |
| Κεντρική κυάνωση Πληκτροδακτυλία Καρδιακή ακρόαση: Φύσημα, έντονος ήχος, καλπαστικός ρυθμός Ρόγχοι, αμβλύτητα, μειωμένοι ήχοι αναπνοής Ευκρινείς ρόγχοι, χρήση επικουρικών μυών, συριγμός και παρατεταμένη εκπνοή, παραγωγικός βήχας Παχυσαρκία, κυφοσκολίωση, διογκομένες αμυγδαλές Πληκτροδακτυλία, αρθρίτιδα, εξάνθημα Περιφερική φλεβική ανεπάρκεια ή απόφραξη | Υποξαιμία, δεξιά προς τα αριστερά διαφυγή Συγγενείς καρδιακές παθήσεις, πνευμονική νευροπάθεια Συγγενής ή επίκτητη νόσος της καρδιάς ή της βαλβίδας Πνευμονική συμφόρηση ή υγρό Πνευμονική παρεγχυματική νόσος Διαταραχή ξαερισμού Διαταραχή του συνδετικού ιστού Φλεβική θρόμβωση |
Mayo Board Review Table 79.3 (σελ. 736).
Το ΗΚΓ έδειξε έναν φυσιολογικό κολπικό ρυθμό, υπερτροφία της αριστεράς κοιλίας και μη ειδικές μεταβολές του ST (Σχήμα 1 (a)). Μια εικοσιτετράωρη συσκευή παρακολούθησης της αρτηριακής πίεσης τεκμηρίωσε μια μέση αρτηριακή πίεση 139/82mmHg με μέγιστη αρτηριακή πίεση 180/118mmHg. Το Holter των περισσοτέρων ασθενών παρακολούθησε τον φλεβοκομβικό ρυθμό με έναν καρδιακό ρυθμό που κυμαινόταν από 53 έως 123 παλμούς/λεπτό με μέσο όρο καρδιακού ρυθμού 70 παλμούς/λεπτό. Δύο-τρεις έως τέσσερις παλμοί κοιλιακής ταχυκαρδίας σημειώθηκαν με ρυθμό αιχμής 132 παλμούς/λεπτό. Δεν παρατηρήθηκαν άλλες πρόωρες κοιλιακές ή υπερκοιλιακές συστολές και ο ασθενής παρέμεινε ασυμπτωματικός κατά την αξιολόγηση Holter.
Η προσθιοπίσθια και πλάγια ακτινογραφία θώρακος έδειξε ήπια καρδιομεγαλία, μια ελικοειδή αορτή και μια ήπια διάμεση προεξοχή μεγαλύτερη στη δεξιά πνευμονική βάση (Εικόνα 1 (b)). Η διαθωρακική υπερηχοκαρδιογραφία έδειξε σοβαρή διάταση της αριστεράς κοιλίας (δισδιάστατη τελική διαστολική διάσταση 64 mm (αναμενόμενη 37-51) και τελική συστολική διάσταση 54 mm (αναμενόμενη 22-34)) με κλάσμα εξώθησης 39% όταν υπολογίστηκε με διπλούς όγκους (Σχήματα 2 (α) και 2 (β)). Το πάχος του οπίσθιου τοιχώματος μετρήθηκε στα 12 mm και ο δείκτης μάζας της αριστεράς κοιλίας ήταν 185 g/m2. Εκτιμήθηκε επίσης η γενικευμένη υποκινητικότητα της αριστεράς κοιλίας. Παρατηρήθηκε ελαφρά ήπια καταστολή της κεντρικής μιτροειδούς βαλβίδας (αποτελεσματικό ανακουφιστικό στόμιο 0,16 cm2 με όγκο επαναρροής 34cc από την εγγύτερη περιοχή επιφάνειας ισοβλεψίας (PISA)) και ήταν πιθανώς δευτερογενής σε διαστολή του μιτροειδούς δακτυλίου. Η αυξημένη πίεση πλήρωσης της αριστεράς κοιλίας αναφέρθηκε με αναλογία Ε προς Α 0,67 και μέση Ε προς e’ αναλογία 20. Στην περιοριστική φυσιολογία, με αυξημένες αριστερές κολπικές πιέσεις, η πρώιμη διαστολική πλήρωση αναμένεται να συμβεί άμεσα μετά τη διάνοιξη της μιτροειδούς βαλβίδας, οδηγώντας έτσι σε έναν απότομο χρόνο επιβράδυνσης. Η αξιολόγηση της δεξιάς κοιλίας αποκάλυψε φυσιολογικό μέγεθος και λειτουργία της δεξιάς κοιλίας με εκτιμώμενη συστολική αρτηριακή πίεση δεξιάς κοιλίας 39 mmHg βασισμένη στην κορυφαία τριγλώχινα παλίνδρομο ταχύτητα 2,90 m/sec και κανφυσιολογικήονική σε μέγεθος κάτω κοίλη φλέβα η οποία κατέρρευσε περισσότερο από 50% τη διάμετρο με την εισπνοή (Σχήματα 3(a) -3(c)).
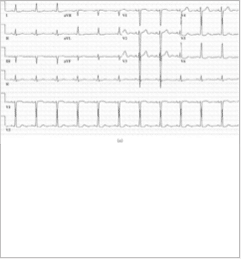
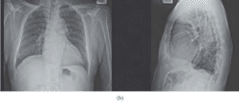
Σχήμα 1: (α) Ηλεκτροκαρδιογράφημα (12-Επαγωγών): ΗΚΓ που δείχνει φλεβοκομβικό ρυθμό με υπερτροφία της αριστεράς κοιλίας με βάση τα κριτήρια τάσης Cornell. (β) Προσθιοπίσθια και πλάγια ακτινογραφία θώρακος: ήπια καρδιομεγαλία, ελικοειδής αορτή και ήπια διάμεση προεξοχή μεγαλύτερη στη δεξιά πνευμονική βάση.
Σχήμα 2: Διαθωρακικό υπερηχοκαρδιογράφημα για το μέγεθος και λειτουργία της καρδίας. (a) Παραστερνικός άξονας που παρουσιάζει σοβαρή διαστολή (τελοδιαστολική διάσταση 64mm) με φυσιολογικό πρόσθιο διάφραγμα και κατώτερο πλευρικό πάχος τοιχώματος (9 και 12mm αντίστοιχα). (β) Παρόμοια εικόνα που δεικνύει αυξημένη τελική συστολική διάσταση (57mm) σε συμφωνία με το μειωμένο κλάσμα εξώθησης.
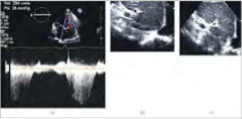
Εικόνα 3: Διαθωρακικό υπερηχοκαρδιογράφημα για τον προσδιορισμό της συστολικής πίεσης της δεξιάς κοιλίας (RVSP). (α) Μέτρηση Doppler με συνεχή κύμα μέγιστης τρικυκλικής ταχύτητας επαναφοράς 2,9m/s. Η συστολική πίεση της δεξιάς κοιλίας υπολογίζεται μέσω της τροποποιημένης εξίσωσης Bernoulli ΔPTV= 4 × (VTR)2 ή ΔPTV = 4 × (2,9m/s)2 = 4mmHg. Μικρή κατώτερη πύλη κατά την εκπνοή (β) που καταρρέει εντελώς από την εισπνοή (γ), συνάδει με μια μέση πίεση στον δεξιό κόλπο 5mmHg.
CMJ 2019 JULY-AUGUST-SEPTEMBER TELIKOOOO:Layout 1.qxd
Σχήμα 1: (α) Ηλεκτροκαρδιογράφημα (12-Επαγωγών): ΗΚΓ που δεί- χνει φλεβοκομβικό ρυθμό με υπερτροφία της αριστεράς κοιλίας με βάση τα κριτήρια τάσης Cornell. (β) Προσθιοπίσθια και πλάγια ακτι- νογραφία θώρακος: ήπια καρδιομεγαλία, ελικοειδής αορτή και ήπια διάμεση προεξοχή μεγαλύτερη στη δεξιά πνευμονική βάση.
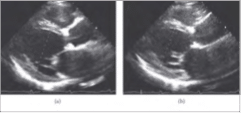
Σχήμα 2: Διαθωρακικό υπερηχοκαρδιογράφημα για το μέγεθος και λειτουργία της καρδίας. (a) Παραστερνικός άξονας που παρουσιάζει σοβαρή διαστολή (τελοδιαστολική διάσταση 64mm) με φυσιολογικό πρόσθιο διάφραγμα και κατώτερο πλευρικό πάχος τοιχώματος (9 και 12mm αντίστοιχα). (β) Παρόμοια εικόνα που δεικνύει αυξημένη τελική συστολική διάσταση (57mm) σε συμφωνία με το μειωμένο κλάσμα εξώθησης.
2.7. Μη επεμβατική Διαγνωστική Συζήτηση. Η εργαστηριακή αξιολόγηση είναι αξιοσημείωτη για ένα αυξημένο NT- pro BNP το οποίο είναι πιο συχνά αυξημένο στην καρδιακή ανεπάρκεια, αν και η αύξηση μπορεί να παρατηρηθεί σε οποιαδήποτε νόσο με αυξημένη μυοκυτταρική έκταση ή φλεγμονή μυοκυττάρων. Το ιστορικό χρόνιας νεφρικής νόσου επιβεβαιώνεται με υπολογισμένο GFR 52mL/min, σε συμφωνία με τη νόσο σταδίου III. Είναι σημαντικό ότι οι μελέτες της TSH, φερριτίνης ορού και μονοκλωνικών πρωτεϊνών ήταν εντός των φυσιολογικών ορίων, γεγονός που υποδηλώνει ότι οι ανωμαλίες του θυρεοειδούς, η αιμοχρωμάτωση ή η αμυλοείδωση δεν παίζουν κάποιο ρόλο στην κλινική παρουσίαση του ασθενούς. Ωστόσο, αν υπήρχαν συγκεκριμένα ευρήματα σχετικά με την κλινική εξέταση, όπως η νευροπάθεια και η μακρογλλωσία, ή τα ηχοκαρδιογραφικά χαρακτηριστικά, όπως η ομόκεντρη υπερτροφία που θα αφορούσε πιθανή αμυλοείδωση, αυτό θα συνιστούσε την λήψη ιστού για παθολογική διάγνωση.
Το ΗΚΓ υποδηλώνει υπερτροφία της αριστεράς κοιλίας (LVH) με βάση τα κριτήρια τάσης Cornell. Αυτό το κριτήριο συνθέτει το κύμα R στην aVL και το κύμα S στη V3 και εάν είναι μεγαλύτερο από 20mm στις γυναίκες ή 28mm στους άνδρες, υποδηλώνει αριστερά καρδιακή υπερτροφία (ΑΚΥ).
Οι μετρήσεις του ηχοκαρδιογραφήματος μπορούν να χρησιμοποιηθούν για περαιτέρω χαρακτηρισμό της υπερτροφίας του ασθενούς (Σχήμα 4). Το πρώτο σχετικό πάχος τοιχώματος μπορεί να μετρηθεί με την ακόλουθη εξίσωση (όπου το LVEDD είναι ίσο με την τελοδιαστολική διάσταση της αριστεράς κοιλίας):
Σχετικό πάχος τοιχώματος = (2 x πάχος οπισθίου τοιχώματος) / (LVEDD). (1)
Στην παρούσα περίπτωση,
σχετικό πάχος τοιχώματος = (2 x 12mm) / 64mm = 0,375. (2)
Στη συνέχεια, ένα σχετικό πάχος τοιχώματος 0.375 μπορεί να συνδυαστεί με έναν υπολογισμένο δείκτη μάζας της αριστεράς κοιλίας με ηχοκαρδιογράφημα 185g/m2 για να δείξει έκκεντρη υπερτροφία (Σχήμα 4). Μελέτες υποδεικνύουν ότι η εξειδίκευση του τύπου της υπερτροφίας όχι μόνο συσχετίζεται με την υποκείμενη παθοφυσιολογία (ομόκεντρη υπερτροφία που σχετίζεται με υπερφόρτωση πίεσης και έκκεντρη υπερτροφία που σχετίζεται με την υπερφόρτωση όγκου), αλλά έχει επίσης και προγνωστικές εφαρμογές6.
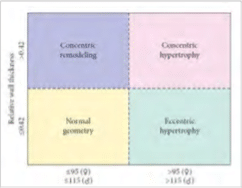
Σχήμα 4: Χαρακτηρισμός της υπερτροφίας της αριστεράς κοιλίας. Το ΗΚΓ του ασθενούς (Σχήμα 2) υποδηλώνει υπερτροφία της αριστερής κοιλίας. Η διαθωρακική ηχοκαρδιογραφική μέτρηση του σχετικού πάχους τοιχώματος (σχετικό πάχος τοιχώματος = (2 × οπίσθιο πάχος τοιχώματος) / (LVEDD) σε συνδυασμό με το δείκτη μάζας της αριστεράς κοιλίας μπορεί να καθορίσει τον συγκεκριμένο τύπο υπερτροφίας. Στην παρούσα περίπτωση, η έκκεντρή υπερτροφία του ασθενούς είναι σύμφωνη με την υπερφόρτωση όγκου δευτερογενώς σε μια διασταλτική μυοκαρδιοπάθεια (Εικόνα από Lang RM, JASE, 2005, 18: 1440-1463).
Τα ηχοκαρδιογραφικά ευρήματα είναι πιο συνεπή με μια διασταλτική μυοκαρδιοπάθεια δεδομένης της ολικής υποκινητικότητας και δεν υπάρχουν 2D ενδείξεις διαταραχών διήθησης όπως η αμυλοείδωση ή η σαρκοείδωση. Η ολική υποκινητικότητα υποδηλώνει μια μη-ισχαιμική αιτιολογία, αλλά δεν μπορεί να αποκλειστεί η ισχαιμική καρδιακή νόσος. Η εύρεση ενός κατεσταλμένου κλάσματος εξώθησης με την παρουσία δύσπνοιας επιβεβαιώνει την HFrEF ως διάγνωση. Ο ασθενής ταξινομείται ως ΑΗΑ σταδίου C με βάση το μειωμένο κλάσμα εξώθησης και τα συμπτώματα (Σχήμα 5).
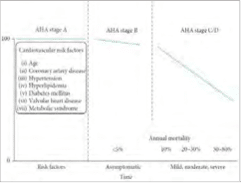
Σχήμα 5: Συσχέτιση σταδίου AHA και επιβίωσης. Σημειώνεται η έντονη επιδείνωση της επιβίωσης μόλις ο ασθενής γίνει συμπτωματικός (ο ασθενής στην τρέχουσα περίπτωση είναι AHA σταδίου C, ήπιος έως μέτριος, με ετήσια θνησιμότητα μεταξύ 10% και 20%) (Mayo Board Review, Εικόνα 93.1 (σελ. 859)).
Η ηχοκαρδιογραφική αξιολόγηση της διαστολικής λειτουργίας υποδεικνύει αυξημένες πιέσεις πλήρωσης. Το Doppler E κύμα, ή πρώιμη διαστολική πλήρωση της αριστερής κοιλίας, αντανακλά την ακτινοβολία πίεσης μεταξύ του αριστερού κόλπου και της αριστεράς κοιλίας7, ενώ ο ιστός Doppler e’ απεικονίζει το ρυθμό χαλάρωσης του μυοκαρδίου8. Η αυξημένη αναλογία E/e΄ δείχνει υψηλές πιέσεις πλήρωσης με μειωμένη χαλάρωση του μυοκαρδιακού ιστού που αντιστοιχεί σε πνευμονική τριχοειδική πίεση ενσφηνώσεως μεγαλύτερη από 12mmHg9. Η αυξημένη αναλογία E/e’ (> 15) είναι ένας ευαίσθητος αλλά όχι ειδικός καθοριστικός παράγοντας για τις πιέσεις πλήρωσης της αριστεράς κοιλίας8. Σε φυσιολογικές καταστάσεις, το πλάγιο e’ είναι μεγαλύτερο από το μέσο e’. Σύμφωνα με τις 2016 ASE Diastolic Function Guidelines, ο μέσος όρος του πλευρικού e’ και του μέσου e’ θα πρέπει να χρησιμοποιείται για τον προσδιορισμό των πιέσεων πλήρωσης της αριστεράς κοιλίας στη ρύθμιση του μειωμένου κλάσματος εξώθησης. Ο υποκείμενος παθοφυσιολογικός μηχανισμός για την HFrEF και τη σχετική διαστολή της LV απεικονίζεται στο Σχήμα 6(a). Μια αρχική προσβολή μειώνει τη συστολική δύναμη της αριστεράς κοιλίας αυξάνοντας τον EDV (άξονα x). Αρχικά, η ενδοδιαστολική πίεση της αριστεράς κοιλίας (LVEDP) (άξονας γ) παραμένει χαμηλή (<15mmHg) και ο ασθενής παραμένει ασυμπτωματικός (AHA σταδίου Β, Σχήμα 5). Ωστόσο, εάν εμφανιστεί προοδευτική διαστολή, το LVEDP αρχίζει να αυξάνεται με επακόλουθη δύσπνοια (AHA σταδίου C). Η περαιτέρω αλλοίωση οδηγεί σε μείωση του όγκου παλμού και αδυναμία διατήρησης της απαραίτητης αιμάτωσης στα τελικά όργανα (AHA σταδίου D).
Η ακτινογραφία θώρακα είναι σύμφωνη με τη διόγκωση της αριστεράς κοιλίας και όχι της δεξιάς κοιλίας, η οποία είναι σύμφωνη με τα ευρήματα της φυσικής εξέτασης. Δεν υπάρχουν ενδείξεις λεμφαδενοπάθειας που να σχετίζονται με τη σαρκοείδωση.
Η περιπατητική πίεση αίματος και οι μετρήσεις Holter παρέχουν σημαντικά δεδομένα. Συγκεκριμένα, ο ασθενής έχει υποβέλτιστο έλεγχο της αρτηριακής πίεσης, αλλά έχει τον κατάλληλο έλεγχο ρυθμού. Επομένως, είναι απίθανο να υποφέρει από καρδιαγγειοπάθεια που προκαλείται από ταχυκαρδία ή πρόωρη κοιλιακή συστολή. Ωστόσο, το μεταφορτίο του είναι σημαντικά αυξημένο, ιδιαίτερα λόγω του μειωμένου κλάσματος εξώθησης, το οποίο μπορεί να παίζει ρόλο στη συμπτωματολογία του.
Όπως υποδεικνύεται από τη φυσική εξέταση, το συστολικό φύσημα ήταν συνεπές με δευτερογενή μιτροειδική παλινδρόμηση λόγω της καλύτερης μιτροειδικής διαστολής. Στο ηχοκαρδιογράφημα, μια μεγάλη κεντρική παλινδρόμηση που συνδέεται με την κεντρική έλλειψη συσσωμάτωσης στη ρύθμιση της αριστεράς κοιλίας και της αριστερής κολπικής διαστολής θα υποστήριζε τη δευτερογενή μιτροειδική παλινδρόμηση. Το μέγεθος και η λειτουργία της δεξιάς κοιλίας βρίσκονται εντός των φυσιολογικών ορίων, τα οποία συμφωνούν με τα ευρήματα της φυσικής εξέτασης χωρίς παραστερνική ανύψωση, αύξηση της σφαγιτιδικής φλεβικής πίεσης, ασκίτη ή ηπατοσφαγιτιδική παλινδρόμηση και ελάχιστο περιφερικό οίδημα. Είναι ενδιαφέρον ότι η συστολική πίεση της δεξιάς κοιλίας είναι μόνο ελαφρώς αυξημένη στα 39mmHg (φυσιολογικά σε κατάσταση ηρεμίας 30mmHg και 40mmHg με άσκηση).
2.8. Πιθανές ” Αντιφατικές” Μετρήσεις. Η συστολική πίεση της δεξιάς κοιλίας, όπως μετριέται με τη μη επεμβατική ηχοκαρδιογραφία Doppler, εμφανίζεται ελαφρώς αυξημένη σε αυτόν τον ασθενή και είναι σε ασυμφωνία με τα ευρήματα της φυσικής εξέτασης ενός έντονου και επίμονα διαιρούμενου δεύτερου καρδιακού ήχου σε όλο το προκάρδιο καθώς και επιδεινούμενης ανοχής στην άσκηση.
Η υπερηχοκαρδιογραφία Doppler αξιολογεί τη συστολική πίεση της δεξιάς κοιλίας (RVSP) χρησιμοποιώντας την τροποποιημένη εξίσωση Bernoulli, η οποία συσχετίζει την μεταβολή της πίεσης με την ταχύτητα μέσω της ακόλουθης εξίσωσης:
ΔΡTV = 4 × (VTR)2, (3)
όπου ΔPTV είναι ίση με το βαθμό της συστολικής πίεσης κατά μήκος της τριγλώχινας βαλβίδας σε mmHg και η VTR είναι η εκτίμηση Doppler της υψηλότερης παλινδρομικής ταχύτητας της τριγλώχινας σε m/s. Στη συνέχεια, το μέγεθος και ο βαθμός κατάρρευσης της κάτω κοίλης φλέβας μπορεί να χρησιμοποιηθεί για την εκτίμηση της σωστής κολπικής πίεσης (RAP). Αυτές οι δύο τιμές μπορούν να συνδυαστούν για την εκτίμηση του RVSP:
RVSP = ΔPTV + RAP. (4)
Αυτή η χρησιμότητα αυτής της μέτρησης εξαρτάται από (1) την απουσία πνευμονικής στένωσης, (2) από την ικανότητα να λαμβάνεται και να μετράται σωστά το σήμα παλινδρομικής ταχύτητας της τριγλώχινας κατά τη διάρκεια της εξέτασης Doppler, και (3) τη σωστή εκτίμηση της πίεσης του δεξιού κόλπου. Είναι σημαντικό ότι, σε σοβαρή παλινδρόμηση της τριγλώχινας, η αξιολόγηση Doppler του RVSP μπορεί να υποτιμηθεί10. Σε αυτά τα συγκεκριμένα σενάρια με τη διαφορά μεταξύ των ευρημάτων των εξετάσεων και της μη επεμβατικής αξιολόγησης, η αξιολόγηση με βάση τον καθετήρα θα αποδώσει μια ακριβέστερη μέτρηση του RVSP.
Προηγούμενες μελέτες έχουν δείξει ότι η συστολική πίεση της δεξιάς κοιλίας με την ηχοκαρδιογραφία μπορεί να επιτευχθεί με ακρίβεια στο 87% των ασθενών. Επιπλέον, η ταυτόχρονη εκτίμηση της συστολικής πίεσης της δεξιάς κοιλίας με επεμβατική αιμοδυναμική και ηχοκαρδιογραφία Doppler εμφανίζει εξαιρετική συσχέτιση (συντελεστής συσχέτισης R = 0,96)11.
Στους ασθενείς εκείνους στους οποίους δεν είναι δυνατόν να ληφθεί ένα παλινδρομικό σήμα της τριγλώχινας, μπορεί να μετρηθεί η τελική διαστολική πνευμονική παλινδρομική ταχύτητα όπως φαίνεται στο Σχήμα 6 (β) (φυσιολογικά λιγότερο από 10mmHg). Για τον υπολογισμό της τελικής διαστολικής πίεσης της πνευμονικής αρτηρίας μπορεί να χρησιμοποιηθεί η ακόλουθη εξίσωση:
PADP = ΔPPVED + RAP, (5)
όπου το PADP υποδεικνύει την τελική διαστολική πνευμονική πίεση, το ΔPPVED ισούται με την κλίση της τελικής διαστολικής πίεσης κατά μήκος της πνευμονικής βαλβίδας και το RAP δεικνύει τη σωστή κολπική πίεση.
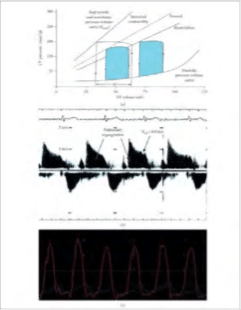
Σχήμα 6: (a) Παθοφυσιολογία της διαστολικής μυοκαρδιοπάθειας. Η αριστερή κοιλία αντιδρά σε μια αρχική προσβολή που μειώνει τη συστολική δύναμη αυξάνοντας τον τελικό διαστολικό όγκο (άξονας x). Αρχικά, η τελική διαστολική πίεση της αριστεράς κοιλίας (άξονας γ) παραμένει χαμηλή (<15mmHg) και ο ασθενής παραμένει ασυμπτωματικός (AHA σταδίου Β). Ωστόσο, εάν εμφανιστεί προοδευτική διαστολή, η τελική διαστολική πίεση αρχίζει να αυξάνεται με την προκύπτουσα δύσπνοια (AHA σταδίου C). Η περαιτέρω αλλοίωση οδηγεί σε μείωση του όγκου του εγκεφαλικού επεισοδίου και αδυναμία διατήρησης της απαραίτητης αιμάτωσης στο τέλος των οργάνων (AHA σταδίου D). (b)Διαθωρακικό ηχοκαρδιογράφημα για τον προσδιορισμό του RVEDP. Τυπικά λαμβάνεται στην παραστερνική άποψη του πλησιέστερου άξονα στην καρδιακή βάση. Το Doppler συνεχούς κύματος του σήματος της πνευμονικής παλινδρόμησης σε συνδυασμό με τη δεξιά κολπική πίεση μπορεί να εκτιμήσει την τελική διαστολική πίεση της πνευμονικής αρτηρίας (PADP) μέσω του PADP = ΔPPVED + RAP. (c) Ενδείξεις αριστεράς κοιλίας (κόκκινο) και πνευμονικής τριχοειδούς σφήνας (PCWP) (πράσινο). Σημειώστε την αυξημένη αριστερή κοιλιακή τελική διαστολική πίεση (λευκό βέλος), αυξημένη PCWP (πράσινο) με προεξέχον κύμα “v” (μπλε βέλος).
3. Επεμβατική Αξιολόγηση
Πότε ενδείκνυται η επεμβατική αξιολόγηση για την HFrEF; Η αρχική επεμβατική αιμοδυναμική αξιολόγηση του περιπατητικού ασθενούς με καρδιακή ανεπάρκεια μπορεί να περιλαμβάνει τα ακόλουθα12:
- Μια στεφανιαία αγγειογραφία για τον προσδιορισμό του βαθμού της στεφανιαίας αθηροσκλήρωσης και της πιθανότητας ισχαιμικής μυοκαρδιοπάθειας ως υποκείμενη αιτιολογία για τη συστολική καρδιακή ανεπάρκεια (Επίπεδο IIc).
- Μια ενδομυοκαρδιακή βιοψία όταν υπάρχει “υποψία ειδικής διάγνωσης που θα επηρέαζε τη θεραπεία” (Επίπεδο IIc). Η ενδομυοκαρδιακή βιοψία ρουτίνας δεν θα πρέπει να διεξάγεται συνήθως σε όλους τους ασθενείς με καρδιακή ανεπάρκεια (Επίπεδο III).
- Αιμοδυναμική αξιολόγηση όταν η συστηματική ή πνευμονική αγγειακή αντίσταση είναι αμφίβολη (Επίπεδο IIc).
Η επεμβατική αξιολόγηση για την επιβεβαίωση της αυξημένης LVEDP και της προκύπτουσας πνευμονικής υπέρτασης τύπου ΙΙ αποτελεί σύσταση της κατηγορίας ΙΙβ από την ACC / AHA12 και την Ευρωπαϊκή Εταιρεία Καρδιολογίας13. Κάποιος θα μπορούσε να υποστηρίξει στην περίπτωση αυτή ότι η υπερηχοκαρδιογραφία του υπερυψωμένου E / e ‘σε Doppler σε συνδυασμό με την υποκείμενη μυοκαρδιοπάθεια ήδη υποδηλώνει αυξημένες πιέσεις πλήρωσης της αριστεράς κοιλίας στο τέλος της διαστολικής φάσης και ότι η θεραπεία πρέπει να αρχίσει χωρίς την ανάγκη περαιτέρω επιβεβαίωσης της διάγνωσης με καθετηριασμό.
Ωστόσο, στην παρούσα περίπτωση, η επεμβατική αιμοδυναμική αξιολόγηση θα διευκρινίσει τόσο τη σοβαρότητα όσο και τη φύση της πνευμονικής υπέρτασης, θα προβλέψει την ανταπόκριση στην παρέμβαση των φαρμάκων και θα βοηθήσει στον καθορισμό της πρόγνωσης. Επίσης, η αγγειογραφία μπορεί να αποκλείσει το CAD ως υποκείμενο μηχανισμό της καρδιακής ανεπάρκειας.
Όσον αφορά τη σοβαρότητα του PH, υπάρχει διαφορά μεταξύ των ευρημάτων της φυσικής εξέτασης ενός προεξάχοντος δεύτερου καρδιακού ήχου ο οποίος είναι διευρυμένος και της ήπιας αύξησης της συστολικής πίεσης της δεξιάς κοιλίας στην υπερηχοκαρδιογραφία Doppler. Η μέτρηση της συστολικής πίεσης της δεξιάς κοιλίας κατά τη διάρκεια του καρδιακού καθετηριασμού θα βοηθήσει στην αποσαφήνιση της σοβαρότητας της πνευμονικής υπέρτασης. Επιπλέον, η μέτρηση της πίεσης ενσφηνώσεως (PCWP) και της διαπνευμονικής κλίσης (TPG), η οποία θα περιγραφεί λεπτομερέστερα στις επόμενες ενότητες, θα καθορίσει από ποιο τύπο ΡΗ πάσχει ο ασθενής (συζητείται στα επόμενα κεφάλαια). Επιπλέον, η μέτρηση της σοβαρότητας της πνευμονικής υπέρτασης με τεκμηρίωση της διαπνευμονικής κλίσης και της πνευμονικής αγγειακής αντίστασης θα βοηθήσει στην αξιολόγηση της πρόγνωσης13. Τέλος, ο καρδιακός καθετηριασμός μπορεί να αποδείξει εάν η οξεία μετεγχειρητική μείωση μειώνει σημαντικά την TPR η οποία μπορεί επίσης να επηρεάσει την πρόγνωση, ιδιαίτερα σε υποψήφιους για μεταμόσχευση καρδιάς13.
Ποιες δοκιμές θα πρέπει να πραγματοποιηθούν σε επεμβατικό καρδιακό καθετηριασμό;
Προσεγγίζοντας την περίπτωση αυτή, ποιες δοκιμές θα επιλέγατε από τις ακόλουθες επιλογές;
[X] Αξιολόγηση της δεξιάς πίεσης της καρδιάς (ΡΑ), πίεση της δεξιάς κοιλίας (RV), πνευμονικής αρτηρίας (ΡΑ) και πιέσεις πνευμονικής τριχοειδικής ενσφηνώσεως (PCW) [X] Πλήρης φάση κορεσμού (περιλαμβανομένης της περιφερικής, κάτω κοίλης φλέβας (IVC), άνω κοίλης φλέβας (SVC) και αρτηριακών μέτρων) [X] Αποκλεισμός των καρδιακών αποδόσεων [_] Θερμοδιάχυση των καρδιακών αποδόσεων [_] Αξιολόγηση πίεσης της αριστεράς κοιλίας (retraortic) [_] Αξιολόγηση πίεσης αριστερού κολπικού (LA) (διαφραγματικός) [X] Μελέτη φαρμάκων: πνευμονικά έναντι συστηματικών αγγειοδιασταλτικών [_] Πρόκληση ενδοφλεβίων υγρών [_] Μελέτη άσκησης [X] Στεφανιαία αγγειογραφία [_] Μελέτη στεφανιαίων αγγειόσπασμων [_] Κοιλιακή κοιλιογραφία [_] Καμπύλες χρωμάτων διπλής δειγματοληψίας [_] Άλλοι χειρισμοί3.1. Αξιολόγηση Επεμβατικού Σχεδιασμού. Υπάρχουν δύο κύριοι στόχοι για την επεμβατική εκτίμηση της υπόθεσης αυτής. Πρώτον, πρέπει να διεξαχθεί διαγνωστική στεφανιαία αγγειογραφία για να εκτιμηθεί η παρουσία και η έκταση της στεφανιαίας αθηροσκλήρωσης. Αυτό θα βοηθήσει να καθοριστεί εάν η διασταλτική μυοκαρδιοπάθεια του ασθενούς είναι ισχαιμική. Μετά την ολοκλήρωση του στεφανιαίου αγγειογράμματος η αορτή μπορεί να διασταυρωθεί με ανάδρομο τρόπο για να εκτιμηθεί η τελική διαστολική πίεση της αριστεράς κοιλίας.
Ο δεύτερος στόχος είναι να επιβεβαιώσουμε και να καθορίσουμε περαιτέρω το SVR και την παρουσία της πνευμονικής υπέρτασης και τον τρόπο με τον οποίο ανταποκρίνονται στην παρέμβαση των φαρμάκων. Για αυτό το τμήμα της μελέτης, θα πρέπει να διεξάγεται καθετηριασμός της δεξιάς καρδίας για την εκτίμηση της πίεσης του δεξιού κόλπου, της δεξιάς κοιλίας, της πνευμονικής αρτηρίας και της πνευμονικής τριχοειδικής ενσφηνώσεως. Οι εκτιμήσεις αυτές θα επιτρέψουν τον υπολογισμό του TPG ο οποίος παρουσιάζεται κατωτέρω. Επιπλέον, κατά τη διάρκεια του καθετηριασμού της δεξιάς καρδίας, θα πρέπει να γίνει μέτρηση του κορεσμού του μεικτού φλεβικού αίματος και του αρτηριακού κορεσμού καθώς και μέτρηση της κατανάλωσης οξυγόνου έτσι ώστε η καρδιακή παροχή να μπορεί να υπολογιστεί μέσω της εξίσωσης Fick και συνεπακόλουθα του υπολογισμού της πνευμονικής αγγειακής αντίστασης (PVR).
Εάν η PCWP του ασθενούς είναι αυξημένη όπως υποπτεύεται, τότε το τελικό βήμα θα είναι να προσδιοριστεί η ανταπόκριση σε θεραπεία οξείας συστηματικής αρτηριακής αγγειοδιαστολής όπως είναι το νιτροπρουσσίδιο. Η παρουσία ή η απουσία μιας ελάττωσης της πιέσεως της πνευμονικής τριχοειδικής ενσφηνώσεως και τελικά η TPG υποδηλώνουν βελτιωμένη πρόγνωση, ιδιαίτερα σε υποψήφιους μεταμόσχευσης καρδιάς.
Το κλινικό ιστορικό, η φυσική εξέταση και η μη επεμβατική αξιολόγηση δεν υποδεικνύουν μια αιτιολογία που θα μπορούσε να προσδιοριστεί εύκολα τόσο στην ενδομυοκαρδιακή βιοψία όσο και στην αλλαγή της θεραπευτικής στρατηγικής. Ως εκ τούτου, σύμφωνα με τις κατευθυντήριες οδηγίες ACC / AHA, δεν επιδιώχθηκε ενδομυοκαρδιακή βιοψία14.
3.2. Παγίδες που Πρέπει να Αποφεύγονται στην Επεμβατική Αξιολόγηση της Καρδιακής Ανεπάρκειας και της Πνευμονικής Υπέρτασης Τύπου II. Υπάρχουν διάφορα κρίσιμα σημεία που πρέπει να ληφθούν υπόψιν κατά την εκτίμηση τόσο της καρδιακής ανεπάρκειας όσο και της πνευμονικής υπέρτασης. Το πρώτο ζήτημα που εξετάζεται είναι η κατάλληλη μέθοδος για τον προσδιορισμό της καρδιακής παροχής. Όπως θα αποδειχθεί στην επόμενη ενότητα, η καρδιακή παροχή χρησιμοποιείται για τον προσδιορισμό της PVR και του βαθμού πρόγνωσης των επιπτώσεων της PVR. Υπάρχουν διάφορες μέθοδοι που χρησιμοποιούνται για τον προσδιορισμό της καρδιακής παροχής στο εργαστήριο επεμβατικής αιμοδυναμικής. Η μέθοδος θερμικής αραίωσης αναλύει τη μεταβολή της θερμοκρασίας του αίματος με την πάροδο του χρόνου μετά την εισαγωγή ενός ψυχρού ενέματος στο σύστημα. Αυτή η μέθοδος έχει τη δυνατότητα να υποεκτιμά την καρδιακή παροχή σε ασθενείς με σημαντικά χαμηλές αποδόσεις έργου ή σοβαρή ανεπάρκεια παλινδρόμησης της τριγλώχινας. Εάν η καρδιακή παροχή έπρεπε να υποτιμηθεί, τότε η πνευμονική αγγειακή αντίσταση θα έπρεπε να υπερεκτιμηθεί. Η εξίσωση Fick χρησιμοποιεί την κατανάλωση οξυγόνου για τον προσδιορισμό της καρδιακής παροχής (εξίσωση που σημειώνεται παρακάτω). Η κατανάλωση οξυγόνου μπορεί να μετρηθεί στο εργαστήριο ή μπορεί να θεωρηθεί ότι βασίζεται στο σωματικό βάρος. Ωστόσο, η υποτιθέμενη τιμή κατανάλωσης οξυγόνου είναι συχνά ανακριβής και θα πρέπει να αποφεύγεται καθώς η δυνητική ανακρίβειά της μπορεί να οδηγήσει σε παραπλανητική PVR.
Δεύτερον, η εκτίμηση του PCWP ως υποκατάστατου της τελικής διαστολικής πίεσης της αριστεράς κοιλίας (LVEDP) έχει αποδειχθεί ότι υποτιμά το πραγματικό LVEDP. Εάν ο χειριστής βασιζόταν αποκλειστικά στο PCWP, τότε ο ασθενής θα μπορούσε να ταξινομηθεί εσφαλμένα ως PΑΗ τύπου Ι όταν όντως είχε PH τύπου II και να ξεκινήσει με μια φαρμακευτική θεραπεία που θα ήταν αναποτελεσματική και πιθανώς ακόμη και επιβλαβής. Μία προηγούμενη έρευνα έδειξε ότι το 53% των περιπτώσεων που ταξινομήθηκαν ως ΡΗ τύπου Ι με βάση ένα χαμηλό PCWP αναταξινομήθηκαν ως ΡΗ τύπου II όταν μετρήθηκε το LVEDP και αποδείχθηκε ότι είναι μεγαλύτερο από 15mmHg15.
Τέλος, θα πρέπει να χρησιμοποιείται προσοχή κατά την εξέταση του κατάλληλου παράγοντα που θα χορηγηθεί κατά τη διάρκεια της μελέτης φαρμάκου. Στο ΡΑΗ τύπου Ι, χορηγείται ένας πνευμονικός αγγειοδιασταλτικός παράγοντας όπως το μονοξείδιο του αζώτου για να καθοριστεί εάν η μέση πνευμονική αρτηριακή πίεση μπορεί να μειωθεί διατηρώντας ή βελτιώνοντας την καρδιακή παροχή. Οι πνευμονικοί αγγειοδιασταλτικοί παράγοντες αυξάνουν το προφορτίο και στον ΠΑΗ τύπο II όπου το LVEDP είναι ήδη αυξημένο, αυτό μπορεί να οδηγήσει σε οξεία υπερφόρτωση όγκου με αποτέλεσμα πνευμονική συμφόρηση. Ο σωστός παράγοντας που χρησιμοποιείται στο μετα-τριχοειδικό ΡΗ (ΡΗ τύπος II) είναι ένας παράγοντας μείωσης του μεταφορτίου, όπως το νιτροπρωσσίδιο. Αυτό θα επιτρέψει στον ερευνητή να προσδιορίσει εάν ο καλύτερος συστηματικός έλεγχος της αρτηριακής πίεσης θα αμβλύνει το αυξημένο LVEDP και με τη σειρά του θα βελτιώσει τη συμπτωματολογία του ασθενούς.
3.3. Αποτελέσματα Καθετηριασμού. Η φλεβική και αρτηριακή πρόσβαση επετευχθει μέσω μιας 7-French δεξιάς φλεβικής φλέβας και 6- French μηριαίας αρτηρίας. Ο αριστερός καθετήρας Judkins 4 και ο δεξιός καθετήρας Judkins 4 χρησιμοποιήθηκαν για να εμπλέξουν το αριστερό και δεξιό στεφανιαίο σύστημα, αντίστοιχα. Η στεφανιαία αγγειογραφία κατέγραψε ήπια διάχυτη νόσο. Ο καθετήρας στη συνέχεια προχώρησε στην αριστερά κοιλία όπου καταγράφηκε τελική διαστολική πίεση 24mmHg.
Ο καθετήρας αποσύρθηκε στην αορτή και μετρήθηκε η αρτηριακή πίεση, όπως σημειώνεται παρακάτω. Η αιμοσφαιρίνη μετρήθηκε και βρέθηκε ότι ήταν 12,4g/dL.
Η κατανάλωση οξυγόνου μετρήθηκε παρά την κλίνη του ασθενούς και ήταν 305.00ml/min. Ο κορεσμός αρτηριακού οξυγόνου ήταν 92% και ο αναμεμειγμένος κορεσμός του φλεβικού αίματος ήταν 45%. Ακολούθως, εισήχθη ένας 7-French 110cm καθετήρας πίεσης με μπαλόνι μέσω του μηριαίου sheath και λήφθηκαν οι ακόλουθες μετρήσεις:
Αορτική πίεση αίματος (mmHg): 144/75 (Σχήμα 6 (c))
Δεξική κολπική πίεση (mmHg): 14/11, μέση τιμή = 10
Δεξιά κοιλιακή πίεση (mmHg): 73/8, τελική διαστολική πίεση = 16
Πίεση πνευμονικής αρτηρίας (mmHg): 72/32, μέσος όρος 49.
Κορεσμός οξυγόνου = 45%
Πίεση πνευμονικής τριχοειδικής ενσφηνώσεως (mmHg): μέση τιμή- 26. Κορεσμός οξυγόνου = 95% (Σχήμα 6 (c))
Καρδιακή παροχή: 3,9 L
Πνευμονική αγγειακή αντίσταση (Μονάδα Woods, WU): 5.96
Χορηγήθηκε νιτροπρωσσίδιον στάγδην 2μg/kg/min και καταγράφηκαν τα επόμενα δεδομένα:
Αορτική πίεση αίματος (mmHg): 92/47
Κορεσμός αρτηριακού οξυγόνου: 97%
Κατανάλωση οξυγόνου: 340,00 ml/λεπτό
Πίεση πνευμονικής αρτηρίας (mmHg): 46/15, μέσος όρος 26.
Κορεσμός οξυγόνου: 73%
Πίεση πνευμονικής τριχοειδικής ενσφηνώσεως (mmHg): 10
Καρδιακή παροχή: 8,3 L
Πνευμονική αγγειακή αντίσταση (Μονάδα Woods, WU): 1.5
Οι αλλαγές στα συστηματικά, MPAP και PCWP καταδεικνύονται στα σχήματα 7 (a) -7 (c).
3.4. Συζήτηση για το Αποτέλεσμα του Καθετηριασμού. Η στεφανιαία αγγειογραφία έδειξε ότι δεν υπάρχει αποφρακτική στεφανιαία νόσος σύμφωνα (συνεπές) με τη διάγνωση της μη ισχαιμικής διαστολής μυοκαρδιοπάθειας.
Οι μετρήσεις πριν από τη χορήγηση νιτροπρωσσίδης επιβεβαιώνουν αξιοσημείωτα αυξημένη πίεση πλήρωσης και χαμηλό CO συνεπές με καρδιακή ανεπάρκεια. Υπάρχει επίσης πνευμονική υπέρταση τύπου II.
Για να εκτιμηθεί καλύτερα η πνευμονική υπέρταση, πρέπει να υπολογιστεί η διαπνευμονική διαβάθμιση:
TPG = MPAP – PCWP, (6)
όπου το TPG είναι ίσο με την διαπνευμονική διαβάθμιση, το MPAP είναι η μέση πνευμονική αρτηριακή πίεση και το PCWP είναι η πίεση της πνευμονικής τριχοειδούς σφήνας. Στην περίπτωσή μας,
TPG = 49 mmHg – 26 mmHg = 23mmHg. (7)
Το TPG είναι ≥12mmHg, το οποίο είναι σύμφωνο με τη μετα-τρικυκλική αντιδραστική πνευμονική υπέρταση, ενώ το μη αντιδραστικό μετατριχοειδικό PH είναι ≤12mmHg. Αυξημένος αγγειοκινητικός τόνος με συνοδευτική αναδιαμόρφωση της πνευμονικής αρτηρίας υπογραμμίζει την παθοφυσιολογία του δραστικού PH13. Δεν είναι σαφές γιατί κάποιοι ασθενείς με ΡΗ τύπου ΙΙ αναπτύσσουν αυξημένο TPG.
Στη συνέχεια, η καρδιακή παροχή πρέπει να υπολογιστεί χρησιμοποιώντας την εξίσωση Fick ως εξής:
CO = VO2 / ((CaO2 – CV02 × 10)),
CaO2 συγκέντρωση αιμοσφαιρίνης (g/dL)
× 1,36ml O2/g αιμοσφαιρίνη
× κορεσμός αρτηριακού οξυγόνου (%), (8)
CV02 συγκέντρωση αιμοσφαιρίνης (g/dL)
× 1,36ml O2/g αιμοσφαιρίνη
× κορεσμός φλεβικού οξυγόνου (%),
όπου το CO είναι η καρδιακή παροχή, το CaO2 είναι η περιεκτικότητα του αρτηριακού αίματος σε οξυγόνο και το CV02 είναι η περιεκτικότητα του φλεβικού αίματος σε οξυγόνο. Η κατανάλωση οξυγόνου δίδεται στα 305ml/min, η αιμοσφαιρίνη χορηγείται στα 12,4g/dL, ο κορεσμός του αρτηριακού οξυγόνου ήταν 92% και ο κορεσμός του φλεβικού οξυγόνου ήταν 45%. Καταχωρώντας αυτά τα δεδομένα, το CO μπορεί να λυθεί για:
CO = 305 / ((15,5 – 7,6) x 10) = 3,86 L/min,
CI = CO / BSA = 3,9 / 1,73 = 2,3 L/min/m2 (9)
Το CO μπορεί στη συνέχεια να χρησιμοποιηθεί για τον προσδιορισμό της πνευμονικής αγγειακής αντίστασης ως εξής:
PVR = (MPAP – PCWP) / CO (10)
όπου το PVR είναι η πνευμονική αγγειακή αντίσταση, το MPAP είναι η μέση πίεση της πνευμονικής αρτηρίας, η MPCWP είναι η μέση πίεση της πνευμονικής τριχοειδικής ενσφηνώσεως και το CO είναι η καρδιακή παροχή. Επομένως, πριν από τη χορήγηση του νιτροπρωσσιδίου, το PVR είναι ίσο
PVR = (49 – 26) / 3,86 = 5,9 WU (11)
Το κανονικό PVR είναι ≤3 WU. Η αυξημένη πνευμονική αγγειακή αντίσταση του ασθενούς είναι σύμφωνη με τον αντιδραστικό PH τύπου II.
Σημειώστε ότι με τη χορήγηση του νιτροπρωσσιδίου, η συστηματική αρτηριακή πίεση μειώθηκε από 144/75mmHg σε 92/47mmHg. Με αυτή την οξεία μείωση μετά την επιβάρυνση, σημειώθηκε αξιοσημείωτη πτώση στο MPAP στα 26mmHg, σστο PCWP στα 10mmHg και το PVR σε 1,5WU. Αυτά τα ευρήματα αντικατοπτρίζουν τις αιμοδυναμικές ενδείξεις που σημειώνονται στα σχήματα 7 (a) -7 (c). Η ανταπόκριση της πνευμονικής αγγειακής αντίστασης υποδηλώνει την αναστρεψιμότητα, υποδηλώνοντας ότι ο υποκείμενος παθοφυσιολογικός μηχανισμός για το αντιδραστικό ΡΗ τύπο II είναι ο αυξημένος αγγειοκινητικός τόνος και όχι η αναδιαμόρφωση13.
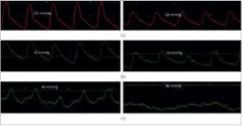
Σχήμα 7: Ανταπόκριση της συστημικής, πνευμονικής αρτηριακής και πνευμονικής πίεσης τριχοειδικής ενσφηνώσεως στο νιτροπρουσσίδιο. Η αορτική πίεση αίματος και κατά συνέπεια η LVEDP μειώθηκε σημαντικά με την εισαγωγή νιτροπρωσσίδης (α). Στη συνέχεια, το MPAP (b) και το PCWP (c) κατέδειξαν σημαντική μείωση των μετρήσεων της πίεσης.
Εξίσου κρίσιμη είναι και η διπλάσια αύξηση του CO από 3,9 σε 8,3 L/λεπτό. Η αύξηση οφείλεται στο αυξημένο VO2 (από 305ml/min σε 340ml/min) καθώς και στην αύξηση του κορεσμού ανάμεικτου φλεβικού οξυγόνου από 45% σε 73%. Το αρτηριακό οξυγόνο επίσης αυξήθηκε από 92% σε 97%. Η καρδιακή παροχή μετά τη χορήγηση του νιτροπρωσσιδίου υπολογίζεται συνεπώς ως εξής:
CO = 340 / ((16,4 – 12,3) × 10) = 8,3 L / λεπτό (12)
3.5. Σύνθεση. Η αιμοδυναμική ανίχνευση της αριστεράς κοιλίας (Σχήμα 6 (c)) είναι σύμφωνη με ένα αυξημένο LVEDP που συσχετίζεται με το ηχοκαρδιογραφικό εύρημα μιας αναλογίας Ε προς e’ 20. Επιπλέον, το “V” που παρατηρήθηκε στην ανίχνευση PCWP (Σχήμα 6 ( c)) είναι συνεπές με την γνωστή μιτροειδική διαταραχή και τις αυξημένες πιέσεις πλήρωσης. Το νιτροπρουσσίδιο μείωσε τη συστηματική αγγειακή αντίσταση και τη μέση αρτηριακή πίεση η οποία μείωσε το LVEDP και βελτίωσε την καρδιακή παροχή.
Η συστολική πίεση της δεξιάς κοιλίας είναι σημαντικά υψηλότερη με την επεμβατική αξιολόγηση (73mmHg) σε σύγκριση με μη επεμβατική αξιολόγηση (39mmHg). Αυτό μπορεί να οφείλεται σε αδυναμία λήψης ενός βέλτιστου σήματος Doppler συνεχούς κύματος ή λόγω ημερήσιας μεταβολής στη συστολική πίεση της δεξιάς κοιλίας. Η συνεχής καθημερινή επεμβατική παρακολούθηση της συστολικής πίεσης της δεξιάς κοιλίας σε ασθενείς με ΡΗ τύπου Ι έχει παρουσιάσει σημαντικές διακυμάνσεις16 και αναμένονται παρόμοιες διακυμάνσεις σε ασθενείς με ΡΗ τύπου II. Οι συνθήκες φόρτωσης μπορούν να επηρεάσουν σε μεγάλο βαθμό τα αποτελέσματα της υπερηχοκαρδιογραφίας Doppler και η υπερηχοκαρδιογραφία άσκησης μπορεί να βοηθήσει αρκετά στην αναγνώριση της πνευμονικής υπέρτασης που προκαλείται από άσκηση και στον καθορισμό των αιτίων της δύσπνοιας.
4. Ανάλυση Υπόθεσης
Ο ασθενής ξεκίνησε σταδιακά με ένα θεραπευτικό σχήμα της καρδιακής ανεπάρκειας που αποτελείται από καρβεδιλόλη 25mg δύο φορές την ημέρα, λισινοπρίλη 20mg ημερησίως, φουροσεμίδη 40mg ημερησίως και σπιρονολακτόνη 25mg ημερησίως. Η διλτιαζέμη διακόπτεται καθώς έχει αρνητική ινοτρόπο δράση. Η αρτηριακή πίεση του ασθενούς παρέμεινε αυξημένη, έτσι προστέθηκαν στο σχήμα η υδραλαζίνη 50mg τρεις φορές ημερησίως και το μονονιτρικό ισοσορβίδιο 30mg ημερησίως. Η τριμηνιαία παρακολούθηση κατέδειξε βελτιωμένο έλεγχο της αρτηριακής πίεσης που συσχετίζεται με αυξημένη ανοχή στην άσκηση.
ΒΙΒΛΙΟΓΡΑΦΙΑ
- S. Go, D. Mozaffarian, V. L. Roger et al., “Heart disease and stroke statistics — 2014 update: a report from the American Heart Association,” Circulation, vol. 129, pp. 399–410, 2014.
- J. J. V. McMurray, “Systolic heart failure,” New England Journal of Medicine, vol. 362, no. 3, pp. 228–238, 2010.
- R. D. S. Watson, C. R. Gibbs, and G. Y. Lip, “ABC of heart failure: clinical features and complications,” BMJ, vol. 320, no. 7229, pp. 236–239, 2000.
- N. Pilatis, L. Jacobs, P. Rerkpattanapipat et al., “Clinical predictors of pulmonary hypertension in patients undergoing liver transplant evaluation,” Liver Transplantation, vol. 6, no. 1, pp. 85–91, 2000.
- A. S. Maisel, J. E. Atwood, and A. L. Goldberger, “Hepatojugular reflux: useful in bedside diagnosis of tricuspid regurgitation,” Annals of Internal Medicine, vol. 101, no. 6, pp. 781-782, 1984.
- A. Verma, A. Meris, H. Skali et al., “Prognostic implications of left ventricular mass and myocardial infarction geometry,” JACC: Cardiovascular Imaging, vol. 1, no. 5, pp. 582–591, 2008.
- R. A. Nishimura and A. J. Tajik, “Evaluation of diastolic filling of the left ventricle in health and disease: Doppler echocardiography by Rosetta Stone’s clinician,” Journal of the American College of Cardiology, vol. 30, no. 1, pp. 8-18, 1997.
- J. K. Oh, S.-J. Park, and S. F. Nagueh, “Established and novel clinical applications of diastolic function assessment by echocardiography,” Circulation: Cardiovascular Imaging, vol. 4, no. 4, pp. 444–455, 2011.
- S. R. Ommen, R. A. Nishimura, C. P. Appleton et al., “Clinical utility of Doppler echocardiography and tissue Doppler imaging in the estimation of left ventricular filling pressures,” Circulation, vol. 102, no. 15, pp. 1788–1794, 2000.
- J. B. Geske, D. C. Scantlebury, J. D. Thomas, and R. A. Nishimura, Hemodynamic evaluation of severe tricuspid regurgitation,” Journal of the American College of Cardiology, vol. 62, no. 20, p. e441, 2013.
- P. J. Currie, J. B. Seward, K.-L. Chan et al., “Continuous-wave Doppler determination of right ventricular pressure: a simultaneous Doppler-catheterization study in 127 patients,” Journal of the American College of Cardiology, vol. 6, no. 4, pp. 750–756, 1985.
- CW Yancy, M. Jessup, B. Bozkurt et al., “2017 ACC / AHA / HFSA focused update of the 2013 ACCF / AHA guide to heart failure management: a report from the American College of Cardiology / American Heart Association Task Force on Clinical Practice Guidelines and Heart Failure Society of America, ”Circulation, vol. 136, no. 6, pp. e137 – e161, 2017.
- N. Galie, M. M. Hoeper, M. Humbert et al., “Guidelines for the diagnosis and treatment of pulmonary hypertension: the task force for the diagnosis and treatment of pulmonary hypertension of the European Society of Cardiology (ESC) and European Respiratory Society (ERS), endorsed by the International Society of Heart and Lung Transplantation (ISHLT), ”European Heart Journal, vol. 30, pp. 2493–2537, 2009.
- L. T. Cooper, K. L. Baughman, A. M. Feldman et al., “The role of endomyocardial biopsy in the management of cardiovascular disease,” Circulation, vol. 116, no. 19, pp. 2216–2233, 2007.
- S. D. Halpern and D. B. Taichman, “Misclassification of pulmonary hypertension due to reliance on pulmonary capillary wedge pressure rather than left ventricular end-diastolic pressure,” Chest, vol. 136, no. 1, pp. 37–43, 2009.
- R. P. Frantz, R. L. Benza, B. Kjellstrom et al., “Continuous hemodynamic monitoring in patients with pulmonary arterial hypertension,” The Journal of Heart and Lung Transplantation, vol. 27, no. 7, pp. 780–788, 2008.









Άφησε σχόλιο